名校
1 . 向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式_______ (如果系数是1,不用填写):

(2)整个过程中的还原剂是_______ 。
(3)把KI换成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2_______ L(标准状况,保留2位小数)。
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式

(2)整个过程中的还原剂是
(3)把KI换成KBr,则CCl4层变为
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2
您最近一年使用:0次
2023-04-26更新
|
296次组卷
|
3卷引用:北京市中国人民大学附属中学2020届高三化学质检试题
名校
2 . 黄铁矿(FeS2,其中铁元素的化合价为+2价)因其浅黄铜色和明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。许多小溪流经黄铁矿,由于黄铁矿暴露在空气中或暴露在含氧的水中,小溪变成酸性。当富含铁的溪水和其它水混合时,溶于水的铁以针铁矿[FeO(OH)]的形式沉淀出来,覆盖小溪的底部,而水仍保持酸性。
(1)写出黄铁矿在溪水中被氧化成Fe2+和SO 的离子方程式
的离子方程式__ 。
(2)写出Fe2+被氧化而生成针铁矿的离子方程式:__ 。
(3)用Fe2(SO4)3水溶液可溶解FeS2(用过的溶液可经简单化学方法处理后转化为Fe2(SO4)3供往复循环使用),写出该反应的化学方程式:__ 。
(1)写出黄铁矿在溪水中被氧化成Fe2+和SO
 的离子方程式
的离子方程式(2)写出Fe2+被氧化而生成针铁矿的离子方程式:
(3)用Fe2(SO4)3水溶液可溶解FeS2(用过的溶液可经简单化学方法处理后转化为Fe2(SO4)3供往复循环使用),写出该反应的化学方程式:
您最近一年使用:0次
名校
3 . 高锰酸钾广泛用作氧化剂。
(1)高锰酸钾在水溶液中放出活性氧,起到消毒作用,同时生成+4价的氢氧化锰和氢氧化钾。若活性氧用[O]来表示,请写出该反应的化学方程式:__ 。
(2)日光对KMnO4的分解有催化作用,所以KMnO4溶液必须保存在棕色瓶中。写出KMnO4见光分解的化学方程式:__ 。(已知KMnO4中的Mn元素全部转化为MnO2)
(1)高锰酸钾在水溶液中放出活性氧,起到消毒作用,同时生成+4价的氢氧化锰和氢氧化钾。若活性氧用[O]来表示,请写出该反应的化学方程式:
(2)日光对KMnO4的分解有催化作用,所以KMnO4溶液必须保存在棕色瓶中。写出KMnO4见光分解的化学方程式:
您最近一年使用:0次
4 . ClO2是一种高效水处理剂,实验室可通过以下反应制得ClO2:KClO3+H2C2O4+H2SO4=ClO2↑+CO2↑+K2SO4+H2O。
(1)配平上述化学方程式___ 。
(2)用双线桥法标出上述反应中电子转移的方向和数目___ 。
(3)上述反应中,发生氧化反应的物质是___ ,被氧化的元素是___ ,还原剂和还原产物的物质的量之比为___ 。
(4)当上述反应中消耗了0.2molH2SO4时,转移的电子数为___ 。
(1)配平上述化学方程式
(2)用双线桥法标出上述反应中电子转移的方向和数目
(3)上述反应中,发生氧化反应的物质是
(4)当上述反应中消耗了0.2molH2SO4时,转移的电子数为
您最近一年使用:0次
名校
解题方法
5 . 氧化还原反应在人类的生产、生活中有着重要的应用:
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: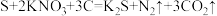 。该反应中,被还原的元素是
。该反应中,被还原的元素是___________ (元素符号),消耗的还原剂和氧化剂质量比为___________ 。
(2)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成球。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)请完成上述火法炼锌反应的化学方程式:ZnCO3+___________ ___________
___________ ___________CO↑,
___________CO↑,___________ ,在该反应中,氧化剂是___________ ,CO是___________ (填“氧化产物”或“还原产物”)。
(3)维生素C又称“抗坏血酸”,在人体内有重要的功能,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
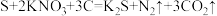 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成球。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)请完成上述火法炼锌反应的化学方程式:ZnCO3+___________
 ___________
___________ ___________CO↑,
___________CO↑,(3)维生素C又称“抗坏血酸”,在人体内有重要的功能,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
您最近一年使用:0次
2021-09-17更新
|
426次组卷
|
3卷引用:江苏省南京市外国语学校2020-2021学年高一上学期化学10月月考化学试卷
名校
解题方法
6 . 消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为_______ ,H2O2被称为“绿色氧化剂”的理由是_______ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为_______ 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______ (用离子方程式表示)。
(5)实验室常用KMnO4和浓盐酸反应制取Cl2,反应的化学方程式为_______ 。被还原的元素是_______ ,还原剂是_______ ,氧化产物是_______ 。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是_______(填序号)。
| A.Cl2 | B.H2O2 | C.ClO2 | D.O3 |
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
(5)实验室常用KMnO4和浓盐酸反应制取Cl2,反应的化学方程式为
您最近一年使用:0次
2021-09-09更新
|
228次组卷
|
3卷引用:湖南省衡阳师范学院祁东附属中学2020-2021学年高三上学期第三次月考化学试题
7 . 某元素X的氧化物很多,其中常见的有A、B两种
(1)A为黄绿色气体,其中X元素在化合物中化合价为+4价,氧含量为47.4%,可用于漂白木浆和水处理,A在液态和浓缩的气态时具有爆炸性,该气体为_______ ;
(2)B为黄棕色气体,氧含量为18.41%,当加热或遇电火花时会发生爆炸,该气体为_______ 。
(3)你认为这两种气体是否可以在防SARS中作为消毒剂_______
(4)写出气体A与NaOH反应的化学方程式_______ 。由于工业上大量使用的A具有爆炸性,A适宜存放在_______ (填“酸”或“碱”)性溶液中。
(5)用SO2还原X的+5价的盐,可制得A,写出该反应的离子方程式_______ 。
(1)A为黄绿色气体,其中X元素在化合物中化合价为+4价,氧含量为47.4%,可用于漂白木浆和水处理,A在液态和浓缩的气态时具有爆炸性,该气体为
(2)B为黄棕色气体,氧含量为18.41%,当加热或遇电火花时会发生爆炸,该气体为
(3)你认为这两种气体是否可以在防SARS中作为消毒剂_______
| A.都可以 | B.都不可以 | C.只有气体A可以 | D.只有气体B可以 |
(5)用SO2还原X的+5价的盐,可制得A,写出该反应的离子方程式
您最近一年使用:0次
8 . 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3 大量地用于电镀工业中。
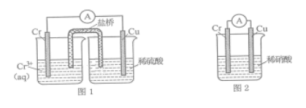
(1)在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体。根据上述现象试推测金属铬的两个重要化学性质___________ 、___________ 。
(2) CrO3 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3 被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为___________ 。
(3) CrO3 的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。
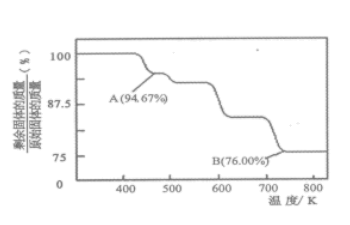
①A点时剩余固体的成分是___________ (填化学式)
②从开始加热到750K 时总反应方程式为___________ 。
(4) CrO3和K2Cr2O7 均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
①电解过程中NaCl的作用是___________ 。
②已知电解后的溶液中c(Fe3+)为2.0×10-13mol·L-1,则溶液中c(Cr3+)为___________ mol·L-1。
(1)在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体。根据上述现象试推测金属铬的两个重要化学性质

(2) CrO3 具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3 被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为
(3) CrO3 的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如下图所示。

①A点时剩余固体的成分是
②从开始加热到750K 时总反应方程式为
(4) CrO3和K2Cr2O7 均易溶于水,这是工业上造成铬污染的主要原因。净化处理方法之一是将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O
 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3 和Cr(OH)3沉淀除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6. 0 × 10-31]。①电解过程中NaCl的作用是
②已知电解后的溶液中c(Fe3+)为2.0×10-13mol·L-1,则溶液中c(Cr3+)为
您最近一年使用:0次
解题方法
9 . 写出下列反应的方程式
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体_______
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质_______
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀_______
(4)金溶解在王水中_______
(1)硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体
(2)氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质
(3)在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀
(4)金溶解在王水中
您最近一年使用:0次
10 . 根据英国地质调查局的报告,我国是世界上锑产量最大的国家,产量占全球的84%。锑在自然界中主要存在于辉锑矿(Sb2S3)中,湖南省冷水江市的锡矿山是世界最大锑矿,估计储量为210万吨。
(1)写出锑原子的核外电子排布,并以此判断其最常见的三个化合价:_______ 。
(2)在一些安全火柴的火柴头中使用了三硫化二锑。写出其燃烧时的化学反应方程式:_______ 。
(3)锑有两种常见氟化物。取其高价态的氟化物,在它的HF溶液中慢慢加入H2O2,得锑含量为44.97%的白色离子化合物A,其阴离子呈八面体结构。A的结构简式为_______ ,A不稳定,易缓慢分解为B和某种气体,写出生成B的化学方程式:_______ 。
(1)写出锑原子的核外电子排布,并以此判断其最常见的三个化合价:
(2)在一些安全火柴的火柴头中使用了三硫化二锑。写出其燃烧时的化学反应方程式:
(3)锑有两种常见氟化物。取其高价态的氟化物,在它的HF溶液中慢慢加入H2O2,得锑含量为44.97%的白色离子化合物A,其阴离子呈八面体结构。A的结构简式为
您最近一年使用:0次



