名校
解题方法
1 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
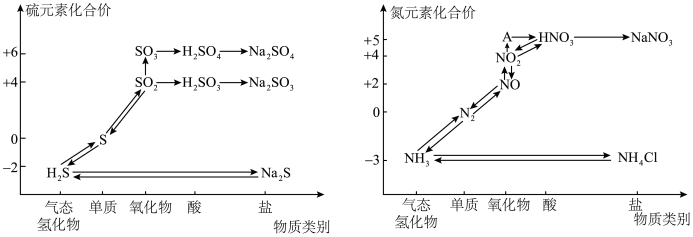
(1)根据 A 对应的化合价和物质类别,A 为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有___________ 。
(2)氮气的结构决定了氮气能够在空气中稳定存在,实验室可用加热 NaNO2与NH4Cl 的混合溶液制备N2,请写出反应的化学方程式___________ 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择___________ ,反应的离子方程式为___________ 。
(4)工业生产中利用氨水吸收SO2 和NO2 ,原理如图所示:
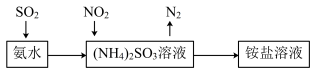
NO2 被吸收过程的离子方程式是___________ 。

(1)根据 A 对应的化合价和物质类别,A 为
(2)氮气的结构决定了氮气能够在空气中稳定存在,实验室可用加热 NaNO2与NH4Cl 的混合溶液制备N2,请写出反应的化学方程式
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(4)工业生产中利用氨水吸收SO2 和NO2 ,原理如图所示:

NO2 被吸收过程的离子方程式是
您最近一年使用:0次
2 . 高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
方法二:Fe(OH)3+KClO+KOH—K2FeO4+KCl+H2O(未配平)
(1)方法一中的氧化产物为_______ (写化学式),将方法一的化学方程式改写为离子方程式_______ ,根据该反应方程式可以判断氧化性强弱:KNO3_______ K2FeO4(填“>”“<”或“=”);
(2)写出方法二配平后的化学方程式_______ ;
(3)利用方法二制备K2FeO4,若有0.2molK2FeO4生成,转移的电子数为_______ mol。
方法一:Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O
方法二:Fe(OH)3+KClO+KOH—K2FeO4+KCl+H2O(未配平)
(1)方法一中的氧化产物为
(2)写出方法二配平后的化学方程式
(3)利用方法二制备K2FeO4,若有0.2molK2FeO4生成,转移的电子数为
您最近一年使用:0次
3 . 唐朝初年,瘟疫频发,人们把它归因于一种叫“年”的怪兽。一位叫李田的人就把硝石、硫磺和木炭装在竹筒里,点燃后驱赶怪兽。后来人们靠此驱散了山林瘴气,战胜了疫情。中国古代四大发明之一的“黑火药”是由“一硫二硝三木炭”混合而成。
(1)写出“黑火药”爆炸的化学反应方程式_______ 。
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的SO2气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是_______ (用文字表述,任写一条合理途径)。
(3)古代曾用硝土[含有 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:

①“反应”过程中的离子反应方程式为_______ 。
②“过滤”操作必须用到的玻璃仪器有烧杯、玻璃棒和_______ ;
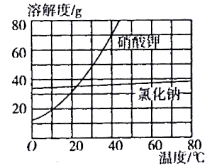
③如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液_______ 、过滤洗涤、干燥等步骤。
(4)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油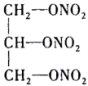 (
(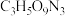 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸),密度是水的1.6倍。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸),密度是水的1.6倍。
①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为_______ ;
②实验室制备硝化甘油的化学方程式为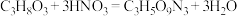 ,用浓硝酸、浓硫酸和甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。
,用浓硝酸、浓硫酸和甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。
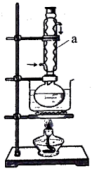
该装置中仪器a名称为_______ ,采用水浴加热而不用酒精灯直接加热的原因是_______ ,从反应后混合溶液中分离硝化甘油的简单方法是_______ 。
(1)写出“黑火药”爆炸的化学反应方程式
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的SO2气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
(3)古代曾用硝土[含有
 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:
①“反应”过程中的离子反应方程式为
②“过滤”操作必须用到的玻璃仪器有烧杯、玻璃棒和
③如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液

(4)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油
 (
(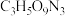 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸),密度是水的1.6倍。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸),密度是水的1.6倍。①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为
②实验室制备硝化甘油的化学方程式为
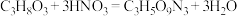 ,用浓硝酸、浓硫酸和甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。
,用浓硝酸、浓硫酸和甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。
该装置中仪器a名称为
您最近一年使用:0次
4 . 化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_______ (填“SiO2”或“Si”);
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为_______ mol •L-1• min-1。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO 2CO2 +
2CO2 + _______ 。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(2)一定条件下,将1 mol N2和3 mol H2置于l L密闭容器中合成 NH3,10 min 后测得H2为 l.2 mol,则用H2 表示该反应的速率为
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO
 2CO2 +
2CO2 +
您最近一年使用:0次
名校
解题方法
5 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
395次组卷
|
3卷引用:湖南省衡阳县第五中学2022-2023学年高一上学期期末考试化学试题
名校
6 . 填空题
(1)现有以下物质:①Al2(SO4)3晶体,②稀盐酸 ,③冰醋酸(固态纯醋酸) ,④石墨, ⑤酒精(C2H5OH),⑥食盐水,⑦葡萄糖(C6H12O6),请回答下列问题:
Ⅰ.以上物质中属于电解质的是_______ (填序号,下同)。
Ⅱ.以上物质中属于非电解质的是_______ 。
Ⅲ.请写出①在水溶液中的电离方程式_______ 。
(2)配平化学方程式:_______ 。_______Cu + _______HNO3(稀)  _______Cu(NO3)2 + _______NO↑+_______H2O
_______Cu(NO3)2 + _______NO↑+_______H2O
(3)新生成的氢氧化亚铁在空气中会迅速变为灰绿色、最后变为红褐色,其过程中涉及到的化学方程式为:_______ 。
(1)现有以下物质:①Al2(SO4)3晶体,②稀盐酸 ,③冰醋酸(固态纯醋酸) ,④石墨, ⑤酒精(C2H5OH),⑥食盐水,⑦葡萄糖(C6H12O6),请回答下列问题:
Ⅰ.以上物质中属于电解质的是
Ⅱ.以上物质中属于非电解质的是
Ⅲ.请写出①在水溶液中的电离方程式
(2)配平化学方程式:
 _______Cu(NO3)2 + _______NO↑+_______H2O
_______Cu(NO3)2 + _______NO↑+_______H2O(3)新生成的氢氧化亚铁在空气中会迅速变为灰绿色、最后变为红褐色,其过程中涉及到的化学方程式为:
您最近一年使用:0次
2022-12-11更新
|
166次组卷
|
3卷引用:湖南省衡阳县第五中学2022-2023学年高一上学期期末考试化学试题
7 . 磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_______ ,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为_______ 杂化,该反应的另一种产物的化学式为_______ 。
(2) 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:_______ 。

(3)工业制备 的流程如图所示。
的流程如图所示。

① 次磷酸属于_______ 元酸。
② 白磷和烧碱溶液反应的化学方程式为:_______ 。
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成_______ mol  (不考虑产物损失)
(不考虑产物损失)
(1)磷元素在元素周期表中的位置:
(2)
 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:
(3)工业制备
 的流程如图所示。
的流程如图所示。
① 次磷酸属于
② 白磷和烧碱溶液反应的化学方程式为:
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成
 (不考虑产物损失)
(不考虑产物损失)
您最近一年使用:0次
8 . 氧化还原反应在物质制取和转化中有重要的应用。请回答下列问题:
(1)Ca(NO2)2(亚硝酸钙)可用作混凝土中钢筋的防护剂,实验室可用如下反应制备:Ca(NO3)2+2CaFe2O4+4NO 3Ca(NO2)2+2Fe2O3。
3Ca(NO2)2+2Fe2O3。
①该反应中的氧化剂是_____ (填化学式,下同),还原剂是_____ 。
②该反应中被氧化的N原子与被还原的N原子的质量之比为____ 。
③用单线桥标出该反应中电子的转移情况:____ 。
(2)某反应体系有反应物和生成物共7种:O2、KMnO4、MnSO4、H2SO4、H2O2、K2SO4。已知该反应中H2O2只发生如下过程:H2O2→O2,试回答下列问题:
①该反应中,发生还原反应的过程是_____ →_____ (填化学式)。
②写出该反应的化学方程式并配平:_____ 。
③若反应消耗2 mol KMnO4,则转移电子的物质的量为_____ mol。
(1)Ca(NO2)2(亚硝酸钙)可用作混凝土中钢筋的防护剂,实验室可用如下反应制备:Ca(NO3)2+2CaFe2O4+4NO
 3Ca(NO2)2+2Fe2O3。
3Ca(NO2)2+2Fe2O3。①该反应中的氧化剂是
②该反应中被氧化的N原子与被还原的N原子的质量之比为
③用单线桥标出该反应中电子的转移情况:
(2)某反应体系有反应物和生成物共7种:O2、KMnO4、MnSO4、H2SO4、H2O2、K2SO4。已知该反应中H2O2只发生如下过程:H2O2→O2,试回答下列问题:
①该反应中,发生还原反应的过程是
②写出该反应的化学方程式并配平:
③若反应消耗2 mol KMnO4,则转移电子的物质的量为
您最近一年使用:0次
9 . I.氧化还原反应与离子反应在生产生活与科学实验中有重要作用,过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.H2O2+2FeSO4+H2SO4=Fe2(SO4)3+2H2O
(1)上述反应中,H2O2仅体现氧化性的反应是_______ (填字母序号,下同),H2O2既体现氧化性又体现还原性的反应是_______ ,H2O2、Ag2O、Fe2(SO4)3的氧化性由强到弱的顺序是_______ 。
(2)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为_______ 。
II.KMnO4在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
①将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色(K2MnO4)熔融态物质。
②冷却,将固体研细,用KOH溶液浸取,过滤,得暗绿色溶液。
③向暗绿色溶液中通入Cl2,溶液变为紫红色。
④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(3)①中生成K2MnO4的化学方程式是_______ 。
(4)②中浸取时用KOH溶液的原因是_______ 。
(5)③中产生两种盐,写出③的方程式,并用单线桥 标出电子转移_______ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.H2O2+2FeSO4+H2SO4=Fe2(SO4)3+2H2O
(1)上述反应中,H2O2仅体现氧化性的反应是
(2)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:Fe3+、Mn2+、MnO
 、H2O、Fe2+、H+,则反应的离子方程式为
、H2O、Fe2+、H+,则反应的离子方程式为II.KMnO4在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
①将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色(K2MnO4)熔融态物质。
②冷却,将固体研细,用KOH溶液浸取,过滤,得暗绿色溶液。
③向暗绿色溶液中通入Cl2,溶液变为紫红色。
④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(3)①中生成K2MnO4的化学方程式是
(4)②中浸取时用KOH溶液的原因是
(5)③中产生两种盐,写出③的方程式,并用
您最近一年使用:0次
名校
解题方法
10 . 元素铬(Cr)的几种化合物存在下列转化关系,依据题目信息,回答下列问题:
(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质。例如,在如图有编号的步骤中:

a反应中Na2Cr2O7是____ (填“氧化剂”或“还原剂”),图中发生氧化反应的步骤是____ (填字母,下同),既没发生氧化反应又没发生还原反应的是____ 。
(2)某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是____ 。
②该反应中,发生还原反应的过程是____ →____ 。
③写出该反应的化学方程式:____ 。
(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质。例如,在如图有编号的步骤中:

a反应中Na2Cr2O7是
(2)某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式:
您最近一年使用:0次



