2022高三·全国·专题练习
1 . 以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。工艺流程如下:
颜料。工艺流程如下:
(1)红渣的主要成分为_______ (填化学式),滤渣①的主要成分为_______ (填化学式)。
(2)黄铁矿研细的目的是_______ 。
(3)还原工序中,不生成S单质的反应的化学方程式为_______ 。
(4)工序①的名称为_______ ,所得母液循环使用。
(5)沉铁工序产生的白色沉淀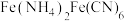 中
中 的化合价为
的化合价为_______ ,氧化工序发生反应的离子方程式为_______ 。
(6)若用还原工序得到的滤液制备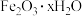 和
和 ,所加试剂为
,所加试剂为_______ 和_______ (填化学式,不引入杂质)。
 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。工艺流程如下:
颜料。工艺流程如下: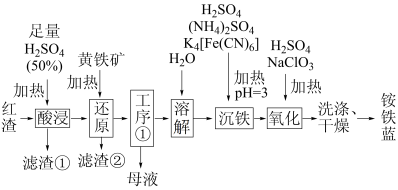
(1)红渣的主要成分为
(2)黄铁矿研细的目的是
(3)还原工序中,不生成S单质的反应的化学方程式为
(4)工序①的名称为
(5)沉铁工序产生的白色沉淀
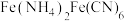 中
中 的化合价为
的化合价为(6)若用还原工序得到的滤液制备
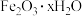 和
和 ,所加试剂为
,所加试剂为
您最近一年使用:0次
2022-07-01更新
|
10303次组卷
|
21卷引用:专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)
(已下线)专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)(已下线)专题15 工艺流程题-2022年高考真题模拟题分项汇编(已下线)2022年新高考河北省高考真题化学试题(部分试题)(已下线)第09讲 铁及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)2022年河北省高考真题化学试题(已下线)易错点32 物质的分离、提纯与检验-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十 工艺流程中的新工艺河北省衡水阳光中学2022-2023学年高二上学期第一次阶段考试化学试题(已下线)2022年河北省高考真题变式题(14-18)第一部分 命题热点剖析——知晓高考新方向 剖析工艺流程题命题热点 构建高效解题思维模型(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)陕西省渭南市2023届高三第一次教学质量检测(一模)化学试题(已下线)第6讲 铁及其重要化合物(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)四川省成都市第七中学2023-2024学年高二上学期10月月考化学试题吉林省长春外国语学校2023-2024学年高三上学期9月月考化学试题(已下线)工业流程题吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷 湖南省浏阳景雅高级中学2024届高三下学期5月全真仿真模拟考试化学试题
2022高三·全国·专题练习
真题
解题方法
2 . 实验室以二氧化铈( )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:

(1)“酸浸”时 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(2)pH约为7的 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为
的加料方式为_______ (填序号)。
A.将 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
 (水层)+3HA(有机层)
(水层)+3HA(有机层)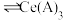 (有机层)+
(有机层)+ (水层)
(水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______ 。
②反萃取的目的是将有机层 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有_______ (填两项)。
③与“反萃取”得到的水溶液比较,过滤 溶液的滤液中,物质的量减小的离子有
溶液的滤液中,物质的量减小的离子有_______ (填化学式)。
(4)实验中需要测定溶液中 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取
。请补充完整实验方案:①准确量取 溶液[
溶液[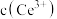 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将
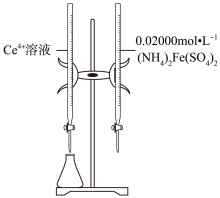
容量瓶中后定容;②按规定操作分别将 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③_______ 。
 )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
(1)“酸浸”时
 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为(2)pH约为7的
 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为
的加料方式为A.将
 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中(3)通过中和、萃取、反萃取、沉淀等过程,可制备
 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (水层)+3HA(有机层)
(水层)+3HA(有机层)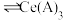 (有机层)+
(有机层)+ (水层)
(水层)①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
②反萃取的目的是将有机层
 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有③与“反萃取”得到的水溶液比较,过滤
 溶液的滤液中,物质的量减小的离子有
溶液的滤液中,物质的量减小的离子有(4)实验中需要测定溶液中
 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取
。请补充完整实验方案:①准确量取 溶液[
溶液[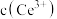 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将
容量瓶中后定容;②按规定操作分别将 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③
您最近一年使用:0次
2022-07-21更新
|
7872次组卷
|
13卷引用:专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)
(已下线)专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题14-17(已下线)易错点33 物质的制备-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十三 实验探究中的新思路(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)江苏省2022年普通高中学业水平选择性考试变式题(实验探究题)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第30讲水的电离和溶液的酸碱性(已下线)题型四 以无机物制备为载体的综合实验-备战2024年高考化学答题技巧与模板构建
名校
解题方法
3 . 碳酸镍是合成纳米镍的一种前驱体。一种用铁镍合金废料(还含有少量铜、钙、镁、硅的氧化物)制备纯度较高的碳酸镍的工艺流程如图:

已知:H2S的电离常数 ,
,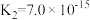 ,
,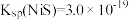 ;
;
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸:
①金属镍溶解的离子方程式是_______ 。
②“酸溶”时产生的废渣成分有_______ 。
③该过程控制温度70℃-80℃的原因是_______ 。
(2)“除铁”时,将“铁”转化成颗粒较大的黄钠铁矾[NaFe3(SO4)2(OH)6]沉淀对后续操作较为有利:
①黄钠铁矾中Fe元素的化合价为_______ 。
②“除铁”加入Na2CO3时,生成黄钠铁矾的离子方程式是_______ 。
(3)“除铜”后,溶液中c(H2S)=0.1mol·L-1,c(Ni2+)=0.1mol·L-1,溶液中c(H+) ≥_______ mol·L-1(列计算式)才不会使Ni2+形成NiS沉淀。
(4)“沉镍”后,滤液的主要成分是_______ 。
(5)“沉镍”时,若用Na2CO3溶液做沉淀剂,产物容易不纯,该杂质的化学式为_______ 。

已知:H2S的电离常数
 ,
,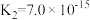 ,
,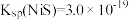 ;
;回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸:
①金属镍溶解的离子方程式是
②“酸溶”时产生的废渣成分有
③该过程控制温度70℃-80℃的原因是
(2)“除铁”时,将“铁”转化成颗粒较大的黄钠铁矾[NaFe3(SO4)2(OH)6]沉淀对后续操作较为有利:
①黄钠铁矾中Fe元素的化合价为
②“除铁”加入Na2CO3时,生成黄钠铁矾的离子方程式是
(3)“除铜”后,溶液中c(H2S)=0.1mol·L-1,c(Ni2+)=0.1mol·L-1,溶液中c(H+) ≥
(4)“沉镍”后,滤液的主要成分是
(5)“沉镍”时,若用Na2CO3溶液做沉淀剂,产物容易不纯,该杂质的化学式为
您最近一年使用:0次
2022-03-07更新
|
1830次组卷
|
4卷引用:广东省广州市执信中学2022届高三下学期联考化学试题
广东省广州市执信中学2022届高三下学期联考化学试题广东广雅中学2023届高三下学期2月阶段测试化学试题(已下线)专题16 工艺流程题-三年(2020-2022)高考真题分项汇编(已下线)微专题26 化学工艺流程题-----核心反应与条件控制-备战2023年高考化学一轮复习考点微专题
4 . 市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:
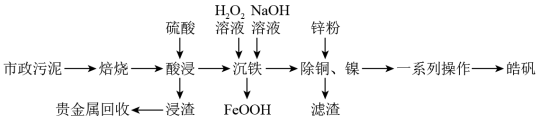
已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有___________ (任写一条)。
(2)“一系列操作”主要包括___________ 、___________ 、过滤、洗涤,干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为___________ 。
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:_______ ,则反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为_______ 。pH对不同金属沉出率的影响如图所示,则“沉铁’时最合理的pH约为_______ 。在pH<6时,Zn2+、Cu2+、Ni2+在溶液中以离子形式存在,但是有铁离子存在时,pH升高,Zn、Cu、Ni损失率均升高,原因可能是_______ 。
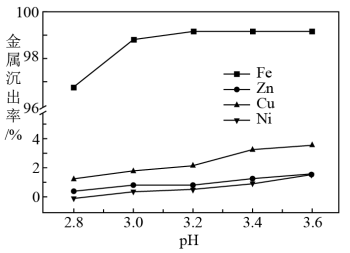

已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)“一系列操作”主要包括
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为
(4)“浸渣”中含有Ag2S,经一系列处理得Ag(NH3)2Cl(可溶于水,电离成[Ag(NH3)2]+和Cl-},用肼(N2H4)还原Ag(NH3)2Cl得到单质银,N2H4的氧化产物为N2,写出该反应的离子方程式:
(5)浸出液中含有Fe2+,“沉铁”步骤中发生反应的离子方程式为

您最近一年使用:0次
2022-01-11更新
|
1501次组卷
|
5卷引用:广东省清远市2021-2022学年高三上学期期末教学质量检测化学试题
名校
5 . 半导体芯片行业是金属靶材的主要应用领域之一。利用镍铂靶材废料(主要成分为Ni、Pt以及微量Fe、Al的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如下:

已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
②王水是按浓盐酸和浓硝酸的体积比为3∶1配制而成;
③氧化性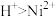
④室温: ;
;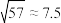
(1)“酸浸”时镍发生反应的化学方程式为_______ 。
(2)铂在王水中生成二元强酸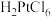 ,其中Pt元素的化合价为
,其中Pt元素的化合价为_______ ,该反应的离子方程式为_______ 。
(3)设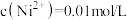 “调pH”应控制的pH范围是
“调pH”应控制的pH范围是_______ 。
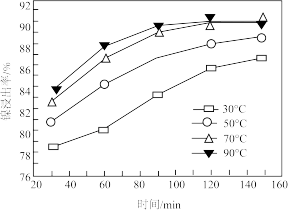
(4)当液固比为4∶1时,"酸浸"过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳温度和时间是_______ 。
(5)沉铂过程中, 的沉淀率随温度的升高而增大,结合平衡移动原理解释
的沉淀率随温度的升高而增大,结合平衡移动原理解释 沉淀率随温度变化的主要原因
沉淀率随温度变化的主要原因_______ 。
(6)在“沉铂”过程中,若向 的溶液里加入等体积的
的溶液里加入等体积的 溶液,使
溶液,使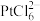 沉淀完全,则加入
沉淀完全,则加入 溶液的浓度最小值为
溶液的浓度最小值为_______ mol/L(结果保留两位小数,忽略溶液混合后体积的变化)。
(7)“操作1”中包括沉淀的洗涤,应选用下列哪种试剂最佳_______。

已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ |  |  |  |
| 开始沉淀时(c=0.01mol/L)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 (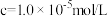 )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
③氧化性
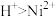
④室温:
 ;
;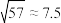
(1)“酸浸”时镍发生反应的化学方程式为
(2)铂在王水中生成二元强酸
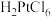 ,其中Pt元素的化合价为
,其中Pt元素的化合价为(3)设
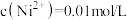 “调pH”应控制的pH范围是
“调pH”应控制的pH范围是(4)当液固比为4∶1时,"酸浸"过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳温度和时间是

(5)沉铂过程中,
 的沉淀率随温度的升高而增大,结合平衡移动原理解释
的沉淀率随温度的升高而增大,结合平衡移动原理解释 沉淀率随温度变化的主要原因
沉淀率随温度变化的主要原因(6)在“沉铂”过程中,若向
 的溶液里加入等体积的
的溶液里加入等体积的 溶液,使
溶液,使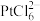 沉淀完全,则加入
沉淀完全,则加入 溶液的浓度最小值为
溶液的浓度最小值为(7)“操作1”中包括沉淀的洗涤,应选用下列哪种试剂最佳_______。
| A.蒸馏水 | B.浓盐酸 | C.氯化铵溶液 | D.王水 |
您最近一年使用:0次
2022-04-29更新
|
1502次组卷
|
4卷引用:广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题
广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题(已下线)押广东卷化学第18题 化学工艺流程题-备战2022年高考化学临考题号押题(广东卷)湖南省衡山县岳云中学2021-2022学年高三下学期期中考试化学试卷(已下线)2022年全国乙卷高考变式题(非选择题)
名校
解题方法
6 . 镍是重要的战略金属资源,一种从某高镁低品位铜镍矿(主要成分为CuFeS2、FeS2、3NiO●4SiO2●H2O、3MgO●4SiO2●H2O等)中回收Cu、Ni的工艺流程如图所示:
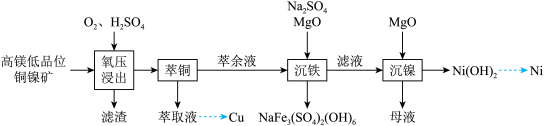
回答下列问题:
(1)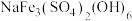 中,
中, 元素的化合价为
元素的化合价为_______ 。
(2)为提高“氧压浸出”的速率,可行的操作有_______ (任填一个)。
(3)“氧压浸出”的滤渣有S和_______ ,该环节中 发生的化学反应方程式为
发生的化学反应方程式为_______ 。
(4)“萃铜”时的反应为: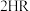 (有机相)
(有机相)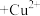 (水相)
(水相)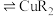 (有机相)
(有机相) (水相),下列说法正确的有_______。
(水相),下列说法正确的有_______。
(5)已知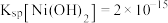 ,“滤液”中
,“滤液”中 ,“沉镍”时,控制
,“沉镍”时,控制 为8.50,此时
为8.50,此时 的沉淀率为
的沉淀率为_______ ,“沉镍”后的母液,含有的主要溶质为_______ (填化学式)。

回答下列问题:
(1)
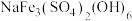 中,
中, 元素的化合价为
元素的化合价为(2)为提高“氧压浸出”的速率,可行的操作有
(3)“氧压浸出”的滤渣有S和
 发生的化学反应方程式为
发生的化学反应方程式为(4)“萃铜”时的反应为:
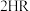 (有机相)
(有机相)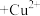 (水相)
(水相)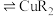 (有机相)
(有机相) (水相),下列说法正确的有_______。
(水相),下列说法正确的有_______。A.向萃取液中加入稀硫酸进行“反萃取”,可得到单质 |
B.萃余液中的阳离子为: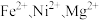 |
C.一定条件下,萃取平衡时,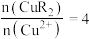 ,则 ,则 的萃取率为80% 的萃取率为80% |
D.为提高 的萃取率,可适当提高溶液 的萃取率,可适当提高溶液 |
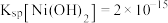 ,“滤液”中
,“滤液”中 ,“沉镍”时,控制
,“沉镍”时,控制 为8.50,此时
为8.50,此时 的沉淀率为
的沉淀率为
您最近一年使用:0次
2023-02-09更新
|
1282次组卷
|
3卷引用:广东省佛山市2023届普通高中教学质量检测(一)化学试题
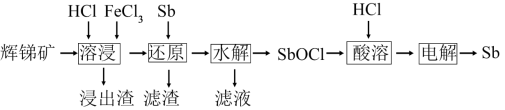
7 . 锑(Sb)可用作阻燃剂、电极材料、催化剂等物质的原材料。一种以辉锑矿(主要成分为Sb2S3,还含有Fe2O3、Al2O3、MgO、SiO2等)为原料提取锑的工艺如下:
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“溶浸”时氧化产物是S,Sb2S3被氧化的化学方程式为___________ 。
(2)“还原”时加入Sb的目的是将___________ 还原,提高产物的纯度。
(3)“水解”时需控制溶液pH=2.5。
①Sb3+发生水解的离子方程式为___________ 。
②下列能促进该水解反应的措施有___________ (填字母)。
A.升高温度 B.增大c(H+) C.增大c(Cl-) D.加入Na2CO3粉末
③为避免水解产物中混入Fe(OH)3,Fe3+浓度应小于___________ mol·L-1。
(4)“滤液”中含有的金属阳离子有___________ 。向“滤液”中通入足量___________ (填化学式)气体,再将滤液pH调至3.5,可析出Fe(OH)3沉淀。将沉淀溶于浓盐酸后,产物可返回___________ 工序循环使用。
(5)Sb可由SbCl 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为___________ 。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 2.2 | 3.7 | 7.5 | 9.6 |
| 完全沉淀时(c=1.0×10-5mol·L-1)的pH | 3.2 | 4.7 | 9.0 | 11.1 |
(1)“溶浸”时氧化产物是S,Sb2S3被氧化的化学方程式为
(2)“还原”时加入Sb的目的是将
(3)“水解”时需控制溶液pH=2.5。
①Sb3+发生水解的离子方程式为
②下列能促进该水解反应的措施有
A.升高温度 B.增大c(H+) C.增大c(Cl-) D.加入Na2CO3粉末
③为避免水解产物中混入Fe(OH)3,Fe3+浓度应小于
(4)“滤液”中含有的金属阳离子有
(5)Sb可由SbCl
 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为
您最近一年使用:0次
2022-03-17更新
|
1530次组卷
|
4卷引用:广东省广州市2022届高三一模考试化学试题
名校
解题方法
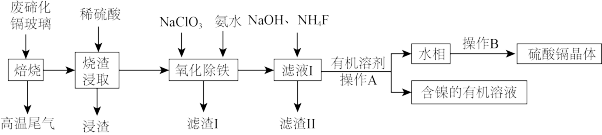
8 . 碲化镉玻璃中主要含有CdTe(其中含有少量Fe、Ni、Mg、Si、O等元素组成的化合物),工业上利用废弃碲化镉(CdTe)玻璃回收其中金属的工艺流程如下。
已知:①常温时,有关物质的 如下表。
如下表。
②当溶液中离子浓度小于 时,可认为沉淀完全。
时,可认为沉淀完全。
回答下列问题:
(1)在“焙烧”时为提高效率可采用的措施有_______ (答出一条即可)。写出“浸渣”的工业用途:_______ 。
(2)实验室中,“操作A”需要的玻璃仪器有_______ 。“高温尾气”中的 在水溶液中可用
在水溶液中可用 将其还原为Te单质,写出该反应的化学方程式:
将其还原为Te单质,写出该反应的化学方程式:_______ 。
(3)“氧化除铁”步骤中可以先调节pH为5,然后再加入 ,则此时
,则此时 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)测得“滤液I”中 浓度为
浓度为 ,取1L滤液,则至少加入
,取1L滤液,则至少加入_______ g 固体才能使
固体才能使 沉淀完全。
沉淀完全。
(5)取1吨含碲化镉80%的废弃玻璃,最终回收得到0.64吨 ,则硫酸镉的回收率为
,则硫酸镉的回收率为_______ (保留三位有效数字)。

已知:①常温时,有关物质的
 如下表。
如下表。 |  |  |  |  |
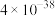 | 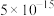 | 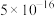 |  | 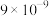 |
 时,可认为沉淀完全。
时,可认为沉淀完全。回答下列问题:
(1)在“焙烧”时为提高效率可采用的措施有
(2)实验室中,“操作A”需要的玻璃仪器有
 在水溶液中可用
在水溶液中可用 将其还原为Te单质,写出该反应的化学方程式:
将其还原为Te单质,写出该反应的化学方程式:(3)“氧化除铁”步骤中可以先调节pH为5,然后再加入
 ,则此时
,则此时 被氧化的离子方程式为
被氧化的离子方程式为(4)测得“滤液I”中
 浓度为
浓度为 ,取1L滤液,则至少加入
,取1L滤液,则至少加入 固体才能使
固体才能使 沉淀完全。
沉淀完全。(5)取1吨含碲化镉80%的废弃玻璃,最终回收得到0.64吨
 ,则硫酸镉的回收率为
,则硫酸镉的回收率为
您最近一年使用:0次
2022-11-04更新
|
1356次组卷
|
4卷引用:广东省2023届高三一轮复习联考(二)广东卷化学试题
广东省2023届高三一轮复习联考(二)广东卷化学试题广东省部分学校2022-2023学年高三上学期一轮复习联考(二)化学试题(已下线)热点情景汇编-专题十 工艺流程中的新工艺福建省惠安第一中学2022-2023学年高三上学期第三次月考化学试题
9 . N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH− 2
2 +H2O
+H2O
2NO2+2OH−
 +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl−和 ,其离子方程式为
,其离子方程式为________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________ 。

(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH−
 2
2 +H2O
+H2O2NO2+2OH−

 +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。①在酸性NaClO溶液中,HClO氧化NO生成Cl−和
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是

您最近一年使用:0次
2019-06-10更新
|
7404次组卷
|
32卷引用:广东省潮州市饶平县第二中学2021-2022学年高一下学期月考(一)化学试题
广东省潮州市饶平县第二中学2021-2022学年高一下学期月考(一)化学试题2019年江苏省高考化学试题湖南省长沙市第一中学2020届高三第一次月考化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——氮及其氧化物的性质(提升练)2019-2020学年新人教版必修2第5章第2节《氮及其化合物》作业专题3.2 非金属及其化合物(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升第2章 化学键化学反应规律 模拟高考——C挑战区 夯实基础(鲁科版(2019)第二册)第2章 化学键 化学反应与能量 模拟高考——C挑战区 夯实基础(鲁科版必修2)专题4 化学科学与人类文明——C挑战区 模拟高考(苏教版必修2)江苏省苏州新草桥中学2020届高三上学期10月月考化学试题(已下线)2020年高考化学押题预测卷01(新课标Ⅰ卷)--《2020年高考押题预测卷》(已下线)专题6.3 化学原理题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升江苏省扬州市江都区大桥高级中学2019-2020学年高二下学期期中考试化学试题江苏省启东中学2021届高三上学期期初考试化学试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关专题7 第三单元综合拔高练-高中化学必修第二册苏教版2019人教版2019必修第二册 第五章 第二~三节综合拔高练江苏省苏州市工业园区星海实验中学高一下学期3月月考化学试题(已下线)【苏州新东方】04 吴县中学重庆市凤鸣山中学2020-2021学年高一下学期期中考试化学试题湖北省广水市普通中学2020-2021学年高一下学期5月月考化学试题(已下线)第12讲 氮及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)海南省海南枫叶国际学校2021-2022学年高三上学期第三次月考(1月)化学试题黑龙江省大庆市第四中学2018-2019学年高二下学期第三次月考化学试题(已下线)专题17 原理综合题(已下线)常见无机物的性质江苏省镇江市句容市南京人民中学等三市四校联考2022-2023学年高一下学期4月月考化学试题湖北省黄石市第二中学2023-2024学年高二上学期第三次统测化学试题江苏省常州市联盟校2023-2024学年高一下学期3月阶段调研化学试题江苏省南京市金陵中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
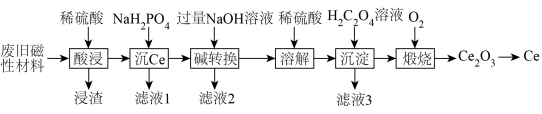
10 . 稀土金属(RE)属于战略性金属,我国的稀土提炼技术位于世界领先地位。一种从废旧磁性材料[主要成分为铈(Ce)、Al、Fe和少量不溶于酸的杂质]中回收稀土金属Ce的工艺流程如图所示。
(1)为提高酸浸的速率,可采取的措施为___________ (写一条即可)。
(2)常温下,“酸浸”后测得溶液中c(Fe2+)=1.0mol/L,c(Ce3+)=0.01mol/L,则“沉Ce”时,为了使Al3+完全沉淀,但不引人Fe(OH)2和Ce(OH)3,需要调节溶液的pH范围为___________ 。
(3)“碱转换”过程中Ce(H2PO4)所发生反应的离子方程式为___________ ,“滤液2”中铝元素的存在形式为___________ (填化学式)。
(4)“沉淀”后所得的固体为Ce2(C2O4)3·10H2O,将其煅烧可得Ce2O3和一种无毒的气体,发生反应的化学方程式为___________ 。
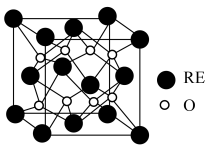
(5)某稀土金属氧化物的立方晶胞如图所示,则该氧化物的化学式为___________ ,距离RE原子最近的O原子有___________ 个。若M(晶胞)=Mg/mol,晶胞边长为anm,NA为阿伏加德罗常数的值,则晶胞的密度为___________ g/cm3(列出计算式)。
(1)为提高酸浸的速率,可采取的措施为
(2)常温下,“酸浸”后测得溶液中c(Fe2+)=1.0mol/L,c(Ce3+)=0.01mol/L,则“沉Ce”时,为了使Al3+完全沉淀,但不引人Fe(OH)2和Ce(OH)3,需要调节溶液的pH范围为
(3)“碱转换”过程中Ce(H2PO4)所发生反应的离子方程式为
(4)“沉淀”后所得的固体为Ce2(C2O4)3·10H2O,将其煅烧可得Ce2O3和一种无毒的气体,发生反应的化学方程式为
(5)某稀土金属氧化物的立方晶胞如图所示,则该氧化物的化学式为
您最近一年使用:0次
2024-03-31更新
|
1063次组卷
|
4卷引用:2024届广东省肇庆市高三上学期二模化学试题
2024届广东省肇庆市高三上学期二模化学试题(已下线)化学(广东卷02)-2024年高考押题预测卷2024届广东省梅州市兴宁市第一中学高三下学期二模化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)



