1 .  是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备
是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备 (熔点:―76℃,沸点:138℃)。下列说法错误的是
(熔点:―76℃,沸点:138℃)。下列说法错误的是
 是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备
是一种橙红色液体,易水解产生使品红溶液褪色的气体,常作橡胶工业的硫化剂。某同学设计如图装置制备 (熔点:―76℃,沸点:138℃)。下列说法错误的是
(熔点:―76℃,沸点:138℃)。下列说法错误的是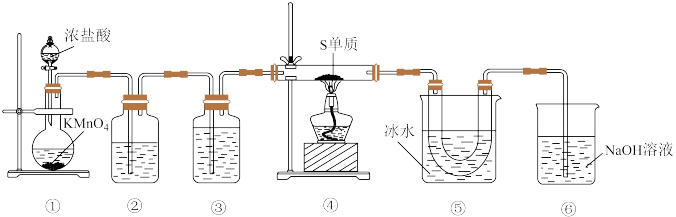
A. 分子中含有非极性共价键 分子中含有非极性共价键 |
B.装置②③中分别装有饱和 溶液、浓硫酸 溶液、浓硫酸 |
C.制备 的过程中可能发生反应: 的过程中可能发生反应: |
| D.该实验装置中有一处明显缺陷,可将装置⑥换成装有碱石灰的球形干燥管 |
您最近半年使用:0次
解题方法
2 . 下列离子方程式书写正确的是
A. 溶液与过量 溶液与过量 溶液混合: 溶液混合: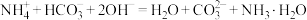 |
B.向 溶液中滴加 溶液中滴加 溶液: 溶液: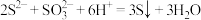 |
C.向AgCl悬浊液中滴入饱和NaBr溶液: |
D.少量铁粉与稀硝酸反应: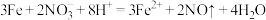 |
您最近半年使用:0次
3 .  催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是
 催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是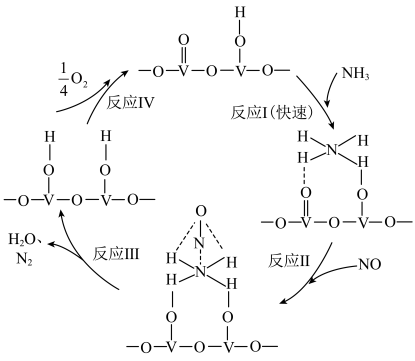
| A.该历程中能垒最高的是反应I |
| B.该历程中,V元素被氧化的只有反应Ⅳ |
C.该催化反应的总反应式为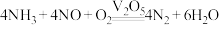 |
| D.整个历程中涉及极性键和非极性键的断裂和形成 |
您最近半年使用:0次
4 . 下列叙述对应的离子方程式正确的是
A.向 溶液中滴加稀氨水: 溶液中滴加稀氨水: |
B.向苯酚钠溶液中通入少量CO2: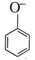 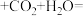 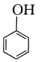 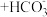 |
C.酸性 溶液氧化 溶液氧化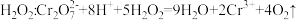 |
D. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
您最近半年使用:0次
解题方法
5 . 二氧化氯(ClO2)是一种高效、安全的杀菌消毒剂。一种综合法制备ClO2的工艺流程及ClO2分子的结构(O-Cl-O的键角为117.6°)如图所示。
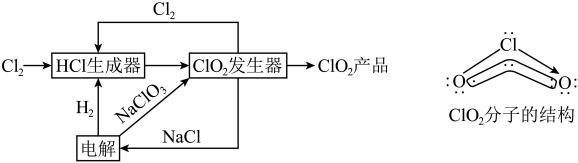
| A.Cl2与ClO2分子中所含化学键类型完全相同 |
B. ClO2分子中含有大π键(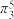 ),Cl原子杂化方式为sp2杂化 ),Cl原子杂化方式为sp2杂化 |
| C.“ClO2发生器”中,NaClO3的还原产物为Cl2 |
| D.“电解”时,阳极与阴极产物的物质的量之比为3:1 |
您最近半年使用:0次
解题方法
6 . 下列离子方程式书写错误的是
A.向银氨溶液中滴入乙醛: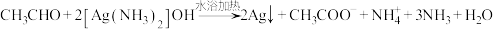 |
B.向硫代硫酸钠溶液中加入稀硫酸: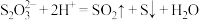 |
C.向漂白粉溶液中通入少量 : :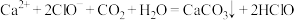 |
D.向加有 的 的 溶液中通入 溶液中通入 : :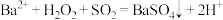 |
您最近半年使用:0次
解题方法
7 . 碱金属和碱土金属元素分别位于元素周期表的ⅠA族和ⅡA族,它们的化合物应用广泛。历史上曾以NaCl为原料生产NaOH作为化学工业开端的标志。 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。
碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
A.侯氏制碱法中的物质转化: |
B.由 制备乙酸的物质转化: 制备乙酸的物质转化: |
C.电解饱和NaCl溶液的阴极反应: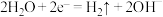 |
D. 与 与 共熔的反应: 共熔的反应: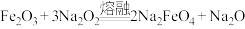 |
您最近半年使用:0次
昨日更新
|
139次组卷
|
2卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
解题方法
8 . 从电子废料(含Au、Ag和Cu等)中可回收金,主要流程如下: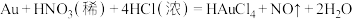
下列说法不正确 的是
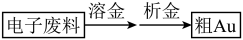
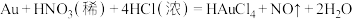
下列说法
A.浓盐酸促进了Au和 的反应,其原因是降低了 的反应,其原因是降低了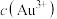 ,增强了Au的还原性 ,增强了Au的还原性 |
B.依据王水溶金原理,NaCN饱和溶液与 也可使Au溶解 也可使Au溶解 |
C. 可实现析金发生反应: 可实现析金发生反应: |
D.以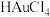 为电解质进行粗金的电解精炼,可能会有AgCl覆盖在阴极发生钝化 为电解质进行粗金的电解精炼,可能会有AgCl覆盖在阴极发生钝化 |
您最近半年使用:0次
9 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是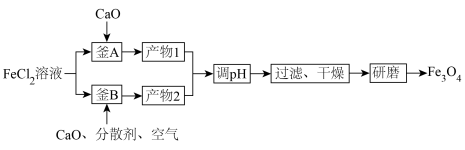
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为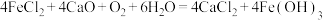 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近半年使用:0次
10 . 亚氯酸钠( )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是
 )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是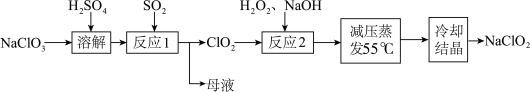
A.“反应1”中 是还原产物,母液中主要成分是 是还原产物,母液中主要成分是 |
B.“反应1”需要通入 稀释 稀释 ,以防发生爆炸 ,以防发生爆炸 |
C.“反应2”中,氧化剂和还原剂的物质的量之比为 |
D.若还原产物均为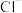 时, 时, 的氧化能力是等质量 的氧化能力是等质量 的2.5倍 的2.5倍 |
您最近半年使用:0次



