1 . 下列表述对应的离子方程式书写正确的是
A.将二氧化硫通入酸性高锰酸钾溶液中: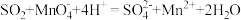 |
B.酸性碘化钾溶液中滴加适量双氧水: |
C.将二氧化碳通入碳酸钠溶液中: |
D.向 溶液中加入足量的NaOH溶液: 溶液中加入足量的NaOH溶液: |
您最近一年使用:0次
2 . 下列离子方程式书写正确的是
A.将 气体通入 气体通入 溶液中: 溶液中: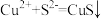 |
B.将稀 加 加 溶液中: 溶液中: |
C.将少量 溶液加入 溶液加入 溶液中: 溶液中: |
D.将 与稀 与稀 按 按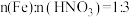 反应时: 反应时: |
您最近一年使用:0次
3 . 下列离子方程式正确且能准确解释相应实验的是
| A | 用稀硝酸洗涤做过银镜反应的试管 | 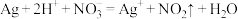 |
| B | 向 溶液中加入过量 溶液中加入过量 稀溶液并加热,有白色沉淀产生 稀溶液并加热,有白色沉淀产生 | 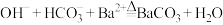 |
| C | 向 悬浊液中滴加 悬浊液中滴加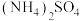 溶液,沉淀溶解 溶液,沉淀溶解 | 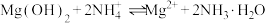 |
| D | FeS溶于足量稀硝酸 | 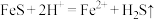 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 工业上从钴镍渣(主要含CoO、NiO和少量FeO、Cu)中回收Co和Ni的流程如下。
 ;②
;② ,完全沉淀时
,完全沉淀时 ;③
;③ 。下列说法正确的是
。下列说法正确的是


 ;②
;② ,完全沉淀时
,完全沉淀时 ;③
;③ 。下列说法正确的是
。下列说法正确的是A.滤渣1是Cu,滤渣2是 |
B.氧化性: |
C.若沉镍完全后滤液中 ,则 ,则 |
| D.“氧化沉钴”中氧化剂、还原剂的物质的量之比为2:1 |
您最近一年使用:0次
2024-05-15更新
|
113次组卷
|
2卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
5 .  催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是
 催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的
催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的 作催化剂,
作催化剂, 将
将 还原成
还原成 的一种反应历程如图所示。下列说法错误的是
的一种反应历程如图所示。下列说法错误的是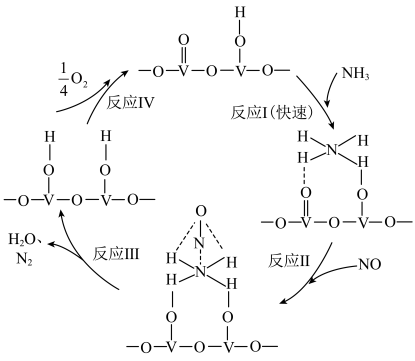
| A.该历程中能垒最高的是反应I |
| B.该历程中,V元素被氧化的只有反应Ⅳ |
C.该催化反应的总反应式为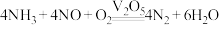 |
| D.整个历程中涉及极性键和非极性键的断裂和形成 |
您最近一年使用:0次
6 . 下列叙述对应的离子方程式正确的是
A.向 溶液中滴加稀氨水: 溶液中滴加稀氨水: |
B.向苯酚钠溶液中通入少量CO2: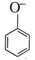 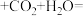 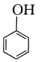 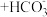 |
C.酸性 溶液氧化 溶液氧化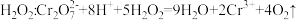 |
D. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
您最近一年使用:0次
解题方法
7 . 下列离子方程式书写错误的是
A.向银氨溶液中滴入乙醛: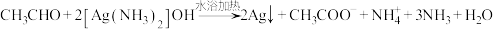 |
B.向硫代硫酸钠溶液中加入稀硫酸: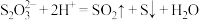 |
C.向漂白粉溶液中通入少量 : :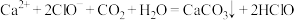 |
D.向加有 的 的 溶液中通入 溶液中通入 : :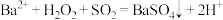 |
您最近一年使用:0次
解题方法
8 . 碱金属和碱土金属元素分别位于元素周期表的ⅠA族和ⅡA族,它们的化合物应用广泛。历史上曾以NaCl为原料生产NaOH作为化学工业开端的标志。 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。
碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
A.侯氏制碱法中的物质转化: |
B.由 制备乙酸的物质转化: 制备乙酸的物质转化: |
C.电解饱和NaCl溶液的阴极反应: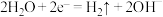 |
D. 与 与 共熔的反应: 共熔的反应: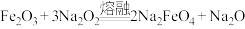 |
您最近一年使用:0次
9 . 亚氯酸钠( )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是
 )具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的
)具有强氧化性、受热易分解,可用作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如图所示.已知高浓度的 易爆炸.下列说法错误的是
易爆炸.下列说法错误的是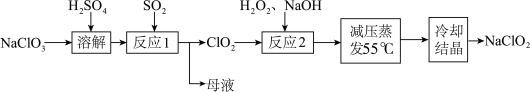
A.“反应1”中 是还原产物,母液中主要成分是 是还原产物,母液中主要成分是 |
B.“反应1”需要通入 稀释 稀释 ,以防发生爆炸 ,以防发生爆炸 |
C.“反应2”中,氧化剂和还原剂的物质的量之比为 |
D.若还原产物均为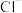 时, 时, 的氧化能力是等质量 的氧化能力是等质量 的2.5倍 的2.5倍 |
您最近一年使用:0次
解题方法
10 . 钛合金在航空航天领域有着广泛的应用.一种利用废脱硝催化剂(含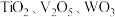 等成分)提取钛的工艺流程如图所示.下列说法错误的是
等成分)提取钛的工艺流程如图所示.下列说法错误的是
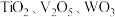 等成分)提取钛的工艺流程如图所示.下列说法错误的是
等成分)提取钛的工艺流程如图所示.下列说法错误的是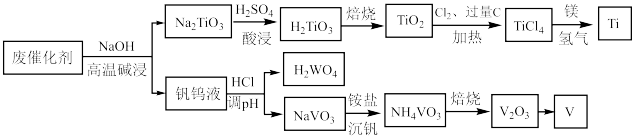
A.基态钛的价层电子排布式为 |
| B.上述流程中共涉及到3个氧化还原反应 |
C.高温碱浸生成 的离子方程式为: 的离子方程式为: |
| D.铝热反应制备钒与上述反应中镁冶炼钛的原理相似 |
您最近一年使用:0次



