1 .  具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。
(1)实验室检验 的方法为
的方法为_______ 。 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是_______ (用离子方程式表示)
(2)实验室可用NaClO氧化酸性 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。若要制取1000mL2mol/L ,则需要NaClO的质量为
,则需要NaClO的质量为_______ g。
(3)通过控制条件, 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为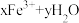
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。
(4)工业上可用废铁屑来制备 ,流程如下:
,流程如下:
废铁屑
 晶体
晶体 无水
无水
①在HCl气流中加热的原因是_______ 。
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为_______ (精确到0.1%)
 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。(1)实验室检验
 的方法为
的方法为 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是(2)实验室可用NaClO氧化酸性
 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为 ,则需要NaClO的质量为
,则需要NaClO的质量为(3)通过控制条件,
 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为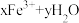
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。| A.降温 | B.加水稀释 | C.加入 | D.加入 |
 ,流程如下:
,流程如下:废铁屑

 晶体
晶体 无水
无水
①在HCl气流中加热的原因是
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的
 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为
您最近一年使用:0次
2 . ClO2是一种消毒杀菌效率高、污染少的绿色消毒剂。可以通过下列两种途径得到:
方法一:
方法二:
(1)用双线桥法表示方法一反应中电子转移的方向和数目。____________________
(2)方法一中浓盐酸在反应中显示出来的性质是__________(填字母)。
(3)配平方法二中的化学方程式。______________________________________
(4)方法二中的氧化剂为__________ (填化学式),在反应中发生______________ (填“氧化”或“还原”)反应。还原产物为_________ (填化学式)。
(5)上述反应为氧化还原反应,氧化还原反应原理在生活中广泛应用。下列物质的用途中,利用了氧化还原反应原理的是______________(填字母)。
方法一:

方法二:

(1)用双线桥法表示方法一反应中电子转移的方向和数目。
(2)方法一中浓盐酸在反应中显示出来的性质是__________(填字母)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(4)方法二中的氧化剂为
(5)上述反应为氧化还原反应,氧化还原反应原理在生活中广泛应用。下列物质的用途中,利用了氧化还原反应原理的是______________(填字母)。
| A.用盐酸除铁锈 | B.用赤铁矿炼铁 |
| C.生石灰作食品干燥剂 | D.用熟石灰改良酸性土壤 |
您最近一年使用:0次
解题方法
3 . 实验小组对Na2S2O3分别与FeCl3、Fe2(SO4)3的反应进行实验探究。 实验药品:0.1mol/LNa2S2O3溶液(pH=7);0.1mol/LFeCl3溶液(pH=1);0.05mol/LFe2(SO4)3溶液(pH=1)。实验过程
资料:i.Na2S2O3在酸性条件下不稳定,发生自身氧化还原反应;
ii.Fe3++
 Fe(S2O3)+(暗紫色),Fe2+遇
Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象
(1)向试管中滴加溶液所用的仪器是___________ ;配制FeCl3溶液时,需要用盐酸酸化,结合离子方程式解释原因:___________ 。
(2)对实验I中现象产生的原因探究如下:
①证明有Fe2+生成:取实验I中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到___________ 。
②实验I中紫色褪去时 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是___________ 。
③实验I和II对比,I中出现淡黄色浑浊,而II中不出现淡黄色浑浊的原因是___________ 。
(3)为探究实验II和III中紫色褪去快慢不同的原因,设计实验如下:
①试剂X是___________ 。
②由实验IV和实验V得出的结论是___________ 。
| 实验编号 | I | II | III |
| 实验操作 | 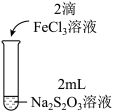 | 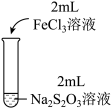 | 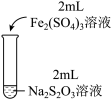 |
| 实验现象 | 溶液呈紫色,静置后紫色迅速褪去,久置后出现淡黄色浑浊 | 溶液呈紫色静置后紫色褪去,久置后不出现淡黄色浑浊 | 溶液呈紫色,静置后紫色缓慢褪去,久置后不出现淡黄色浑浊 |
ii.Fe3++

 Fe(S2O3)+(暗紫色),Fe2+遇
Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象(1)向试管中滴加溶液所用的仪器是
(2)对实验I中现象产生的原因探究如下:
①证明有Fe2+生成:取实验I中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到
②实验I中紫色褪去时
 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是③实验I和II对比,I中出现淡黄色浑浊,而II中不出现淡黄色浑浊的原因是
(3)为探究实验II和III中紫色褪去快慢不同的原因,设计实验如下:
| 实验编号 | IV | V |
| 实验操作 | 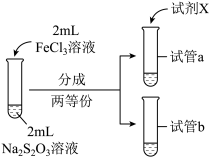 | 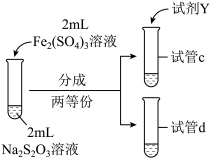 |
| 实验现象 | 紫色褪去时间a>b | 紫色褪去时间c<d |
②由实验IV和实验V得出的结论是
您最近一年使用:0次
4 . 某钒矿炼钢后剩余的尾渣中含有 、
、 、
、 、
、 、
、 等,现从该钒渣中回收
等,现从该钒渣中回收 及少量单质铝的工艺流程如图。(已知:高温条件下
及少量单质铝的工艺流程如图。(已知:高温条件下 可与
可与 反应生成
反应生成 )
)
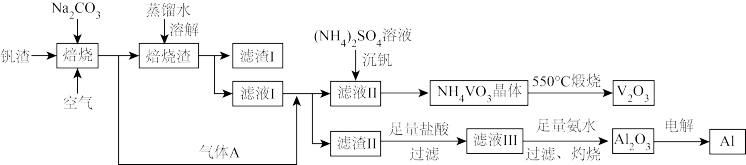
(1)滤液I的成分是 、
、 和
和_______ (填化学式)。
(2)滤渣I含有 、
、 ,检验滤渣I中含有
,检验滤渣I中含有 的方法是
的方法是_______
(3)写出“焙烧”时生成 的化学方程式:
的化学方程式:_______ ,生成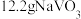 时,转移的电子数目为
时,转移的电子数目为_______  。
。
(4)滤渣II是_______ (填化学式)。
(5)滤液III与氨水反应生成沉淀的离子方程式为_______ 。
 、
、 、
、 、
、 、
、 等,现从该钒渣中回收
等,现从该钒渣中回收 及少量单质铝的工艺流程如图。(已知:高温条件下
及少量单质铝的工艺流程如图。(已知:高温条件下 可与
可与 反应生成
反应生成 )
)
(1)滤液I的成分是
 、
、 和
和(2)滤渣I含有
 、
、 ,检验滤渣I中含有
,检验滤渣I中含有 的方法是
的方法是(3)写出“焙烧”时生成
 的化学方程式:
的化学方程式: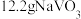 时,转移的电子数目为
时,转移的电子数目为 。
。(4)滤渣II是
(5)滤液III与氨水反应生成沉淀的离子方程式为
您最近一年使用:0次
2022-08-12更新
|
142次组卷
|
2卷引用:陕西省汉中市2021-2022学年高二下学期期末联考化学试题
名校
解题方法
5 . 过碳酸钠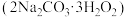 俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。

(1)装置中仪器A的名称为_______ 。
(2)按图连接好装置后,先将饱和 溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入
溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入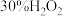 溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
(3)反应过程中要控制温度不能太高,原因是________
(4)反应后向混合物中加入 固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入
固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入 固体的作用是
固体的作用是________
(5)过碳酸钠样品纯度的测定。
取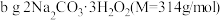 配成
配成 溶液,取
溶液,取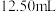 溶液于锥形瓶,加入足量稀硫酸,用
溶液于锥形瓶,加入足量稀硫酸,用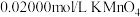 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: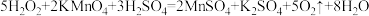 )
)
①实验达到滴定终点的现象是_______ ;
②该过氧碳酸钠的产品纯度为_______ (用字母表示);
③滴定时间过长,测得过碳酸钠产品纯度将_______ (填“偏高”、“偏低”或“无影响”)。
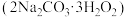 俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
(1)装置中仪器A的名称为
(2)按图连接好装置后,先将饱和
 溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入
溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入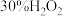 溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。A. | B. | C. | D. |
(4)反应后向混合物中加入
 固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入
固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入 固体的作用是
固体的作用是(5)过碳酸钠样品纯度的测定。
取
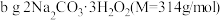 配成
配成 溶液,取
溶液,取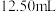 溶液于锥形瓶,加入足量稀硫酸,用
溶液于锥形瓶,加入足量稀硫酸,用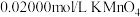 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: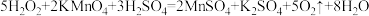 )
)①实验达到滴定终点的现象是
②该过氧碳酸钠的产品纯度为
③滴定时间过长,测得过碳酸钠产品纯度将
您最近一年使用:0次
2022-05-20更新
|
334次组卷
|
3卷引用:陕西省汉中市龙岗学校2022-2023学年高三上学期第一次质量检测化学试题
解题方法
6 . 铁元素是生产生活中的一种重要的金属元素,其最常见的价态是+2、+3价,但在碱性条件的溶液中也可能会以+6价的形式存在,如高铁酸根离子(化学式为 ,具有强氧化性,其钠盐或钾盐均可用作水处理剂)。某些铁盐溶于水中可生成Fe(OH)3胶体,可用作净水剂。
,具有强氧化性,其钠盐或钾盐均可用作水处理剂)。某些铁盐溶于水中可生成Fe(OH)3胶体,可用作净水剂。
(1)高铁酸钠(Na2FeO4)是一种水处理剂,因为它具有_______ 性,可对水杀菌消毒;一定条件下,向NaClO与NaOH的混合溶液中加入FeCl3溶液,发生反应可得到高铁酸钠,该反应的化学方程式为_______ ;根据信息,分析Na2FeO4可除去水中的微细悬浮物的原因_______ 。
(2)铁元素的单质及其部分化合物的转化关系如图:

①溶液D→溶液E的过程中,试剂2作_______ (填“氧化剂”或“还原剂”,溶液B中含有的金属阳离子为_______ (填离子符号)。
②高温条件下,铁与水蒸气反应生成固体A的反应的化学方程式为_______ 。
③溶液E→溶液F的过程中溶液颜色变化的原因是_______ (用文字说明)。
④某同学向溶液D中直接滴入NaOH溶液,可观察到的现象为_______ 。
 ,具有强氧化性,其钠盐或钾盐均可用作水处理剂)。某些铁盐溶于水中可生成Fe(OH)3胶体,可用作净水剂。
,具有强氧化性,其钠盐或钾盐均可用作水处理剂)。某些铁盐溶于水中可生成Fe(OH)3胶体,可用作净水剂。(1)高铁酸钠(Na2FeO4)是一种水处理剂,因为它具有
(2)铁元素的单质及其部分化合物的转化关系如图:

①溶液D→溶液E的过程中,试剂2作
②高温条件下,铁与水蒸气反应生成固体A的反应的化学方程式为
③溶液E→溶液F的过程中溶液颜色变化的原因是
④某同学向溶液D中直接滴入NaOH溶液,可观察到的现象为
您最近一年使用:0次
名校
7 . 国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g•L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中的SO2,并对其含量进行测定。
实验步骤如图1:

I.向B中加入300.00mL葡萄酒和适量稀硫酸,加热,使SO2全部逸出并与C中的H2O2完全反应,加热除去H2O2,得到待测液并稀释至500mL。
II.取25.00mL待测液于锥形瓶中,加入指示剂,用0.0100mol·L-1NaOH标准溶液进行滴定。
III.数据处理。
回答下列问题:
(1)仪器A的名称为____ 。
(2)写出C中发生的离子反应方程式_____ 。
(3)NaOH标准溶液盛装在图2____ (填“甲”或“乙”)滴定管中。若滴定终点溶液pH为8.8,则选择的指示剂为____ ;滴定过程中,眼睛应注视____ ;滴定终点的判断依据为____ 。

(4)根据下列表格中的数据计算该葡萄酒中SO2含量为___ g•L-1。
(5)下列操作会导致实验结果偏低的是____ (填字母)。
a.滴定管在装液前未用标准溶液润洗
b.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
实验步骤如图1:

I.向B中加入300.00mL葡萄酒和适量稀硫酸,加热,使SO2全部逸出并与C中的H2O2完全反应,加热除去H2O2,得到待测液并稀释至500mL。
II.取25.00mL待测液于锥形瓶中,加入指示剂,用0.0100mol·L-1NaOH标准溶液进行滴定。
III.数据处理。
回答下列问题:
(1)仪器A的名称为
(2)写出C中发生的离子反应方程式
(3)NaOH标准溶液盛装在图2

(4)根据下列表格中的数据计算该葡萄酒中SO2含量为
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.10 | 7.60 |
| 2 | 25.00 | 7.60 | 15.00 |
| 3 | 25.00 | 0.20 | 7.80 |
a.滴定管在装液前未用标准溶液润洗
b.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
您最近一年使用:0次
2022-05-01更新
|
23次组卷
|
2卷引用:陕西省汉中市2021-2022学年高二下学期期中考试化学试题
解题方法
8 . 下列离子反应方程式的书写错误的是
| A.AgCl浊液中通入H2S,变黑:2AgCl+H2S=Ag2S+2H++2Cl- |
B.用亚硫酸钠溶液吸收少量氯气:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
| C.醋酸除去水垢中的碳酸钙:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.氯化铁溶液腐蚀电路板:2Fe3++Cu=2Fe2++Cu2+ |
您最近一年使用:0次
名校
解题方法
9 . 实验室用如图方法制备饮用水消毒剂 :
:
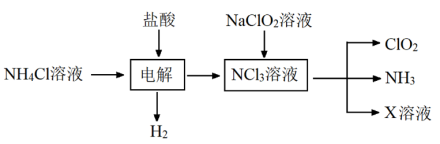
已知: 为强氧化剂,其中N元素为
为强氧化剂,其中N元素为 价。下列说法
价。下列说法不正确 的是
 :
:
已知:
 为强氧化剂,其中N元素为
为强氧化剂,其中N元素为 价。下列说法
价。下列说法A. 的电子式为 的电子式为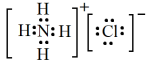 |
B.电解池中总反应的化学方程式为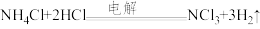 |
C.若 与 与 恰好完全反应,则X为 恰好完全反应,则X为 |
D.饮用水中残留的 可用适量 可用适量 溶液去除 溶液去除 |
您最近一年使用:0次
2021-06-09更新
|
953次组卷
|
14卷引用:陕西省汉中市龙岗学校2022-2023学年高三上学期第三次质量检测化学试题
陕西省汉中市龙岗学校2022-2023学年高三上学期第三次质量检测化学试题新疆昌吉州2021-2022学年高三下学期高考适应性第一次诊断性测试化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(河北专用)北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题北京市中国人民大学附属中学2022-2023学年高三上学期统练6化学试题北京市朝阳区2021届高三一模化学试题(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)安徽省名校2020-2021学年高二下学期5月第二次联考化学试题北京市北京理工大学附属中学2022届高三十月月考化学试题福建省福州高级中学2022届高三第二阶段考试化学试卷(10月) 山东省青岛第十七中学2020-2021学年高三下学期期中考试化学试题广东省广州市2021届高三下学期模拟考试化学试题
名校
解题方法
10 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO3还原法制备保险粉的流程如下:
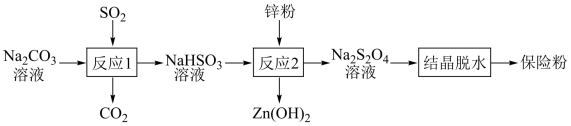
下列说法错误的是

下列说法错误的是
| A.反应1说明酸性:H2SO3>H2CO3 |
| B.反应1结束后,可用盐酸酸化的 BaCl2溶液检验NaHSO3是否被氧化 |
| C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2 |
| D.反应2最好在无氧条件下进行 |
您最近一年使用:0次
2021-01-25更新
|
2876次组卷
|
28卷引用:陕西省洋县中学2021-2022学年高一上学期期末考试化学试题
陕西省洋县中学2021-2022学年高一上学期期末考试化学试题(已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)辽宁省沈阳市东北育才学校2021-2022高一下学期期中考试化学试题(已下线)第14讲 硫、二氧化硫【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)山西省长治市第二中学校2021-2022学年高一下学期第二次月考化学试题 河南省洛阳市2021-2022学年高一下学期期末质量检测化学试题重庆市璧山来凤中学校2022-2023学年高三10月月考化学试题重庆市2021年普通高中学业水平选择考适应性测试化学试题山东省聊城市第一中学2021届高三下学期开学模拟考试化学试题(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)天津市第一中学2020-2021学年高一下学期期中考试化学试题广东省广州市广州大学附属中学2020-2021学年高一下学期4月月考试题湖南省衡阳市第八中学2020-2021学年高一下学期期末考试化学试题(已下线)2021年秋季高三开学摸底考化学试卷03(江苏专用)江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期第一次阶段性诊断测试化学试题湖南省天壹名校联盟.宁乡市2021-2022学年高三11月调研考试化学试题湖南师范大学附属中学2021-2022学年高三上学期月考(三)化学试题福建省师范大学附属中学擎云级2021-2022学年高三上学期12月月考化学试题湖南省长沙市宁乡市2021-2022学年高三11月调研考试化学试题山东省泰安市新泰中学2021-2022学年高一上学期12月月考化学试题福建省泉州科技中学2021-2022学年高三上学期期中考试化学试题福建省泉州科技中学2021-2022学年高三上学期期中考试化学试题 天津市实验中学2021-2022学年高三上学期第一次阶段考试化学试题 江西省丰城中学2023-2024学年高三上学期开学考试化学试题河南省南阳镇平一高2023-2024学年高一上学期化学学科训练试题黑龙江省哈尔滨师范大学青冈实验中学校2023-2024学年高三上学期12月份考试化学试题



