名校
1 . 用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新方法。高铁酸钠可通过湿法或干法来制备,反应原理如下:
湿法:
干法:
下列说法不正确的是
湿法:

干法:

下列说法不正确的是
| A.Na2FeO4中铁元素为+6价,具有强氧化性,能消毒杀菌 |
B.湿法中氧化性: >ClO- >ClO- |
| C.干法中Na2O2既是氧化剂又是还原剂 |
| D.干法中生成1molO2转移8mol电子 |
您最近一年使用:0次
名校
2 .  常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为
常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为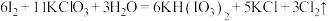 ,下列说法正确的是
,下列说法正确的是
 常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为
常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为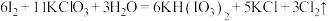 ,下列说法正确的是
,下列说法正确的是A.还原产物为 和 和 |
B.可用 与 与 燃烧后的产物溶于水制备盐酸 燃烧后的产物溶于水制备盐酸 |
C.还原剂和氧化剂的物质的量之比为 |
D.产生 时反应中转移 时反应中转移 |
您最近一年使用:0次
名校
3 . 工业上,常用浓氨水检验氯气管道是否漏气,反应原理为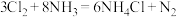 。
。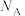 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
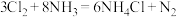 。
。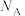 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是| A.用玻璃棒蘸取浓氨水点击管道接口处产生“白烟”表明漏气 |
B.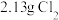 完全反应,作还原剂的 完全反应,作还原剂的 分子数为 分子数为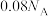 |
C.生成 时氧化产物分子中共用电子对数为 时氧化产物分子中共用电子对数为 |
| D.还原产物中含有离子键和共价键 |
您最近一年使用:0次
4 . 化学源于生活,她与我们生活息息相关。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。
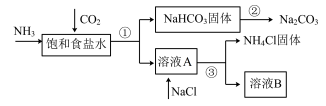
(1)①~③所涉及的操作方法中,包含过滤的是_______ (填序号)。
(2)根据上图,将化学方程式补充完整:
_______ 
_______ 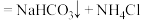
(3)煅烧 固体的化学方程式是
固体的化学方程式是_______ 。
(4)关于上述过程,下列说法中正确的是_______ (填字母)。
a. 不可循环使用
不可循环使用
b.副产物 可用作肥料
可用作肥料
c.反应过程中应先通入极易溶于水的 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体
Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠( )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是_______ ,还原剂是_______ ;被氧化与被还原元素的物质的量之比为:_______ 。
(6)某离子反应中涉及 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是_______ 。
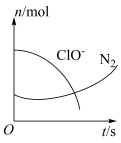
a.该反应的氧化剂是
b.消耗 还原剂,转移
还原剂,转移 电子
电子
c.氧化剂与还原剂的物质的量之比为
d.当生成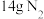 时,消耗的
时,消耗的 为
为
e.氧化性: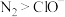
(7)高铁酸钠( ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为_______ ;写出制备高铁酸钠的离子方程式_______ 。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上图,将化学方程式补充完整:


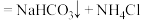
(3)煅烧
 固体的化学方程式是
固体的化学方程式是(4)关于上述过程,下列说法中正确的是
a.
 不可循环使用
不可循环使用b.副产物
 可用作肥料
可用作肥料c.反应过程中应先通入极易溶于水的
 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠(
 )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是(6)某离子反应中涉及
 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是
a.该反应的氧化剂是

b.消耗
 还原剂,转移
还原剂,转移 电子
电子c.氧化剂与还原剂的物质的量之比为

d.当生成
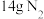 时,消耗的
时,消耗的 为
为
e.氧化性:
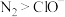
(7)高铁酸钠(
 ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为
您最近一年使用:0次
解题方法
5 . 研究表明:多种海产品如虾、蟹、牡蛎等,体内含有 价的砷(
价的砷( )元素,但它对人体是无毒的,砒霜的成分是
)元素,但它对人体是无毒的,砒霜的成分是 ,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜
,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜 大量维生素
大量维生素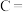 砒霜。下面有关解释不正确的是
砒霜。下面有关解释不正确的是
 价的砷(
价的砷( )元素,但它对人体是无毒的,砒霜的成分是
)元素,但它对人体是无毒的,砒霜的成分是 ,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜
,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜 大量维生素
大量维生素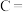 砒霜。下面有关解释不正确的是
砒霜。下面有关解释不正确的是| A.青菜中含有维生素C | B.维生素C具有氧化性 |
| C.致人中毒过程中砷发生还原反应 | D.砒霜是还原产物 |
您最近一年使用:0次
名校
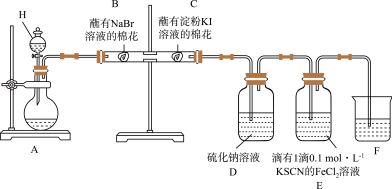
6 . 某同学利用以下装置探究非金属元素性质的递变规律,并验证氯气的性质。
(1)仪器H的名称为______ 。
(2)能说明氯气的氧化性强于溴的实验现象为______ 。
(3)氯气进入D中,有黄色固体产生,反应的离子方程式为______ 。
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:
a: 被氧化; b:
被氧化; b:______ 。
设计实验方案验证以上假设,向褪色后的溶液中滴加______ ,若观察到______ ,可验证假设b成立。
(5)将溴水滴入淀粉 溶液中,溶液变蓝,再结合B处实验现象,可以得出的结论正确的是______(填标号)。
溶液中,溶液变蓝,再结合B处实验现象,可以得出的结论正确的是______(填标号)。
(1)仪器H的名称为
(2)能说明氯气的氧化性强于溴的实验现象为
(3)氯气进入D中,有黄色固体产生,反应的离子方程式为
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:
a:
 被氧化; b:
被氧化; b:设计实验方案验证以上假设,向褪色后的溶液中滴加
(5)将溴水滴入淀粉
 溶液中,溶液变蓝,再结合B处实验现象,可以得出的结论正确的是______(填标号)。
溶液中,溶液变蓝,再结合B处实验现象,可以得出的结论正确的是______(填标号)。A.氧化性: | B.同主族元素从上到下非金属性减弱 |
| C.同周期元素从左到右非金属性减弱 | D. 、 、 、I对应含氧酸酸性逐渐减弱 、I对应含氧酸酸性逐渐减弱 |
您最近一年使用:0次
名校
解题方法
7 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
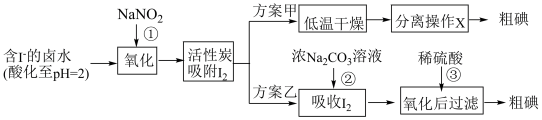
资料显示:Ⅰ.pH=2时,NaNO2溶液只能将I-氧化为I2;
Ⅱ. ;
;
Ⅲ.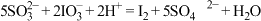 ;
;
(1)反应①生成一种无色气体,遇空气变为红棕色。则反应①的离子方程式是________ 。
(2)方案甲中,根据I2的特性,分离操作X的名称是________ 。
(3)已知I2在碱性溶液中反应生成I-和 。反应②的离子方程式是
。反应②的离子方程式是________ 。
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是________ 。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、 。请设计实验检验滤液中的
。请设计实验检验滤液中的 ,将实验方案补充完整。
,将实验方案补充完整。
可供选择的试剂:稀H2SO4、淀粉溶液、Na2SO3溶液
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B.________ 。

资料显示:Ⅰ.pH=2时,NaNO2溶液只能将I-氧化为I2;
Ⅱ.
 ;
;Ⅲ.
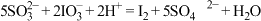 ;
;(1)反应①生成一种无色气体,遇空气变为红棕色。则反应①的离子方程式是
(2)方案甲中,根据I2的特性,分离操作X的名称是
(3)已知I2在碱性溶液中反应生成I-和
 。反应②的离子方程式是
。反应②的离子方程式是(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、
 。请设计实验检验滤液中的
。请设计实验检验滤液中的 ,将实验方案补充完整。
,将实验方案补充完整。可供选择的试剂:稀H2SO4、淀粉溶液、Na2SO3溶液
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B.
您最近一年使用:0次
名校
解题方法
8 .  是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
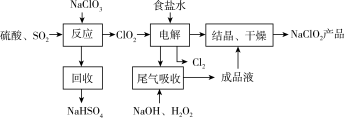
下列说法正确的是
 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
下列说法正确的是
A. 中 中 的化合价为 的化合价为 价 价 |
B.“反应”步骤中, 被氧化为 被氧化为 |
C.“电解”步骤中, 被还原为 被还原为 |
D.“尾气吸收”是吸收少量的 ,此吸收反应中, ,此吸收反应中, 作氧化剂 作氧化剂 |
您最近一年使用:0次
2024-01-19更新
|
76次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一上学期第三次月考化学科试题
名校
解题方法
9 . 价-类二维图是梳理元素及其化合物性质的重要工具,以下是硫及其常见化合物的价-类二维图,图示中横坐标表示物质类别,纵坐标表示其中硫元素的化合价
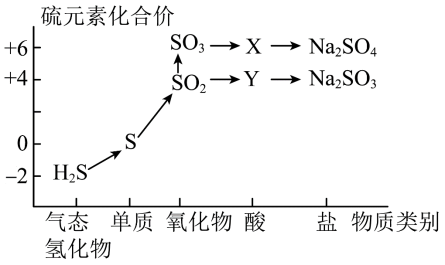
根据图示回答下列问题:
(1)X的化学式为_______ ,Y中硫元素的化合价为_______ 。
(2)根据“价-类”二维图预测,下列能与 反应且使
反应且使 表现还原性的物质是_______(填序号)。
表现还原性的物质是_______(填序号)。
(3)分析 的物质类别,写出它和过量
的物质类别,写出它和过量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(4)欲制备 ,结合元素化合价,从氧化还原角度分析,合理的是_______(填序号)。
,结合元素化合价,从氧化还原角度分析,合理的是_______(填序号)。

根据图示回答下列问题:
(1)X的化学式为
(2)根据“价-类”二维图预测,下列能与
 反应且使
反应且使 表现还原性的物质是_______(填序号)。
表现还原性的物质是_______(填序号)。A. | B. | C.酸性 溶液 溶液 | D. 溶液 溶液 |
 的物质类别,写出它和过量
的物质类别,写出它和过量 溶液反应的离子方程式
溶液反应的离子方程式(4)欲制备
 ,结合元素化合价,从氧化还原角度分析,合理的是_______(填序号)。
,结合元素化合价,从氧化还原角度分析,合理的是_______(填序号)。A. | B. |
C. | D. |
您最近一年使用:0次
2024-01-19更新
|
129次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一上学期第三次月考化学科试题
名校
解题方法
10 . 根据反应:① ;②
;② 。下列说法正确的是
。下列说法正确的是
 ;②
;② 。下列说法正确的是
。下列说法正确的是A.氧化性: | B.还原性: |
C. 不能发生 不能发生 | D.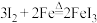 可以发生 可以发生 |
您最近一年使用:0次
2024-01-19更新
|
72次组卷
|
2卷引用:海南省琼海市嘉积中学2023-2024学年高一上学期第三次月考化学科试题



