1 . 高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室用 固体来配制
固体来配制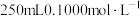 的
的 酸性溶液。
酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、___________ 。
②计算所需 固体的质量为
固体的质量为___________ 克。
③下列关“容量瓶及其使用”的叙述中正确的是___________ (填序号)。
a.使用前必须检查是否漏水 b.能配制一定体积准确浓度的标准溶液
c.可用来长期贮存溶液 d.能用作溶解固体、稀释浓溶液的容器
④下列操作会导致溶液浓度偏高的是___________ (填序号)。
a.加水定容时俯视刻度线
b.未洗涤溶解后的烧杯和玻璃棒
c.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
d. 溶解时放热,没有将溶液冷却即加水至刻度线
溶解时放热,没有将溶液冷却即加水至刻度线
(2)用 酸化的上述新配制的
酸化的上述新配制的 溶液10mL氧化并测定
溶液10mL氧化并测定 溶液中
溶液中 的物质的量浓度,消耗0.05mol/L的
的物质的量浓度,消耗0.05mol/L的 溶液100mL,则反应后锰元素的价态为
溶液100mL,则反应后锰元素的价态为___________ 。
(3)某同学利用 氧化
氧化 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略): )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: ;
;
①装置A中a的作用是___________ ,装置A中制备 的化学方程式为
的化学方程式为___________ 。
②上述装置存在一处缺陷,会导致 产率降低,改进的方法是
产率降低,改进的方法是___________ 。
③装置C中发生反应的离子方程式为___________ 。
(1)实验室用
 固体来配制
固体来配制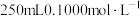 的
的 酸性溶液。
酸性溶液。①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、
②计算所需
 固体的质量为
固体的质量为③下列关“容量瓶及其使用”的叙述中正确的是
a.使用前必须检查是否漏水 b.能配制一定体积准确浓度的标准溶液
c.可用来长期贮存溶液 d.能用作溶解固体、稀释浓溶液的容器
④下列操作会导致溶液浓度偏高的是
a.加水定容时俯视刻度线
b.未洗涤溶解后的烧杯和玻璃棒
c.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
d.
 溶解时放热,没有将溶液冷却即加水至刻度线
溶解时放热,没有将溶液冷却即加水至刻度线(2)用
 酸化的上述新配制的
酸化的上述新配制的 溶液10mL氧化并测定
溶液10mL氧化并测定 溶液中
溶液中 的物质的量浓度,消耗0.05mol/L的
的物质的量浓度,消耗0.05mol/L的 溶液100mL,则反应后锰元素的价态为
溶液100mL,则反应后锰元素的价态为(3)某同学利用
 氧化
氧化 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略):
 )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: ;
;①装置A中a的作用是
 的化学方程式为
的化学方程式为②上述装置存在一处缺陷,会导致
 产率降低,改进的方法是
产率降低,改进的方法是③装置C中发生反应的离子方程式为
您最近一年使用:0次
2 . 下列转化中.需要加入氧化剂才能实现的是
A. | B. | C. | D.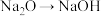 |
您最近一年使用:0次
3 . 反应8NH33Cl2N26NH4Cl,下列说法正确的是
| A.Cl2 发生氧化反应 |
| B.NH3 既是氧化剂又是还原剂 |
| C.每生成22.4L N2,转移的电子数为6NA |
| D.被氧化的NH3与被还原的Cl2的化学计量数之比为 2∶3 |
您最近一年使用:0次
解题方法
4 . 下列转化过程必须加入还原剂才能实现的是
| A.H2O2→O2 | B.FeCl3→FeCl2 | C.Cu→CuO | D.KI→I2 |
您最近一年使用:0次
解题方法
5 . 已知乙醇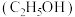 能与
能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: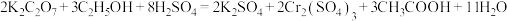 ,
, 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应现象是___________ 。
(2)该反应___________ (填“是”或“不是”)氧化还原反应,判断的依据是___________ 。
(3)你认为能否用这一反应来检测司机是否酒后驾车?___________ (填“能”或“不能”),简述其原理:___________ 。
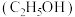 能与
能与 和
和 的混合溶液在一定条件下发生反应:
的混合溶液在一定条件下发生反应: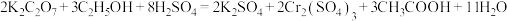 ,
, 和
和 在溶液中分别显橙色和绿色,回答下列问题:
在溶液中分别显橙色和绿色,回答下列问题:(1)该反应现象是
(2)该反应
(3)你认为能否用这一反应来检测司机是否酒后驾车?
您最近一年使用:0次
6 . 能正确表示下列反应的离子方程式为
A.向 溶液中通入过量 溶液中通入过量 : : |
B.食醋去除水垢中的 : :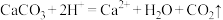 |
C.向碳酸钠溶液中通入少量 : : |
D.次磷酸(一元弱酸)与足量NaOH溶液反应: |
您最近一年使用:0次
2024-04-03更新
|
63次组卷
|
2卷引用:海南省华东师范大学第二附属中学乐东黄流中学2023-2024学年高一上学期11月期中化学试题
7 . 硫代硫酸钠(Na2S2O3)是重要的化工原料易溶于水,在中性或碱性环境下稳定,在酸性溶液水,分解产生S、SO2。
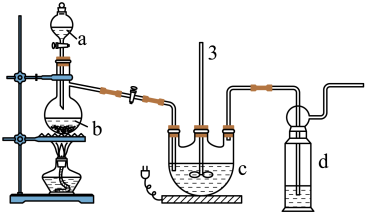
Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为_____ 。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是_____ 。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是_____ 。
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品_____ 。
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O
(5)根据实验①的现象,初步判断最终Fe3+被S2O 还原为Fe2+,通过
还原为Fe2+,通过_____ (填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅰ的现象:_____ 。
(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是_____ 。
(7)进一步探究Ag+和S2O 反应。
反应。
实验③中白色絮状沉淀最后变为黑色沉淀(Ag2S)的化学方程式如下,填入合适的物质和系数:_____ 。
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和_____ 有关(写出两条)。

Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O

| 装置 | 编号 | 试剂X | 实验现象 |
 | ① | Fe(NO3)3溶液 | 混合后溶液先变成紫黑色,30s后溶液几乎变为无色 |
| ② | AgNO3溶液 | 先生成白色絮状沉淀,振荡后,沉淀溶解,得到无色溶液 |
(5)根据实验①的现象,初步判断最终Fe3+被S2O
 还原为Fe2+,通过
还原为Fe2+,通过(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是
(7)进一步探究Ag+和S2O
 反应。
反应。| 装置 | 编号 | 试剂X | 实验现象 |
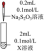 | ② | AgNO3溶液 | 先生成白色絮状沉淀,沉淀很快变成黄色、棕色,最后为黑色沉淀。 |
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和
您最近一年使用:0次
名校
解题方法
8 . 利用空气催化氧化法除掉电石渣浆[含Ca(OH)2]上清液中的S2-,制取石膏(CaSO4·2H2O)的过程如图:
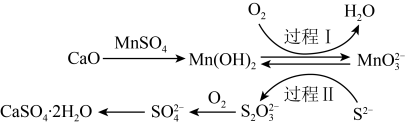
下列说法正确的是
| A.CaSO4∙2H2O属于混合物 |
| B.过程Ⅱ中,S2-为还原剂 |
| C.上述流程中,有两种元素的化合价发生变化 |
D.过程I中,反应的离子方程式为 |
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”),下列物质均能与它们发生反应的是______ (填字母)。
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应: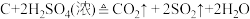 。作还原剂的物质是
。作还原剂的物质是______ ,硫元素的化合价______ (填“升高”或“降低”)。
(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、 、H2O和一种未知离子X
、H2O和一种未知离子X
①已知 在反应中得到电子,则X是
在反应中得到电子,则X是______ 。
②该反应的离子方程式是______ 。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应:
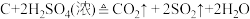 。作还原剂的物质是
。作还原剂的物质是(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、
 、H2O和一种未知离子X
、H2O和一种未知离子X①已知
 在反应中得到电子,则X是
在反应中得到电子,则X是②该反应的离子方程式是
您最近一年使用:0次
解题方法
10 . 现有下列几个离子反应:① +14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++
+14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++ +4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
+4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
 +14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++
+14H++6Cl-=2Cr3++3Cl2↑+7H2O;②2Fe2++Br2=2Fe3++2Br-;③2Fe3++SO2+2H2O=2Fe2++ +4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是
+4H+;④Cl2+2Br-=2Cl-+Br2,下列判断正确的是A.氧化性: >Cl2>Fe3+ >Cl2>Fe3+ |
| B.若在FeBr2溶液中通入少量Cl2,则优先发生反应④ |
| C.还原性:SO2<Fe2+<Br- |
D. 不能将Fe2+氧化为Fe3+ 不能将Fe2+氧化为Fe3+ |
您最近一年使用:0次



