解题方法
1 . 工业上用黄铁矿(FeS2)为原料制备硫酸的流程如下:
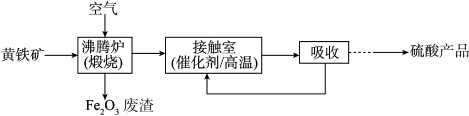
(1)沸腾炉中发生反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2,该反应被氧化的元素是
2Fe2O3+8SO2,该反应被氧化的元素是_______ (填元素名称)。
(2)利用Fe2O3废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化学方程式为_______ 。
(3)从接触室出来的混合气体中含有SO2、SO3、O2、N2等气体,设计一个实验方案证明其中含有SO2:_______ 。
(4)有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热时浓硫酸与木炭反应的化学方程式为_______ 。
(5)将一定量锌与100mL18mol/L浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol,将反应后的溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO2物质的量为_______ mol。

(1)沸腾炉中发生反应的化学方程式为4FeS2+11O2
 2Fe2O3+8SO2,该反应被氧化的元素是
2Fe2O3+8SO2,该反应被氧化的元素是(2)利用Fe2O3废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化学方程式为
(3)从接触室出来的混合气体中含有SO2、SO3、O2、N2等气体,设计一个实验方案证明其中含有SO2:
(4)有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热时浓硫酸与木炭反应的化学方程式为
(5)将一定量锌与100mL18mol/L浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol,将反应后的溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO2物质的量为
您最近一年使用:0次
2021高三·浙江·专题练习
解题方法
2 . 某兴趣小组为验证日常生活用的火柴头上的成分,设计以下实验方案:
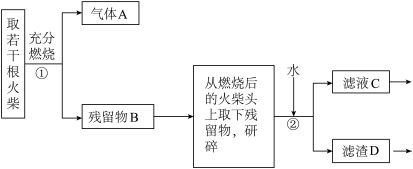
请回答以下问题:
(1)为验证气体A,按如图所示进行实验:若能观察到________ 的现象,即可证明火柴头上含有S元素。可用于替代试管中高锰酸钾酸性溶液的试剂有________ (填编号)。
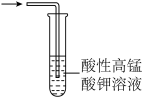
A.品红溶液 B.饱和石灰水 C.稀溴水 D.烧碱溶液
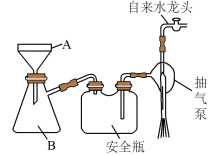
(2)步骤②的实验操作装置如下图所示,其中仪器A的名称是________ ,仪器B的名称是________ ,该操作的工作原理是________________________________________________ 。
(3)要证明火柴头中含有Cl元素的后续实验步骤是___________________________ 。
(4)有学生提出检验火柴头上KClO3另一套实验方案:

有关的离子反应方程式为_____________________________________________ ,
有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是______________________________ (已知AgNO2微溶于水)。

请回答以下问题:
(1)为验证气体A,按如图所示进行实验:若能观察到

A.品红溶液 B.饱和石灰水 C.稀溴水 D.烧碱溶液
(2)步骤②的实验操作装置如下图所示,其中仪器A的名称是

(3)要证明火柴头中含有Cl元素的后续实验步骤是
(4)有学生提出检验火柴头上KClO3另一套实验方案:

有关的离子反应方程式为
有人提出上述方法中出现白色沉淀并不能充分说明火柴头上KClO3的存在,其理由是
您最近一年使用:0次
名校
解题方法
3 . 某小组在验证H2O2氧化Fe2+时发现异常现象,并对其进行深入探究。
实验I:
(1)实验I中溶液变红是因为Fe3+与SCN-发生了反应,其离子方程式是__ 。
(2)探究实验I中红色褪去的原因:取反应后溶液,___ (填实验操作和现象),证明溶液中有Fe3+,而几乎无SCN-。
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:__ 。
实验II:
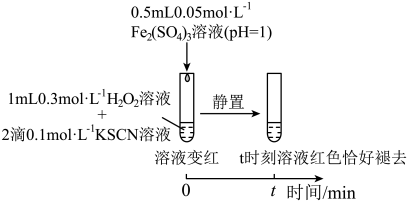
实验III:
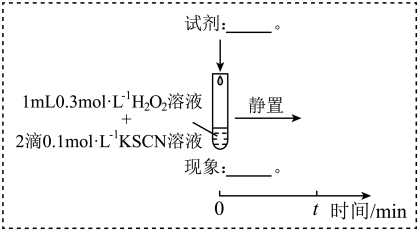
(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,___ 。
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:____ 。
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有___ 。
实验I:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加H2O2溶液,红色变浅并逐渐褪去 |
(2)探究实验I中红色褪去的原因:取反应后溶液,
(3)研究发现,酸性溶液中H2O2能氧化SCN-,但反应很慢且无明显现象,而实验I中褪色相对较快,由此推测Fe3+能加快H2O2与SCN-的反应。通过实验II和III得到了证实。参照实验II的图例,在虚线框内补全实验III:
实验II:

实验III:

(4)查阅资料:Fe3+加快H2O2与SCN-反应的主要机理有
i.Fe3++H2O2=Fe2++HO2·+H+
ii.Fe2++H2O2=Fe3++·OH+OH-
iii.OH(羟基自由基)具有强氧化性,能直接氧化SCN-
为探究Fe2+对H2O2与SCN-反应速率的影响,设计实验如图:
实验IV:

①t′<t,对比实验IV和II可得出结论:在本实验条件下,
②结合资料和(1)~(4)的研究过程,从反应速率和化学平衡的角度解释实验I中溶液先变红后褪色的原因:
③实验I~IV中均有O2生成,小组同学推测可能是HO2·与溶液中其他微粒相互作用生成的,这些微粒有
您最近一年使用:0次
2021-08-13更新
|
633次组卷
|
7卷引用:考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)
4 . 探究Na2SO3固体的热分解产物。
资料:①4Na2SO3 Na2S+3Na2SO4②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。③BaS易溶于水。
Na2S+3Na2SO4②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。③BaS易溶于水。
隔绝空气条件下,加热无水Na2SO3固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到浊液,放置得无色溶液B。
(1)检验分解产物Na2S:取少量溶液B,向其中滴加CuSO4溶液,产生黑色沉淀,证实有S2-。反应的离子方程式是____ 。
(2)检验分解产物Na2SO4:取少量溶液B,滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(H2S),由于沉淀增多对检验造成干扰,另取少量溶液B,加入足量盐酸,离心沉降(固液分离)后,____ (填操作和现象),可证实分解产物中含有SO 。
。
(3)探究(2)中S的来源。
来源1:固体A中有未分解的Na2SO3,在酸性条件下与Na2S反应生成S。
来源2:溶液B中有Na2Sx,加酸反应生成S。
针对来源1进行如图实验:____ 。
②不能用盐酸代替硫酸的原因是____ 。
③写出来源2产生S的反应的离子方程式:____ 。
(4)实验证明Na2SO3固体热分解有Na2S,Na2SO4和S产生。运用氧化还原反应规律分析产物中S产生的合理性:____ 。
资料:①4Na2SO3
 Na2S+3Na2SO4②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。③BaS易溶于水。
Na2S+3Na2SO4②Na2S能与S反应生成Na2Sx,Na2Sx与酸反应生成S和H2S。③BaS易溶于水。隔绝空气条件下,加热无水Na2SO3固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到浊液,放置得无色溶液B。
(1)检验分解产物Na2S:取少量溶液B,向其中滴加CuSO4溶液,产生黑色沉淀,证实有S2-。反应的离子方程式是
(2)检验分解产物Na2SO4:取少量溶液B,滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(H2S),由于沉淀增多对检验造成干扰,另取少量溶液B,加入足量盐酸,离心沉降(固液分离)后,
 。
。(3)探究(2)中S的来源。
来源1:固体A中有未分解的Na2SO3,在酸性条件下与Na2S反应生成S。
来源2:溶液B中有Na2Sx,加酸反应生成S。
针对来源1进行如图实验:
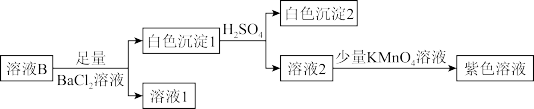
②不能用盐酸代替硫酸的原因是
③写出来源2产生S的反应的离子方程式:
(4)实验证明Na2SO3固体热分解有Na2S,Na2SO4和S产生。运用氧化还原反应规律分析产物中S产生的合理性:
您最近一年使用:0次
2020-08-19更新
|
7816次组卷
|
28卷引用:解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)
(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题讲座(十)化学实验设计与探究(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题四 非金属及其化合物 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点10 硫元素及其化合物-备战2023年高考化学考试易错题(已下线)专题七 非金属元素及其化合物-实战高考·二轮复习核心突破(已下线)专题28 性质探究类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)2020年北京市高考化学试卷北京市第四十三中学2021届高三上学期1月月考化学试题北京市第五中学2020-2021学年高一下学期第一次阶段考试化学试题北京师范大学附属中学2021-2022学年高三上学期期中考试化学试题2020年北京高考化学真题变式题11-19北京市第一六六中学2022届高三下学期三模化学试题北京市第一六六中学2022届高三下学期三模化学试题福建省晋江市第一中学2021-2022学年高三上学期第二次阶段考化学试题山西省运城市稷山县稷山中学2021-2022学年高一下学期期中测试化学试题北京市昌平区第二中学2022-2023 学年高三上学期期中考试化学试题北京一0一教育集团2022-2023学年高一下学期3月月考化学试题北京师范大学第二附属中学2022-2023学年高一下学期期中测试化学试题北京师范大学第二附属中学2023-2024学年高三上学期10月月考化学试题北京市第五十五中学2023-2024学年高一下学期3月调研化学试题北京市大兴一中2023-2024学年高一下学期3月月考化学试题北京市第三十五中学2023-2024学年高一下学期3月月考化学试卷北京市北京师范大学第二附属中学2023-2024学年高一下学期期中考试化学试题
5 . 高铁酸钾是一种新型的消毒剂,可以做到消毒、净水两用。高铁酸钾常用反应3ClO-+2Fe3++10OH-=2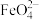 +3Cl-+5H2O制备,下列说法不正确的是
+3Cl-+5H2O制备,下列说法不正确的是
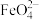 +3Cl-+5H2O制备,下列说法不正确的是
+3Cl-+5H2O制备,下列说法不正确的是A.生成1mol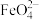 ,转移3mol电子 ,转移3mol电子 |
| B.高铁酸钾可以消毒净水两用是因其有强氧化性且生成胶体 |
| C.高铁酸钾消毒剂不能和洁厕灵混合 |
| D.氧化产物与还原产物物质的量之比为2:5 |
您最近一年使用:0次
解题方法
6 . CuCl为白色粉末状固体,难溶于水和乙醇,在潮湿环境中,容易被空气氧化,是一种重要工业原料。工业以硫化铜精矿为原料,制备氯化亚铜的流程如下图所示:
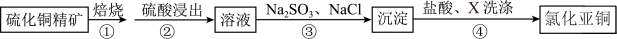
| A.步骤①会产生有毒气体,可用石灰乳吸收 |
| B.步骤②适当增大硫酸浓度、加热可以加快浸出速率 |
C.步骤③应先加入 溶液,再缓慢滴加NaCl溶液 溶液,再缓慢滴加NaCl溶液 |
| D.步骤④中X可以是无水乙醇 |
您最近一年使用:0次
2023-12-05更新
|
285次组卷
|
4卷引用:压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)浙江省稽阳联谊学校2023-2024学年高三上学期联考化学试题(已下线)专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题
解题方法
7 . Ni单原子催化剂具有良好的电催化性能,催化转化 的历程如下。
的历程如下。
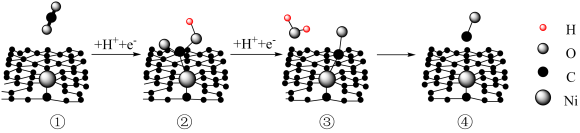
下列说法不正确的是
 的历程如下。
的历程如下。
下列说法不正确的是
| A.CO2催化转化的产物是CO和H2O | B.过程②→③涉及化学键的断裂与生成 |
| C.生成1mol CO,需要转移2mol电子 | D.反应过程中,C的化合价未发生改变 |
您最近一年使用:0次
名校
8 . 高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如图所示方案制备高铁酸钾。下列说法不正确的是
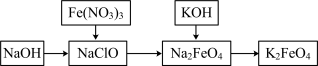
| A.高铁酸钾中铁元素的化合价为+6,具有强氧化性 |
B.反应2Fe3++3ClO−+10OH−=2FeO +3Cl−+5H2O中,生成2 mol FeO +3Cl−+5H2O中,生成2 mol FeO 时,转移6个电子 时,转移6个电子 |
| C.制备高铁酸钾的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度大于高铁酸钾的溶解度 |
| D.明矾、硫酸铁、高铁酸钾都能处理水质,其处理水原理不完全相同 |
您最近一年使用:0次
真题
名校
9 . 化学烫发巧妙利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程示意图如下。下列说法不正确 的是

| A.药剂A具有还原性 |
B.①→②过程若有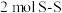 键断裂,则转移 键断裂,则转移 电子 电子 |
C.②→③过程若药剂B是 ,其还原产物为 ,其还原产物为 |
D.化学烫发通过改变头发中某些蛋白质中 键位置来实现头发的定型 键位置来实现头发的定型 |
您最近一年使用:0次
2023-06-21更新
|
5206次组卷
|
20卷引用:2023年高考浙江卷化学真题(6月)变式题(选择题6-10)
(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题6-10)2023年高考浙江卷化学真题(6月)(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第5讲 生物大分子 合成高分子浙江省湖州市吴兴高级中学2023-2024学年高一上学期12月月考化学试题浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题吉林省长春外国语学校2022-2023学年高二下学期7月期末考试化学试题2.4.3氨基酸和蛋白质(课中)-鲁科版选择性必修3山西省阳泉市第一中学校2023-2024学年高二上学期开学考试化学试题新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题北京理工大学附属中学2023-2024学年高三上学期10月月考化学试题福建泉州培元中学2023-2024学年上学期高三10月月考化学试题湖南省常德市汉寿县第一中学2023-2024学年高三上学期10月月考化学试题海南省海口市琼山华侨中学2023-2024学年高三上学期第二次月考化学试题云南省宣威市第六中学2023-2024学年高二上学期11月月考化学试题广东省深圳实验学校高中部2023-2024学年高一上学期第二阶段考试化学试题 江西省宜春市百树学校2023-2024学年高三上学期11月期中考试化学试卷北京市第二中学2023-2024学年高三下学期三模化学试题宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷2北京市第二中学2023-2024学年高三下学期模拟测试化学试题
10 . 以肼( )为原料与醋酸铜反应制取
)为原料与醋酸铜反应制取 的反应为:
的反应为: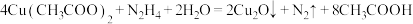 。下列说法不正确的是
。下列说法不正确的是
 )为原料与醋酸铜反应制取
)为原料与醋酸铜反应制取 的反应为:
的反应为: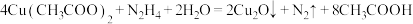 。下列说法不正确的是
。下列说法不正确的是A.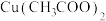 是氧化剂 是氧化剂 |
B.还原性: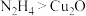 |
| C.氧化产物和还原产物的物质的量之比为2:1 |
D.生成0.5mol 时转移1mol电子 时转移1mol电子 |
您最近一年使用:0次



