名校
1 . 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
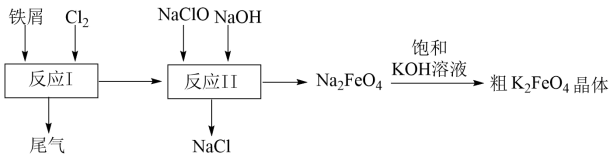
下列叙述不正确的是

下列叙述不正确的是
| A.Cl2和NaClO在反应中均作氧化剂 |
| B.用K2FeO4对饮用水杀菌消毒的同时,还产生Fe(OH)3胶体吸附杂质净化水 |
| C.反应II中氧化剂与还原剂的物质的量之比为2∶3 |
| D.该生产条件下,物质的溶解性:Na2FeO4>K2FeO4 |
您最近一年使用:0次
2022-02-23更新
|
2076次组卷
|
6卷引用:广东省梅州市五华县2019-2020学年高三下学期第一次质检化学试题
广东省梅州市五华县2019-2020学年高三下学期第一次质检化学试题上海市财经大学附属北郊高级中学2022-2023学年高二上学期等级班阶段性检测化学试题(已下线)专项05 氧化还原反应-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)广东省广州市第二中学2022-2023学年高一上学期12月月考化学试题广东省梅州市大埔县虎山中学2022-2023学年高一上学期12月月考化学试题广东省广州市白云中学2023-2024学年高一上学期12月月考化学试题
13-14高三·四川成都·阶段练习
名校
解题方法
2 . 已知氯气有强氧化性,能氧化Fe2+、Br-、I-等。又已知还原性I->Fe2+>Br-。向含有Fe2+、I-、Br-的溶液中通入一定量氯气后,对所得溶液中离子的成分分析正确的是
| A.I-、Fe3+、Cl- | B.Fe2+、Cl-、Br- |
| C.Fe2+、Fe3+、Cl- | D.Fe2+、I-、Cl- |
您最近一年使用:0次
2021-10-18更新
|
485次组卷
|
21卷引用:上海市虹口区2020届高三上学期一模化学试题
上海市虹口区2020届高三上学期一模化学试题上海市虹口区2014届高三二模化学试题(已下线)2015届四川省都江堰中学高三第三次理综考试化学试卷【区级联考】上海市闵行区2019届高三第二学期二模质量调研考试化学试题(已下线)专题04 氧化还原反应——2019年高考真题和模拟题化学分项汇编黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期末考试化学试题江西省横峰中学等五校2019-2020学年新高一竞赛班联考化学试题浙江省温州十五校联合体2019-2020学年高一上学期期中联考化学试题甘肃省天水一中2019-2020学年高一上学期第三学段(期末)考试化学试题吉林省白城市第一中学2019-2020学年高二下学期期末考试化学试题宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题吉林省辽源市第五中学校2019-2020学年高一期中考试化学试题上海市青浦高级中学2021届高三下学期3月月考化学试题辽宁省六校协作体2021-2022学年高一上学期第一次联考化学试题(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)黑龙江省双鸭山市第一中学2022-2023学年高一10月月考化学试题黑龙江省鹤岗市绥滨县第一中学2021-2022学年高三上学期期中考试化学试题微专题(二)——氧化还原反应的简单规律及应用微专题(四) 氧化还原反应的简单规律及应用辽宁省大连市第八中学2021-2022学年高一上学期12月月考化学试题辽宁省沈阳市第十中学2023-2024学年高一上学期12月份考试化学试题
名校
3 . 已知在酸性条件下有以下反应关系:
①KBrO3能将I-氧化成KIO3,本身被还原为Br2;
②Br2能将I-氧化为l2;
③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,本身被还原为l2。
酸性条件下,向KBrO3溶液中滴加少量KI溶液后,氧化还原产物为
①KBrO3能将I-氧化成KIO3,本身被还原为Br2;
②Br2能将I-氧化为l2;
③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,本身被还原为l2。
酸性条件下,向KBrO3溶液中滴加少量KI溶液后,氧化还原产物为
| A.Br-、I2 | B.Br2、 | C.Br2、Br-、I2 | D.Br2、I2、 |
您最近一年使用:0次
4 . 在硝化细菌作用下,溶液中铵根可发生反应: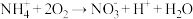 +下列说法错误的是
+下列说法错误的是
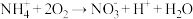 +下列说法错误的是
+下列说法错误的是A. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
| B.氧化剂与还原剂的物质的量之比为1:2 |
| C.反应一段时间后,溶液的酸性增强 |
D.1mol 完全反应,转移电子8mol 完全反应,转移电子8mol |
您最近一年使用:0次
2020-09-26更新
|
185次组卷
|
5卷引用:上海市复兴高级中学2019-2020学年高三上学期10月检测化学试题
2012·上海虹口·二模
5 . 阅读下列材料,并完成相应填空,制备碘的方法之一是从碘酸盐开始,共分为两步。
(1)第一步的反应为:NaIO3 + 3NaHSO3=NaI + 3NaHSO4,此反应中氧化剂为_______ ,被氧化的元素为________ 。
(2)第二步的反应共包含NaIO3、NaI、I2、Na2SO4、NaHSO4和H2O六种物质,请完成并配平方程式:_________ → ________ 。
(3)第二步反应中氧化产物与还原产物的物质的量之比为________ ,当有1.5mol氧化产物生成时,转移电子的物质的量为________ mol。
(4)要使碘的产率最高,全程投入的NaIO3与NaHSO3的总物质的量之比为_________ 。
(1)第一步的反应为:NaIO3 + 3NaHSO3=NaI + 3NaHSO4,此反应中氧化剂为
(2)第二步的反应共包含NaIO3、NaI、I2、Na2SO4、NaHSO4和H2O六种物质,请完成并配平方程式:
(3)第二步反应中氧化产物与还原产物的物质的量之比为
(4)要使碘的产率最高,全程投入的NaIO3与NaHSO3的总物质的量之比为
您最近一年使用:0次
2012·上海虹口·二模
解题方法
6 . 次氯酸钠(NaClO)固体在一定条件下发生分解反应,可能形成的产物是
| A.NaCl和O2 | B.NaClO3和O2 | C.NaClO3和Cl2 | D.NaClO3和NaCl |
您最近一年使用:0次
7 . 高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:2K2FeO4 + 16HCl → 4 KCl + 2FeCl3 + 8 H2 O + 3Q ↑,下列说法正确的是
| A.反应中涉及的6种物质均为电解质 |
| B.当电子转移0.5NA时,生成氯气5.6 L |
| C.可用湿润的淀粉碘化钾试纸检验产物Q |
| D.反应中氧化剂与还原剂的物质的量之比为1∶8 |
您最近一年使用:0次
8 . 下列反应中,二氧化硫既不是氧化剂又不是还原剂的是
| A.SO2+NO2=SO3+NO | B.SO2+2NaOH=H2O+Na2SO3 |
C.SO2+2Mg  2MgO+S 2MgO+S | D.SO2+Br2+2H2O=H2SO4+2HBr |
您最近一年使用:0次
2019-10-26更新
|
93次组卷
|
2卷引用:上海市同济中学2016-2017学年高二上学期期末考试化学试题
9 . 高温下炼铁的主要反应为:Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g) - Q
(1)写出该反应的平衡常数的表达式_____________________ 。当混合气体的________________ (填物理量名称)不变时,表明上述反应已达到平衡。
(2)写出一种能提高上述反应中氧化铁转化率的措施__________________ 。取一定量铝热剂,在高温下进行铝热反应:2Al + Fe2O3  2Fe + Al2O3。
2Fe + Al2O3。
(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁_______ g。
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
_____________________________________________
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
______________________________________________________________________
______________________________________________________________________
(1)写出该反应的平衡常数的表达式
(2)写出一种能提高上述反应中氧化铁转化率的措施
 2Fe + Al2O3。
2Fe + Al2O3。(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
您最近一年使用:0次
2017-04-19更新
|
335次组卷
|
2卷引用:2017届上海市虹口区高三二模化学试卷
10 . 室温下,H2 + Cl2  2HCl 生成 0.1 mol HCl,下列说法正确的是
2HCl 生成 0.1 mol HCl,下列说法正确的是
 2HCl 生成 0.1 mol HCl,下列说法正确的是
2HCl 生成 0.1 mol HCl,下列说法正确的是| A.生成 0.1 NA 根共价键 |
| B.消耗反应物总体积 2.24L |
| C.转移了 2 NA 个电子 |
| D.产物溶于水后,溶液 pH=1 |
您最近一年使用:0次



