名校
解题方法
1 . 硫元素的几种化合物及其单质存在下列转化关系(反应条件省略)。

下列判断不正确的是

下列判断不正确的是
A.反应①中氧化剂与还原剂物质的量之比为 |
B.反应②表明 具有酸性氧化物的性质 具有酸性氧化物的性质 |
| C.反应③的原子利用率是100% |
D.反应④中稀 是氧化剂 是氧化剂 |
您最近一年使用:0次
2023-12-27更新
|
243次组卷
|
9卷引用:山东省菏泽市第一中学2023-2024学年高一上学期第三次月考化学试题
山东省菏泽市第一中学2023-2024学年高一上学期第三次月考化学试题山东省菏泽市曹县第一中学2023-2024学年高一上学期 月考化学试题辽宁省锦州市2019-2020学年高一下学期期末考试化学试题(已下线)5.1.3 不同价态含硫物质的转化-2021-2022学年高一化学课后培优练(人教版2019必修第二册)湖北省竹山县第二中学2021-2022学年高一下学期第一次月考化学试题浙江省玉环市玉城中学2021-2022学年高一下学期开学考试化学试题第五章 化工生产中的重要非金属元素(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第01练 硫及其化合物-2023年【暑假分层作业】高一化学(人教版2019必修第二册)第3课时 不同价态含硫物质的转化
名校
2 . 关于反应 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是A.该反应中 中N元素被氧化 中N元素被氧化 |
| B.氧化产物与还原产物的物质的量之比为3∶4 |
C.反应中每生成1.4mol  时转移的电子数为4.8 时转移的电子数为4.8 |
D. 发生还原反应 发生还原反应 |
您最近一年使用:0次
2023-12-01更新
|
160次组卷
|
3卷引用:山东省菏泽市鄄城县第一中学2023-2024学年高一上学期12月月考化学试题
3 . 含钡的三效催化剂常用于处理汽车尾气,催化表面的物质转化过程如图所示。下列说法正确的是


| A.转化过程中的所有反应,氮元素均被还原 |
| B.依据图示判断催化剂参与化学反应 |
C.“还原”过程中生成 气体,转移 气体,转移 电子 电子 |
D.“储存”过程中,当 中 中 时,理论上消耗的 时,理论上消耗的 与O2的物质的量之比为 与O2的物质的量之比为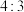 |
您最近一年使用:0次
名校
4 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO3还原法制备保险粉的流程如图所示。下列说法正确的是


A.反应1的离子方程式为 |
| B.反应1结束后,可用盐酸酸化的BaCl2溶液检验NaHSO3是否被氧化 |
| C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2 |
| D.反应2以及结晶脱水均可在空气中进行 |
您最近一年使用:0次
2023-01-15更新
|
783次组卷
|
5卷引用:山东省菏泽市鄄城县第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 向200 mL某稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列说法正确的是


A.OA段发生反应的离子方程式为 |
| B.OA段和BC段生成气体的物质的量之比为2∶1 |
| C.溶液中H2SO4与HNO3的物质的量浓度之比为2∶1 |
| D.C点时溶液的溶质为FeSO4和Fe(NO3)2 |
您最近一年使用:0次
2023-01-15更新
|
280次组卷
|
3卷引用:山东省菏泽市鄄城县第一中学2022-2023学年高一上学期期末考试化学试题
名校
6 . 已知有如下反应:
①
②
根据上述反应,下列说法正确的是
①

②

根据上述反应,下列说法正确的是
| A.NaBrO3中Br的化合价为+5 |
B.反应①中氧化性: |
| C.反应②中氧化产物与还原产物的物质的量之比为1∶5 |
| D.反应②中每生成3 mol Cl2,转移5 mol电子 |
您最近一年使用:0次
7 . 已知反应: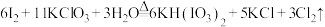 ,下列说法正确的是
,下列说法正确的是
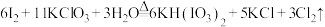 ,下列说法正确的是
,下列说法正确的是A.还原产物只有 |
| B.反应中氧化剂和还原剂的物质的量之比为6:11 |
C.可用碱石灰吸收反应产生的 制备漂白粉 制备漂白粉 |
D.产生 (标准状况) (标准状况) 时,转移 时,转移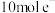 |
您最近一年使用:0次
解题方法
8 . 铁、氯元素的单质及化合物与生产、生活密切相关,请回答下列问题。
(1)铁元素与人体健康密切相关,工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,原因是NaNO2把人体内血红蛋白中的Fe2+转化为Fe3+而失去与O2结合的能力。上述事实说明NaNO2具有_______ 性,工业盐中毒后,可服用维生素C来缓解中毒状况,说明维生素C具有_______ 性。
(2)含氯消毒剂在生产生活中有着广泛的用途。
①写出实验室实中用二氧化锰与浓盐酸制取氯气的离子方程式_______ ,在制备和收集氯气的实验过程中,下列选项正确的是_______ (填字母)。
a.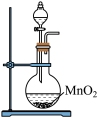 b.
b. 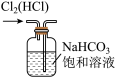 c.
c. 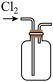 d.
d. 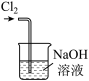
A.用装置a制取氯气 B.用装置b除去氯气中的少量氯化氢
C.用装置c收集氯气 D.用装置d吸收多余的氯气
②实验室也可以用高锰酸钾与浓盐酸制取氯气。已知KMnO4与浓盐酸反应的化学方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。0.1molKMnO4发生上述反应,消耗_______ molHCl,其中有_______ molHCl被氧化。分别利用二氧化锰和高锰酸钾制备等量的氯气,消耗HCl的物质的量之比为_______ 。
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ 。
④氯气通入石灰乳中可以制得漂白粉,氯气被氧化得到的产物是_______ ,还原剂与氧化剂的质量之比为_______ 。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 的个数比为1∶3,则被氧化与被还原的氯气物质的量之比为
的个数比为1∶3,则被氧化与被还原的氯气物质的量之比为_______ 。
(1)铁元素与人体健康密切相关,工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,原因是NaNO2把人体内血红蛋白中的Fe2+转化为Fe3+而失去与O2结合的能力。上述事实说明NaNO2具有
(2)含氯消毒剂在生产生活中有着广泛的用途。
①写出实验室实中用二氧化锰与浓盐酸制取氯气的离子方程式
a.
 b.
b.  c.
c.  d.
d. 
A.用装置a制取氯气 B.用装置b除去氯气中的少量氯化氢
C.用装置c收集氯气 D.用装置d吸收多余的氯气
②实验室也可以用高锰酸钾与浓盐酸制取氯气。已知KMnO4与浓盐酸反应的化学方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。0.1molKMnO4发生上述反应,消耗
③实验室还可以利用如下反应制取氯气:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
④氯气通入石灰乳中可以制得漂白粉,氯气被氧化得到的产物是
 的个数比为1∶3,则被氧化与被还原的氯气物质的量之比为
的个数比为1∶3,则被氧化与被还原的氯气物质的量之比为
您最近一年使用:0次
名校
解题方法
9 . 某工业生产中有一主要反应: ,其中
,其中 中
中 为+2价。下列说法正确的是
为+2价。下列说法正确的是
 ,其中
,其中 中
中 为+2价。下列说法正确的是
为+2价。下列说法正确的是A.氧化剂为 ,还原剂为 ,还原剂为 |
B.氧化产物是 ,还原产物是 ,还原产物是 和 和 |
C.当转移 电子时,有 电子时,有 参加反应 参加反应 |
D.氧化性 |
您最近一年使用:0次
2021-01-27更新
|
197次组卷
|
2卷引用:山东省菏泽地区2020-2021学年高一上学期期末联考化学试题
名校
解题方法
10 . SO2通入足量Fe(NO3)3稀溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程,下列说法不正确的是( )
| A.上述过程中,最终被还原的是NO3- |
| B.从上述过程中可以得出氧化性:稀硝酸>稀硫酸>Fe3+ |
| C.上述过程中,会产生一种无色的难溶于水的气体 |
| D.若通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积比为3∶2 |
您最近一年使用:0次
2019-12-05更新
|
560次组卷
|
7卷引用:山东省菏泽一中南京路校区2023-2024学年高一上学期1月月考化学试题
山东省菏泽一中南京路校区2023-2024学年高一上学期1月月考化学试题2015-2016学年天津市六校高一上学期期末化学试卷2015-2016学年安徽省六安一中高一下周末作业二化学试卷鲁科版必修一2019—2020学年第三章检测试题贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高一上学期期末考试化学试题(已下线)第三单元 物质的性质与转化(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)山东省枣庄市第八中学2022-2023学年高一上学期期末考试化学试题



