解题方法
1 . 三聚氯氰(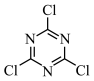 )是许多农药、活性染料和荧光增白剂的重要原料,实验室可用如图所示装置制备(部分装置省略)。
)是许多农药、活性染料和荧光增白剂的重要原料,实验室可用如图所示装置制备(部分装置省略)。

回答下列问题:
(1)仪器a的名称为___________ 。
(2)检查装置B的气密性操作为___________ 。
(3)装置A的作用为___________ 。可选用的试剂为___________ (填标号),发生反应的离子方程式为___________ 。
A.浓盐酸和MnO2 B.盐酸和KMnO4
(4)装置B中盛放的试剂是___________ ,该装置的作用是___________ 。
(5)装置C中是为了获得氯化氰(CNCl)。发生反应的化学方程式为___________ 。
(6)装置E出来的尾气中含有___________ (填化学式),可用___________ (填试剂)除去。
 )是许多农药、活性染料和荧光增白剂的重要原料,实验室可用如图所示装置制备(部分装置省略)。
)是许多农药、活性染料和荧光增白剂的重要原料,实验室可用如图所示装置制备(部分装置省略)。
回答下列问题:
(1)仪器a的名称为
(2)检查装置B的气密性操作为
(3)装置A的作用为
A.浓盐酸和MnO2 B.盐酸和KMnO4
(4)装置B中盛放的试剂是
(5)装置C中是为了获得氯化氰(CNCl)。发生反应的化学方程式为
(6)装置E出来的尾气中含有
您最近一年使用:0次
2022-03-24更新
|
368次组卷
|
3卷引用:广东省汕头市潮南区陈店实验学校2021-2022学年高二下学期第一次月考化学试题
广东省汕头市潮南区陈店实验学校2021-2022学年高二下学期第一次月考化学试题吉林省白山市2021-2022学年下学期高三第一次模拟考试理综化学试题(已下线)三轮冲刺卷03-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)
名校
解题方法
2 . 无水  是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水  的实验装置如图所示:
的实验装置如图所示:

E和G用来收集产物。回答下列问题:
(1)在E、G处收集产物是利用了
___________ 的性质。
(2)实验过程中若F处出现堵塞,则在B处可观察到的现象是___________ 。可通过___________ (填简单操作),使实验能继续
(3)Ⅰ中反应的离子方程式为___________ 。
(4)实验室中还常用 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为___________ 。检验水合三氯化铁原料中是否存在 的试剂是
的试剂是___________ 。
 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水  的实验装置如图所示:
的实验装置如图所示:
E和G用来收集产物。回答下列问题:
(1)在E、G处收集产物是利用了

(2)实验过程中若F处出现堵塞,则在B处可观察到的现象是
(3)Ⅰ中反应的离子方程式为
(4)实验室中还常用
 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为 的试剂是
的试剂是
您最近一年使用:0次
解题方法
3 . 实验室利用下图装置制备 ,并探究其性质。据图回答下列问题:
,并探究其性质。据图回答下列问题:
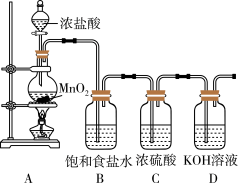
(1)组装该装置的一般原则是___________ ,气密性检查应在盛装药品___________ (填“前”或“后”)。
(2)B为洗气装置,制作它需要玻璃导管、双孔塞,还有___________ (填写所需仪器的名称)。
(3)A中发生反应的化学方程式为___________ 。
(4)制备 的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是
的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________ 。除上述不足外,是否存在“设计错误”___________ (填是或否)。
(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入 溶液,有紫红色的高铁酸钾(
溶液,有紫红色的高铁酸钾( )生成,由此可知
)生成,由此可知 具有
具有___________ 性(填“氧化”或“还原”),根据提示完成并配平该反应的化学方程式:___________ 。
提示: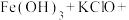 _______
_______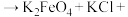 _______(未配平)
_______(未配平)
 ,并探究其性质。据图回答下列问题:
,并探究其性质。据图回答下列问题:
(1)组装该装置的一般原则是
(2)B为洗气装置,制作它需要玻璃导管、双孔塞,还有
(3)A中发生反应的化学方程式为
(4)制备
 的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是
的反应是放热反应,反应温度升高时有副反应发生,改进该实验装置以减少副反应发生的方法是(5)在一支试管中依次加入氢氧化铁和氢氧化钾溶液,再加入
 溶液,有紫红色的高铁酸钾(
溶液,有紫红色的高铁酸钾( )生成,由此可知
)生成,由此可知 具有
具有提示:
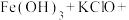 _______
_______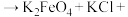 _______(未配平)
_______(未配平)
您最近一年使用:0次
2022-01-24更新
|
81次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2022-2023学年高一上学期第三次月考试化学试题
名校
解题方法
4 . 水合肼(N2H4·H2O)及其衍生物在许多工业中被广泛的使用。利用NaClO氧化尿素制备水合肼的实验流程如图所示:
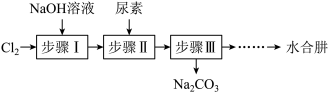
已知:①氯气与NaOH溶液的反应是放热反应,温度高时,易生成NaClO3;②N2H4·H2O的沸点约为118℃,有强还原性,能与NaClO剧烈反应生成N2。
下列说法错误的是

已知:①氯气与NaOH溶液的反应是放热反应,温度高时,易生成NaClO3;②N2H4·H2O的沸点约为118℃,有强还原性,能与NaClO剧烈反应生成N2。
下列说法错误的是
| A.步骤I、II反应过程中需控制好温度 |
| B.步骤II中可将尿素水溶液逐滴滴入NaClO碱性溶液中 |
C.步骤II中生成水合肼的离子方程式为:ClO—+CO(NH2)2+2OH—=Cl—+N2H4·H2O+CO |
| D.步骤III所得副产物Na2CO3溶液可用于工业上吸收SO2尾气 |
您最近一年使用:0次
名校
5 . 下图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略):

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:___________ 。
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、___________ 、干燥的有色布条。
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:___________
(5)装置F的作用是:___________ 。
(6)反应G中的离子方程式为___________ 。
(7)设计最简单的实验方案验证E中生成的固体中存在HCO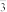 :
:___________ 。

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:
(5)装置F的作用是:
(6)反应G中的离子方程式为
(7)设计最简单的实验方案验证E中生成的固体中存在HCO
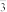 :
:
您最近一年使用:0次
2021-11-27更新
|
138次组卷
|
2卷引用:河北省邢台市第一中学2021-2022学年高一上学期第二次月考化学试题
解题方法
6 . 无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用Al和氯气通过下装置制备。已知A中产生的氯气混有少许HCl和水蒸气。则下列说法正确的是
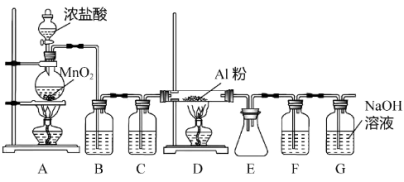

| A.试剂瓶B、C、F中分别盛饱和NaHCO3、浓硫酸、浓硫酸 |
| B.氯化铝产品最后在装置E中收集 |
| C.A、D两处酒精灯,实验开始时应先点燃A处 |
| D.装置F和G可用盛无水CaCl2的干燥管替换 |
您最近一年使用:0次
2021-11-26更新
|
1436次组卷
|
2卷引用:江西省丰城市第九中学2021-2022学年高一上学期第二次月考化学试卷
名校
解题方法
7 . Ⅰ.二氯砜(SO2Cl2)是一种发烟液体,遇水剧烈水解,69.1℃时沸腾。某小组拟用干燥的Cl2和SO2在活性炭催化下制备二氯砜。反应的方程式为: ,实验装置如图所示(部分夹持装置略去):
,实验装置如图所示(部分夹持装置略去):

(1)装置A中发生反应的离子反应方程式为___________ 。
(2)仪器C的名称为___________ ,冷凝管的进水口为___________ (选填“a”或“b”)。
(3)分液漏斗中盛放的最佳试剂为___________ ,装置B、D的作用为___________ 。
(4)装置F的作用为___________ 。
Ⅱ.二氯亚砜(SO2Cl2)也是一种发烟液体,常用作脱水剂,遇水会形成白雾,并有刺激性气味的气体逸出。
(5)写出二氯亚砜与水反应的化学方程式___________ 。
(6)用硫磺、液氯和SO3为原料,在一定条件下合成二氯亚砜(SOCl2),原子利用率可达 ,则三者的物质的量之比为
,则三者的物质的量之比为___________ 。
 ,实验装置如图所示(部分夹持装置略去):
,实验装置如图所示(部分夹持装置略去):
(1)装置A中发生反应的离子反应方程式为
(2)仪器C的名称为
(3)分液漏斗中盛放的最佳试剂为
(4)装置F的作用为
Ⅱ.二氯亚砜(SO2Cl2)也是一种发烟液体,常用作脱水剂,遇水会形成白雾,并有刺激性气味的气体逸出。
(5)写出二氯亚砜与水反应的化学方程式
(6)用硫磺、液氯和SO3为原料,在一定条件下合成二氯亚砜(SOCl2),原子利用率可达
 ,则三者的物质的量之比为
,则三者的物质的量之比为
您最近一年使用:0次
2021-11-11更新
|
773次组卷
|
3卷引用:甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题
8 . 铋酸钠(NaBiO3)广泛应用于制药业。其粉末呈浅黄色,不溶于冷水,遇沸水或酸则迅速分解。某同学设计如下实验,利用白色且难溶于水的Bi(OH)3在NaOH溶液中与Cl2反应制备NaBiO3,并探究其应用与纯度测定。请按要求回答下列问题:
Ⅰ. NaBiO3的制备,实验装置如下图(加热和夹持仪器已略去)
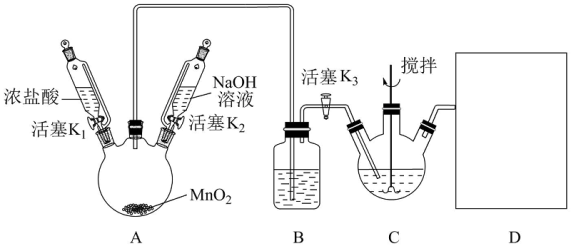
(1)B装置的作用是______ ;补全上图D装置图(并标注试剂名称) ____ 。
(2)C中反应的离子方程式为______ 。当观察到现象为_______ 时,可以初步判断C中反应已经完成。
(3)反应完成后,为从装置C中获得尽可能多的产品,需进行的操作:_______ 、过滤、洗涤、干燥。
Ⅱ.铋酸钠的应用,检测Mn2+
(4)向含有Mn2+的溶液中加入铋酸钠,再加入硫酸酸化,溶液变为紫红色,此反应中铋酸钠的作用是___________ 。
Ⅲ.产品纯度的测定
(5)取上述NaBiO3(Mr=280)产品a g,加入适量稀硫酸和MnSO4稀溶液使其完全转化为Bi3+,再用b mol·L-1的H2C2O4标准溶液滴定,当溶液紫红色恰好褪去时,消耗V mL标准溶液。该产品的纯度为___________ (用含a、b、V的代数式表示)。
Ⅰ. NaBiO3的制备,实验装置如下图(加热和夹持仪器已略去)

(1)B装置的作用是
(2)C中反应的离子方程式为
(3)反应完成后,为从装置C中获得尽可能多的产品,需进行的操作:
Ⅱ.铋酸钠的应用,检测Mn2+
(4)向含有Mn2+的溶液中加入铋酸钠,再加入硫酸酸化,溶液变为紫红色,此反应中铋酸钠的作用是
Ⅲ.产品纯度的测定
(5)取上述NaBiO3(Mr=280)产品a g,加入适量稀硫酸和MnSO4稀溶液使其完全转化为Bi3+,再用b mol·L-1的H2C2O4标准溶液滴定,当溶液紫红色恰好褪去时,消耗V mL标准溶液。该产品的纯度为
您最近一年使用:0次
解题方法
9 . 二氯化二硫(S2Cl2)可作硫、碘和某些有机物及金属化合物的溶剂,也可作橡胶硫化剂。一种由氯气与熔化的硫反应制取S2Cl2的装置(夹持和加热装置已省略)如图所示:

已知:①Cl2和S反应生成S2Cl2,同时有少量SCl2及其他氯化物生成;
②常温下,S2Cl2是一种浅黄色的油状液体,极易水解;
③S2Cl2的沸点为138℃,SCl2的沸点为59.6℃,硫的熔点为112.8℃、沸点为444.6℃。回答下列问题:
(1)已知S2Cl2分子结构与H2O2相似,则S2Cl2的结构式为__ ,装置B中盛放的试剂是___ 。
(2)A装置中发生反应的化学方程式为___ 。
(3)装置D中冷凝管的进水口是___ (填“a”或“b”)。
(4)要得到纯净的S2Cl2,需要进行的操作是将粗品___ 。
(5)F中碱石灰的作用是___ 。
(6)取约1mLS2Cl2于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为____ 。

已知:①Cl2和S反应生成S2Cl2,同时有少量SCl2及其他氯化物生成;
②常温下,S2Cl2是一种浅黄色的油状液体,极易水解;
③S2Cl2的沸点为138℃,SCl2的沸点为59.6℃,硫的熔点为112.8℃、沸点为444.6℃。回答下列问题:
(1)已知S2Cl2分子结构与H2O2相似,则S2Cl2的结构式为
(2)A装置中发生反应的化学方程式为
(3)装置D中冷凝管的进水口是
(4)要得到纯净的S2Cl2,需要进行的操作是将粗品
(5)F中碱石灰的作用是
(6)取约1mLS2Cl2于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为
您最近一年使用:0次
2021-10-26更新
|
403次组卷
|
2卷引用:山西省运城市2021-2022学年高三上学期10月质量检测化学试题
解题方法
10 . 常温常压下,将 缓慢通入
缓慢通入 水中至饱和,然后向所得饱和氯水中逐滴加入
水中至饱和,然后向所得饱和氯水中逐滴加入 溶液,整个过程中
溶液,整个过程中 的变化如图所示(不考虑
的变化如图所示(不考虑 、
、 挥发和
挥发和 的分解,忽略溶液体积变化)。下列说法正确的是
的分解,忽略溶液体积变化)。下列说法正确的是

已知:常温常压下, 水中溶解
水中溶解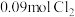 得到饱和氯水;
得到饱和氯水;
 缓慢通入
缓慢通入 水中至饱和,然后向所得饱和氯水中逐滴加入
水中至饱和,然后向所得饱和氯水中逐滴加入 溶液,整个过程中
溶液,整个过程中 的变化如图所示(不考虑
的变化如图所示(不考虑 、
、 挥发和
挥发和 的分解,忽略溶液体积变化)。下列说法正确的是
的分解,忽略溶液体积变化)。下列说法正确的是
已知:常温常压下,
 水中溶解
水中溶解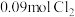 得到饱和氯水;
得到饱和氯水;
A.点①溶液中,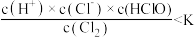 |
B.点②溶液中, |
C.点③溶液中, |
| D.点②和点④对应溶液导电能力几乎相同 |
您最近一年使用:0次



