解题方法
1 . Ⅰ.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)Ca(ClO)2中Cl的化合价为___________ ,Ca(ClO)2具有较强的_________ (填“氧化”或“还原”)性,是常用的漂白粉的有效成分。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为 ,该反应的离子方程式为:
,该反应的离子方程式为:___________ 。
②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):
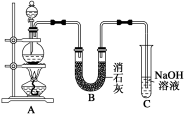
(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:___ 。
(4)C装置的作用是(用离子方程式表示)_____________ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于________ 中(填“冰水浴还是热水浴”)。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为______ 。
(1)Ca(ClO)2中Cl的化合价为
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为
 ,该反应的离子方程式为:
,该反应的离子方程式为:②NaClO可将酸性废水中的Fe2+氧化为Fe3+,本身被还原为NaCl,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题(消石灰为氢氧化钙):

(3)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式:
(4)C装置的作用是(用离子方程式表示)
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是将U型管置于
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为
您最近一年使用:0次
2 . 回答下列问题:
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是______ ,原因是______ 。
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸______ ,反应的化学方程式为____________ 。
(1)将新鲜的花瓣放入干燥的氯气中可观察到的现象是
(2)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸
您最近一年使用:0次
3 . 氯气与碱的反应:
(1)与_______ 反应制漂白液,化学方程式:_______ 。漂白液的有效成分_______ 。
(2)制漂白粉化学方程式:_______ ,漂白粉的有效成分为_______ 。
(1)与
(2)制漂白粉化学方程式:
您最近一年使用:0次
4 . FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。常见水处理剂还有高铁酸盐及ClO2,请回答下列问题:
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式________________ ;高铁酸盐是一种绿色净水剂,其有效成分是高铁酸根FeO 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:_______________
(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式_________________
(4)描述实验室制备氢氧化铁胶体的方法______________ ;写出对应的化学方程式_______________
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:_____ 。
___________ClO + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
(1)FeCl3可以用来刻蚀铜箔制造电路板,写出对应离子方程式
 。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:
。能消毒,且能净水。工业上常在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠,该反应的化学方程式为:(2)ClO2是一种高效、低毒的消毒剂,工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(3)漂白粉在工业中常用氯气通入石灰乳来制备,写出对应化学方程式
(4)描述实验室制备氢氧化铁胶体的方法
(5)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3,配平下列反应:
___________ClO
 + _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
+ _____Fe2+ + _____ ( ) = ____Fe3+ + ___ Cl-+ _______ ( )
您最近一年使用:0次
名校
5 . “7•20”特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和ClO2等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理____ ,标况下56L氯气完全被吸收,需要____ L1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为_____ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论____ (填“同意”或“不同意”),若不同意,你认为的结论是____ (若同意,此空不用填)
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是_____ (从①②③中选填)。
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为_____ 。ClO2还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式_____ 。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为
您最近一年使用:0次
6 . 已知A、B、C、D、E是中学化学中的常见气体,它们都是由1-18号元素组成的单质或化合物,并有如下的信息:
①A气体能使湿润的红色石蕊试纸变蓝;
②B气体通入品红溶液,红色褪去,继续加热,溶液又变红色;
③C气体通入紫色石蕊试液,溶液先变红色,迅速变为无色;
④D为红棕色、有刺激性气味的气体,能和水反应生成无色气体。
⑤E为黄绿色的、有刺激性气味的气体。
试确定它们的化学式:A_____ ,B____ ,C____ ,D____ ,E____ 。
①A气体能使湿润的红色石蕊试纸变蓝;
②B气体通入品红溶液,红色褪去,继续加热,溶液又变红色;
③C气体通入紫色石蕊试液,溶液先变红色,迅速变为无色;
④D为红棕色、有刺激性气味的气体,能和水反应生成无色气体。
⑤E为黄绿色的、有刺激性气味的气体。
试确定它们的化学式:A
您最近一年使用:0次
2022-12-03更新
|
233次组卷
|
2卷引用:吉林江城中学2021-2022学年高三上学期9月月考化学试题
解题方法
7 . 填空
(1)金属钠与水反应的化学方程式:_______
(2)写出次氯酸见光分解的化学方程式:_______
(3)写出氯气和氢氧化钠溶液反应的离子方程式 :_______
(1)金属钠与水反应的化学方程式:
(2)写出次氯酸见光分解的化学方程式:
(3)写出氯气和氢氧化钠溶液反应的
您最近一年使用:0次
解题方法
8 . ①纯碱、②浓盐酸、③漂白粉、④小苏打、⑤氯气、⑥烧碱等均为重要的化工原料。
回答下列问题:
(1)上述物质中属于混合物的是_______ (填序号,下同);属于碱的是_______ 。
(2)小苏打的化学式为_______ 。
(3)纯碱在水中的电离方程式为_______ 。
(4)实验室制备 的化学方程式为
的化学方程式为_______ 。
(5)写出工业上制备漂白粉的化学方程式:_______ 。
回答下列问题:
(1)上述物质中属于混合物的是
(2)小苏打的化学式为
(3)纯碱在水中的电离方程式为
(4)实验室制备
 的化学方程式为
的化学方程式为(5)写出工业上制备漂白粉的化学方程式:
您最近一年使用:0次
9 . 科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:
Ⅰ.实验室制备和收集氯气的常用装置如下图。
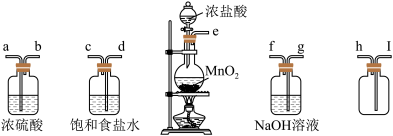
(1)利用该装置制备氯气的化学方程式为_______ 。
(2)在实验过程中饱和食盐水的作用是_______ 。
(3)实验装置接口的连接顺序为e→_______→_______→_______→_______→i→h→g→f。_______
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和_______ ,若反应产生0.5molCl2,则反应转移的电子数是_______ 。
II.漂白粉的制备( 装置如图所示)
查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。

(5)装置C中发生反应的化学方程式为_______ 。
(6)多孔球泡的作用是_______ ,使用冰水浴的目的是_______ 。
Ⅰ.实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为
(2)在实验过程中饱和食盐水的作用是
(3)实验装置接口的连接顺序为e→_______→_______→_______→_______→i→h→g→f。
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和
II.漂白粉的制备( 装置如图所示)
查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2
 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。
(5)装置C中发生反应的化学方程式为
(6)多孔球泡的作用是
您最近一年使用:0次
解题方法
10 . 回答下列问题
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为_______ 。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是_______ ,这是因为氯气通入水中发生化学反应,生成了具有漂白性的物质:_______ (填化学式),化学方程式为_______ 。
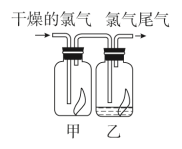
(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_______ 溶液吸收多余的氯气,原理是_______ (用化学方程式表示)。
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体主要是_______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是

(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
您最近一年使用:0次



