解题方法
1 . 回答下列问题:
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)9.03×1023个CO2的物质的量是_______ ,在标准状况下的体积为_______ 。
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为_______ ,所含氧原子数之比为_______ 。
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=_______ 。
(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为_______ 。
(6)FeCl2溶液通入氯气的反应,用离子方程式表示为_______ 。
(7)铜丝与浓硫酸反应的化学方程式为_______ ,若1molCu完全反应,则被还原的硫酸物质的量是_______ 。
(1)NaClO中Cl的化合价为
(2)9.03×1023个CO2的物质的量是
(3)质量比为11:7:16的CO2、CO、O2,其物质的量之比为
(4)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+、Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=(5)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。工业生产漂白粉的化学方程式为
(6)FeCl2溶液通入氯气的反应,用离子方程式表示为
(7)铜丝与浓硫酸反应的化学方程式为
您最近一年使用:0次
2 . 消毒液在我们日常生活中必不可少,请结合相关知识回答下列问题。
(1)生产消毒液是将氯气通入 溶液中,发生反应的化学方程式为:
溶液中,发生反应的化学方程式为:___________ 。
(2)取少量消毒液滴加 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有___________ 离子。向氯水中滴加紫色石蕊试剂的现象:___________ 。
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,该物质的化学式:___________ ;该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学方程式:___________ 。
(1)生产消毒液是将氯气通入
 溶液中,发生反应的化学方程式为:
溶液中,发生反应的化学方程式为:(2)取少量消毒液滴加
 溶液,现象是出现白色沉淀,说明消毒液中有
溶液,现象是出现白色沉淀,说明消毒液中有(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,该物质的化学式:
您最近一年使用:0次
解题方法
3 . 氯气与氢气在点燃条件下反应的实验现象:____________ 。
您最近一年使用:0次
4 . 某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次
名校
5 . 实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目_______ 。

 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_______ 倍(保留小数点后2位,消毒能力可以用氧化剂转移电子数来衡量)。
 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的
您最近一年使用:0次
名校
6 . 工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
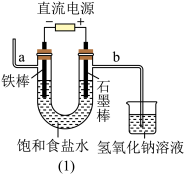
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
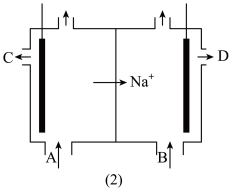
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近一年使用:0次
名校
7 . 向含有Fe2+、I-、Br- (已知还原性 >Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
>Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
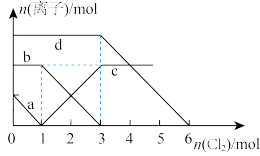
(1)图中线a、b、c、d依次代表___________ 、___________ 、___________ 、___________ 离子的物质的量变化情况(填写离子符号)。
(2)当通入2mol 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:___________ 。
(3)原溶液中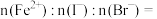
___________ 。
(4)在通入氯气的总反应中,下列离子方程式中不可能的发生的是___________
 >Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
>Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
(1)图中线a、b、c、d依次代表
(2)当通入2mol
 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:(3)原溶液中
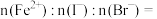
(4)在通入氯气的总反应中,下列离子方程式中不可能的发生的是___________
A. |
B. |
C.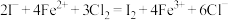 |
D. |
您最近一年使用:0次
8 . 碘及其化合物广泛应用于医药、染料等领域。 的一种制备方法如下:
的一种制备方法如下:
步骤1:向净化除氯后的海水中加入硝酸银溶液,得到AgI的悬浊液,静置,过滤。
步骤2:过滤后的沉淀与适量铁粉混合,加水搅拌,充分反应,静置,过滤。
步骤3:向滤液中通入适量氯气,得到含 的溶液。
的溶液。
(1)加入Fe粉进行转化反应的离子方程式为_______ ,“转化”步骤提高转化率的方法为_______ 。
(2)“氧化”时,理论上
_______ 。若氯气过量单质碘的收率会降低,原因是_______ 。
(3)“氧化”后溶液中的溶质可以制备 。
。 蒸汽状态下以双聚分子形式存在,其结构中含有四元环结构,画出该双聚分子的结构
蒸汽状态下以双聚分子形式存在,其结构中含有四元环结构,画出该双聚分子的结构_______ 。
(4)已知: 、
、 均可氧化
均可氧化 。酸性条件下,
。酸性条件下, 也可氧化
也可氧化 。以
。以 为原料制备
为原料制备 的实验方案为:
的实验方案为:_______ ,得到含 的溶液(可选用试剂:
的溶液(可选用试剂: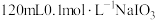 溶液、
溶液、 溶液、
溶液、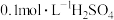 溶液)
溶液)
 的一种制备方法如下:
的一种制备方法如下:步骤1:向净化除氯后的海水中加入硝酸银溶液,得到AgI的悬浊液,静置,过滤。
步骤2:过滤后的沉淀与适量铁粉混合,加水搅拌,充分反应,静置,过滤。
步骤3:向滤液中通入适量氯气,得到含
 的溶液。
的溶液。(1)加入Fe粉进行转化反应的离子方程式为
(2)“氧化”时,理论上

(3)“氧化”后溶液中的溶质可以制备
 。
。 蒸汽状态下以双聚分子形式存在,其结构中含有四元环结构,画出该双聚分子的结构
蒸汽状态下以双聚分子形式存在,其结构中含有四元环结构,画出该双聚分子的结构(4)已知:
 、
、 均可氧化
均可氧化 。酸性条件下,
。酸性条件下, 也可氧化
也可氧化 。以
。以 为原料制备
为原料制备 的实验方案为:
的实验方案为: 的溶液(可选用试剂:
的溶液(可选用试剂: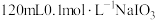 溶液、
溶液、 溶液、
溶液、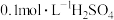 溶液)
溶液)
您最近一年使用:0次
名校
解题方法
9 . 下图是实验室用二氧化锰和浓盐酸制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)该实验中A部分的装置是___________ (填写下列装置的序号)。发生反应的化学方程式是___________ 。
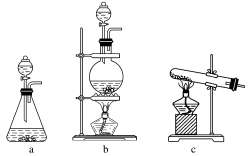
(2)装置B中饱和食盐水的作用是___________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___________ 。
(4)装置F的作用为___________ 。若用NaOH溶液替代Na2SO3溶液,则发生反应的离子方程式为___________ 。

(1)该实验中A部分的装置是

(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 无水氯化钙 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F的作用为
您最近一年使用:0次
名校
10 . 价一类二维图是基于核心元素的化合价和物质类别研究物质的一种方法。钠元素的价一类二维图如图所示,通过该图,可以从不同角度认识含钠元素的物质的性质及其转化关系,图中a~e均为含钠元素的物质,b为白色固体。回答下列问题:
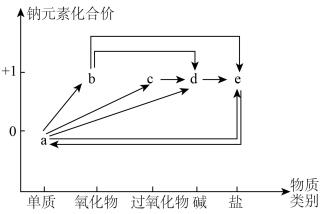
(1)a通常保存在______ 中,a与水反应时能说明a的密度比水小的现象是______ a在空气中加热时发生反应的化学方程式为______ (用单线桥法标明电子的转移情况)。
(2)c中阴、阳离子个数比为______ ,c常用作______ (填一种用途即可)。
(3)将氯气通入d的溶液中可制得漂白液,该反应的离子方程式为______ 。实验室制取氯气的装置如图:
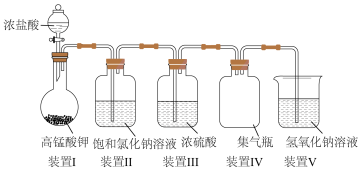
装置I中发生反应的离子方程式为______ ;完善装置Ⅳ:______ 。

(1)a通常保存在
(2)c中阴、阳离子个数比为
(3)将氯气通入d的溶液中可制得漂白液,该反应的离子方程式为

装置I中发生反应的离子方程式为
您最近一年使用:0次



