解题方法
1 . 工业上利用电解饱和食盐水可制得重要化工产品,该工业又称为“氯碱工业”。
(1)电解饱和食盐水的化学方程式为_______ ;常用_______ 检验与电源正极相连的电极上产生的气体,相关的化学方程式为_______ 。
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为_______ ;氯水不稳定,需现用现配,下列制备氯水的装置最合理的是_______ (填字母)。

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为_______ 。
(1)电解饱和食盐水的化学方程式为
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为
您最近一年使用:0次
解题方法
2 . 物质检验、分离、提纯和制备是化学实验中的常见操作。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是_______ (用离子方程式表示)。
(2)检验食盐中所含阳离子的实验操作名称是_______ 。
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是_______ 。
(4)除去Cl2中混有的HCl气体所用的试剂是_______ 。
(5)实验室制备氯气的化学反应方程式为_______ 请在方程式中标出电子转移的方向和数目。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是
(2)检验食盐中所含阳离子的实验操作名称是
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是
(4)除去Cl2中混有的HCl气体所用的试剂是
(5)实验室制备氯气的化学反应方程式为
您最近一年使用:0次
3 . 有以下7种生活中常见的物质:① ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:
(1)以上物质中属于电解质的是_______ (填序号,下同);属于碱的是_______ ;属于盐的是_______ 。
(2)①在水中电离的方程为_______ 。
(3)②与稀盐酸反应的离子方程式为_______ 。
(4)写出④转化成①的化学方程式_______ 。
(5)现设计实验由大理石( )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:_______ 。
 ;②氧化钠;③漂白粉;④
;②氧化钠;③漂白粉;④ ;⑤食盐水;⑥NaOH。回答下列问题:
;⑤食盐水;⑥NaOH。回答下列问题:(1)以上物质中属于电解质的是
(2)①在水中电离的方程为
(3)②与稀盐酸反应的离子方程式为
(4)写出④转化成①的化学方程式
(5)现设计实验由大理石(
 )、水、氯气来制取③:大理石(
)、水、氯气来制取③:大理石( )
) ③溶液
③溶液 ③,请写出在制取③的实验过程中发生的化学方程式:
③,请写出在制取③的实验过程中发生的化学方程式:
您最近一年使用:0次
解题方法
4 . A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
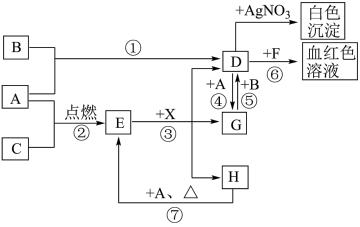
请回答下列问题:
(1)写出下列物质的化学式:X_______ 、F_______ 。
(2)反应④的离子方程式是_______
(3)反应①的化学方程式是_______ 。

请回答下列问题:
(1)写出下列物质的化学式:X
(2)反应④的离子方程式是
(3)反应①的化学方程式是
您最近一年使用:0次
解题方法
5 . 氯气能溶于水,其水溶液俗称氯水。按照表中要求完成氯水的性质实验,将实验现象及有关结论填入表中:
| 实验操作 | 实验现象 | 实验结论 |
 | ||
 |
您最近一年使用:0次
6 . 中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中 Cl2(aq)、HClO和 ClO-的物质的量分数(a)随pH变化的关系如图所示。
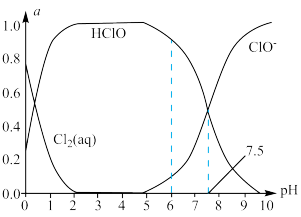
由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=___________ 时杀菌效果强,当pH=7.5时,氯水中含氯元素的微粒有 HClO、ClO-和___________ 。
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是___________ ;在使用时也不能与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为___________ 。
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为∶2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2CO2+2H2O ,每生成 1 mol ClO2,反应中转移电子___________ mol。
②在进行饮用水消毒时,ClO2可转化为Cl-,1 mol ClO2与___________ g(保留两位小数)NaClO氧化消毒能力相当(用得电子数目多少衡量氧化消毒能力强弱)。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中 Cl2(aq)、HClO和 ClO-的物质的量分数(a)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为∶2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2CO2+2H2O ,每生成 1 mol ClO2,反应中转移电子
②在进行饮用水消毒时,ClO2可转化为Cl-,1 mol ClO2与
您最近一年使用:0次
名校
解题方法
7 . 人类的生活离不开化工产品。化工产品的生产涉及反应原理、物料选择、能源消耗、工艺流程、环境保护等许多问题。请完成下列各题:
(1)下列符合实际并用于工业生产的是_______。
(2)有关工业制硫酸的下列说法中,正确的是_______。(多选)
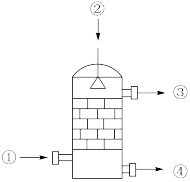
(3)在硫酸工业生产中,SO3的吸收过程是在吸收塔(如图)中进行,吸收塔里还装入了大量瓷杯。下列有关说法错误的是_______。
(1)下列符合实际并用于工业生产的是_______。
| A.NaOH与盐酸中和反应制NaCl | B.H2和Cl2光照制HCl |
| C.Cl2通入澄清石灰水中制漂白粉 | D.用硫磺制硫酸 |
| A.二氧化硫的催化氧化在转化器中发生 |
| B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫 |
| C.转化器中装有催化剂 |
| D.以硫磺为原料制硫酸使用的设备之一是沸腾炉 |

| A.从①处通入的气体中含大量SO3,整个吸收操作采取逆流的形式 |
| B.从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积 |
| C.从③处导出的气体只含有少量SO2,可直接排入大气 |
| D.从④处流出的是可用水或稀硫酸稀释的硫酸 |
您最近一年使用:0次
解题方法
8 . 图为实验室制取和收集纯净干燥的氯气,并进行氯气的性质实验的装置图:
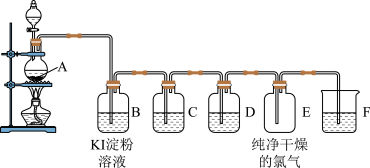
(1)装置A中所发生反应的化学方程式是_______________________________________ 。 若反应过程转移的电子的物质的量为0.4mol,则生成的Cl2体积(标准状况)为_______ L。
(2)装置B中的现象是__________ ,反应的化学方程式为________________________________ 。
(3)装置D中所装试剂是_________________ ,作用是____________________________________ 。
(4)装置F中所装试剂是_________________ ,作用是___________________________________ 。

(1)装置A中所发生反应的化学方程式是
(2)装置B中的现象是
(3)装置D中所装试剂是
(4)装置F中所装试剂是
您最近一年使用:0次
名校
9 . 现有下列物质:①熔融NaCl ② 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨ 过氧化钠 ⑩
⑧铜 ⑨ 过氧化钠 ⑩
(1)上述物质中属于电解质的是_______ (填标号)。
(2)将②逐滴加入⑥中的现象是_______ 。
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为_______ 。
(4)③通入石灰乳中,发生反应的离子方程式为_______ 。
(5)⑦与⑨反应的方程式为:_______ ,标准状况下,生成22.4L氧气转移的电子数目为_______ 。
 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨ 过氧化钠 ⑩
⑧铜 ⑨ 过氧化钠 ⑩
(1)上述物质中属于电解质的是
(2)将②逐滴加入⑥中的现象是
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为
(4)③通入石灰乳中,发生反应的离子方程式为
(5)⑦与⑨反应的方程式为:
您最近一年使用:0次
名校
解题方法
10 . 某兴趣小组设计如下装置进行氯气与金属钠的反应,先将钠预热,在钠熔融成小球时,撤火,并通入氯气发生反应。

(1)实验室制备氯气的化学方程式为_______ 。
(2) 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是_______ (填化学式)。
(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为_______ 。
(4)浸有NaOH溶液的棉球的作用是_______ 。若将 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为_______ 。

(1)实验室制备氯气的化学方程式为
(2)
 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为
 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为(4)浸有NaOH溶液的棉球的作用是
 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2022-12-08更新
|
230次组卷
|
2卷引用:北京市第五中学2022-2023学年高一上学期第二次阶段检测化学试题



