名校
解题方法
1 . 碘酸钙[Ca(IO3)2]是一种新型食品添加剂,实验室制取Ca(IO3)2的流程如图所示:

已知:HIO3易溶于水,不溶于有机溶剂;Ca(IO3)2不溶于乙醇,在水中的溶解度随温度降低而减小。
回答下列问题:
(1)实验室用MnO2固体和浓盐酸制取氯气的离子方程式为___________ 。
(2)“转化”步骤是为了获得碘酸,其装置如图(部分仪器已省略)。
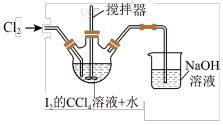
①“转化”反应在___________ (填仪器名称)中发生,其化学方程式为___________ 。
②判断“转化”反应完全的实验现象是___________ 。
(3)“分离”操作过程中所用的主要玻璃仪器是___________ ,验证所得水溶液中不含I2的方法是___________ 。
(4)加入CaCl2后保持在冰水浴中静置,抽滤,依次用冰水、乙醇洗涤,干燥。采用冰水浴的目的是___________ ;与过滤相比,抽滤的优点是___________ 。
(5)准确称取产品2.5000g,加酸溶解,转入250mL容量瓶内加水定容。移取25.00mL所配溶液,加入足量KI固体( +5I-+6H+=3I2+3H2O),暗处放置3min后,用0.2000mol·L-1Na2S2O3标准溶液滴定至溶液呈浅黄色(I2+2
+5I-+6H+=3I2+3H2O),暗处放置3min后,用0.2000mol·L-1Na2S2O3标准溶液滴定至溶液呈浅黄色(I2+2 =2I-+
=2I-+ ),滴入2~3滴淀粉溶液,继续滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液30.00mL。产品中Ca(IO3)2的质量分数为
),滴入2~3滴淀粉溶液,继续滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液30.00mL。产品中Ca(IO3)2的质量分数为___________ %。

已知:HIO3易溶于水,不溶于有机溶剂;Ca(IO3)2不溶于乙醇,在水中的溶解度随温度降低而减小。
回答下列问题:
(1)实验室用MnO2固体和浓盐酸制取氯气的离子方程式为
(2)“转化”步骤是为了获得碘酸,其装置如图(部分仪器已省略)。

①“转化”反应在
②判断“转化”反应完全的实验现象是
(3)“分离”操作过程中所用的主要玻璃仪器是
(4)加入CaCl2后保持在冰水浴中静置,抽滤,依次用冰水、乙醇洗涤,干燥。采用冰水浴的目的是
(5)准确称取产品2.5000g,加酸溶解,转入250mL容量瓶内加水定容。移取25.00mL所配溶液,加入足量KI固体(
 +5I-+6H+=3I2+3H2O),暗处放置3min后,用0.2000mol·L-1Na2S2O3标准溶液滴定至溶液呈浅黄色(I2+2
+5I-+6H+=3I2+3H2O),暗处放置3min后,用0.2000mol·L-1Na2S2O3标准溶液滴定至溶液呈浅黄色(I2+2 =2I-+
=2I-+ ),滴入2~3滴淀粉溶液,继续滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液30.00mL。产品中Ca(IO3)2的质量分数为
),滴入2~3滴淀粉溶液,继续滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液30.00mL。产品中Ca(IO3)2的质量分数为
您最近一年使用:0次
2 . 以生活中常见的调味品X为原料可以制备多种物质。下图是几种常见物质的转化关系图(部分产物和反应条件已略去),其中B、C、G都是单质,常温下B、C为气体,I为红棕色固体,J是白色沉淀。

请回答下列问题:
(1)C的化学式是___________ 。
(2)反应②的离子方程式是___________ 。
(3)H露置于空气中发生反应的化学方程式是___________ 。
(4)设计检验F中阳离子的实验方案___________ 。

请回答下列问题:
(1)C的化学式是
(2)反应②的离子方程式是
(3)H露置于空气中发生反应的化学方程式是
(4)设计检验F中阳离子的实验方案
您最近一年使用:0次
3 . 九种物质的转化关系如图所示。常温下,甲、乙、丙为气体,A、B为金属单质。(图中有些反应的产物和条件未标出)

(1)A的化学式为___________ ,其焰色试验为___________ 变化(填“物理”或“化学”)。
(2)向沸水中滴入几滴物质F的饱和溶液,并继续煮沸至红褐色,制得的分散系为___________ ,该反应的化学方程式为___________ 。
(3)向物质E的溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应的化学方程式___________ 。
(4)实验室保存物质E的水溶液时要加固体___________ ,其原因是___________ (用离子方程式解释)。

(1)A的化学式为
(2)向沸水中滴入几滴物质F的饱和溶液,并继续煮沸至红褐色,制得的分散系为
(3)向物质E的溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
(4)实验室保存物质E的水溶液时要加固体
您最近一年使用:0次
名校
解题方法
4 . 如图是一套制取并验证氯气部分化学性质的实验装置。已知:I2遇淀粉变蓝色。
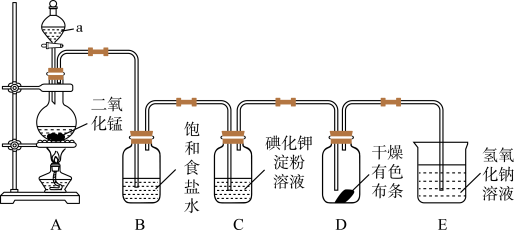
(1)装置A中,仪器a的名称___________ ,该仪器中盛放的试剂为___________ ,写出A装置发生反应的离子方程式:___________ 实验室用固体KClO3与浓HCl反应也可以制Cl2,反应的化学方程式为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,若该反应生成6.72L(标准状况)Cl2,转移的电子数为___________ mol。
(2)B装置中饱和食盐水的作用是___________ ;当有少量Cl2通过后,观察到装置C中溶液变成蓝色,反应的离子方程式为:___________ 说明氧化性Cl___________ I(填“>”或“<”)。
(3)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?___________ 。
(4)若要证明Cl2无漂白性,则必须在装置___________ (用装置字母序号填写)之前增加一个___________ 的装置。
(5)装置E的作用是尾气处理,该反应的离子方程式为___________ 。
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:___________ 。
(7)Cl2可用于自来水消毒,但Cl2会与水中的有机物发生反应,生成对人体有害的有机氯化物,因此,从2000年开始,国家开始逐渐用ClO2取代Cl2对自来水消毒。ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可利用KClO3与H2C2O4(已知H2C2O4为弱酸)在酸性条件下反应,制取ClO2.请写出该反应的离子方程式:___________ 。该反应中还原产物的化学式是___________ ,被氧化的元素是___________ (填元素符号)。

(1)装置A中,仪器a的名称
(2)B装置中饱和食盐水的作用是
(3)当Cl2持续通过时,装置D中干燥的有色布条能否褪色?
(4)若要证明Cl2无漂白性,则必须在装置
(5)装置E的作用是尾气处理,该反应的离子方程式为
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:
(7)Cl2可用于自来水消毒,但Cl2会与水中的有机物发生反应,生成对人体有害的有机氯化物,因此,从2000年开始,国家开始逐渐用ClO2取代Cl2对自来水消毒。ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可利用KClO3与H2C2O4(已知H2C2O4为弱酸)在酸性条件下反应,制取ClO2.请写出该反应的离子方程式:
您最近一年使用:0次
2023高一·全国·专题练习
解题方法
5 . 铁,铝是人类社会生活中应用最广泛的金属材料。现将铁,铝的混合物进行如图所示实验。已知反应: ,回答下列问题。
,回答下列问题。
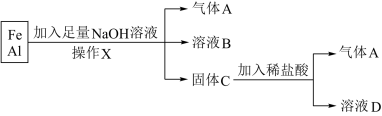
(1)操作X的名称是___________ 。
(2)气体A是___________ 。
(3)A与 混合光照后可能发生爆炸,生成
混合光照后可能发生爆炸,生成___________ (填化学式),A在该反应中作为___________ (填“氧化剂”或“还原剂”)。
(4)溶液B中的负离子除 外,还有
外,还有___________ ,溶液D中存在的金属离子为___________ 。
 ,回答下列问题。
,回答下列问题。
(1)操作X的名称是
(2)气体A是
(3)A与
 混合光照后可能发生爆炸,生成
混合光照后可能发生爆炸,生成(4)溶液B中的负离子除
 外,还有
外,还有
您最近一年使用:0次
名校
6 . 自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。高铁酸钾(K2FeO4,极易溶于水)是常见的水处理剂,其原理如图所示。完成下列问题:
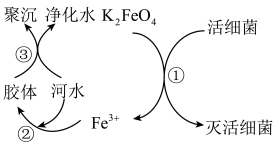
(1)K2FeO4的电离方程式______ 。过程①中K2FeO4表现了______ (填“氧化”或“还原”)性。
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有______ 、______ (填两个)。
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO______ K2FeO4。
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用单线桥法 表示电子转移的方向和数目说明______ ;
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:
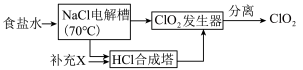
(4)该工艺中,需要补充的物质X为______ (填化学式,下同)。
(5)能参与循环的物质是______ 。
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:
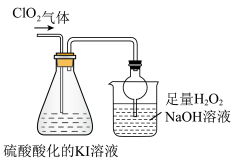
(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是______ 。
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是______ 。
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:______ 。
②请设计实验证明你的假设(仅用离子方程式表示):______ 。

(1)K2FeO4的电离方程式
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O
 NaClO3+3H2↑
NaClO3+3H2↑发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:

(4)该工艺中,需要补充的物质X为
(5)能参与循环的物质是
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:

(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:
②请设计实验证明你的假设(仅用离子方程式表示):
您最近一年使用:0次
2023-03-04更新
|
302次组卷
|
2卷引用:上海市杨浦高级中学2022-2023学年高一上学期期末考试化学试题
解题方法
7 .  在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。

已知:① ,
, ,
,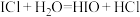
② 、
、 易溶于正己烷(分子式:
易溶于正己烷(分子式: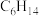 ,沸点:69℃)
,沸点:69℃)
③ 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,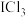 的正己烷溶液呈黄色
的正己烷溶液呈黄色
(1)装置A中反应的化学方程式为_______ 。
(2)仪器a的名称为_______ ,该装置的作用是_______ 。
(3)为使 和
和 充分反应,并溶解在正己烷中,对装置A进行的操作为
充分反应,并溶解在正己烷中,对装置A进行的操作为_______ 。
(4)从B、C、D、E、F中选择合适的装置制备 ,装置正确的连接顺序为A→
,装置正确的连接顺序为A→_______ 。
(5)制备 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是_______ ,当观察到C中的颜色变为_______ 色时,停止加热A装置。
(6)制备 时,
时,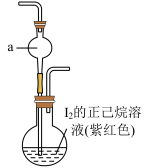 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有_______ (答一条即可)。
 在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。
已知:①
 ,
, ,
,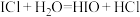
②
 、
、 易溶于正己烷(分子式:
易溶于正己烷(分子式: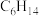 ,沸点:69℃)
,沸点:69℃)③
 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,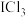 的正己烷溶液呈黄色
的正己烷溶液呈黄色(1)装置A中反应的化学方程式为
(2)仪器a的名称为
(3)为使
 和
和 充分反应,并溶解在正己烷中,对装置A进行的操作为
充分反应,并溶解在正己烷中,对装置A进行的操作为(4)从B、C、D、E、F中选择合适的装置制备
 ,装置正确的连接顺序为A→
,装置正确的连接顺序为A→(5)制备
 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是(6)制备
 时,
时, 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有
您最近一年使用:0次
名校
解题方法
8 . 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面框图进行反应,又知E溶液是无色的,请回答:
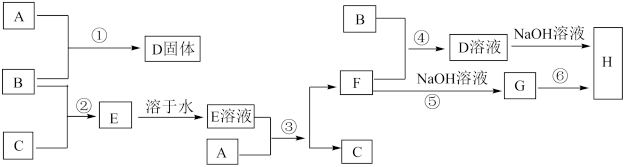
(1)A是_______ ,B是_______ ,C是_______ (均填化学式)。
(2)反应⑥的化学方程式为:_______ 。
(3)反应④的离子方程式为:_______ 。
(4)检验D溶液中阳离子的离子方程式为:_______ 。

(1)A是
(2)反应⑥的化学方程式为:
(3)反应④的离子方程式为:
(4)检验D溶液中阳离子的离子方程式为:
您最近一年使用:0次
9 . A~G为中学化学常见纯净物,常温常压下,A、B、D均为气体单质,且A为黄绿色,E为无色液体,F为淡黄色固体,它们之间的转化关系如下图所示。(反应条件及部分生成物已省略)
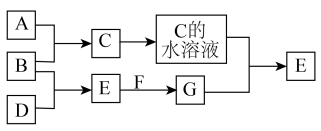
请回答下列问题:
(1)A与B反应的化学方程式是_______ 。
(2)D的化学式是_______ ,E的化学式是_______ 。
(3)E与F反应的化学方程式是_______ 。
(4)C的水溶液与G反应的离子方程式是_______ 。

请回答下列问题:
(1)A与B反应的化学方程式是
(2)D的化学式是
(3)E与F反应的化学方程式是
(4)C的水溶液与G反应的离子方程式是
您最近一年使用:0次
解题方法
10 . 利用电解饱和食盐水制备盐酸和漂白液的流程如图:

已知A是一种无色的气体,在空气中燃烧发出淡蓝色的火焰,B是一种黄绿色的有毒气体,C溶液能使酚酞变红色。请回答下列问题:
(1)步骤Ⅰ用到的玻璃仪器有玻璃棒、_______ 。
(2)步骤Ⅱ反应的化学方程式为:_____________________ 。
(3)步骤Ⅴ反应的离子方程式为:_____________________ 。
(4)往装有KI溶液的试管通入B,发生反应的离子方程式为:_____________________ 。

已知A是一种无色的气体,在空气中燃烧发出淡蓝色的火焰,B是一种黄绿色的有毒气体,C溶液能使酚酞变红色。请回答下列问题:
(1)步骤Ⅰ用到的玻璃仪器有玻璃棒、
(2)步骤Ⅱ反应的化学方程式为:
(3)步骤Ⅴ反应的离子方程式为:
(4)往装有KI溶液的试管通入B,发生反应的离子方程式为:
您最近一年使用:0次



