名校
解题方法
1 . 室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E溶液是无色溶液,F是淡绿色溶液。B和C反应发出苍白色火焰。请回答:
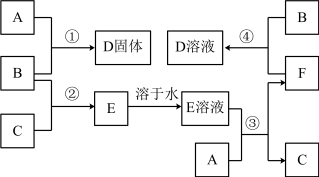
(1)A是_______ ,B是_______ (请填写化学式);
(2)反应①的化学方程式_______ ;
(3)反应③的离子方程式_______ ;
(4)反应④的离子方程式_______ 。

(1)A是
(2)反应①的化学方程式
(3)反应③的离子方程式
(4)反应④的离子方程式
您最近一年使用:0次
2021-06-16更新
|
506次组卷
|
5卷引用:河南省安阳市洹北中学2020-2021学年高一下学期期初考试化学试题
河南省安阳市洹北中学2020-2021学年高一下学期期初考试化学试题(已下线)2.2.1 氯及其化合物-2021-2022学年高一化学课后培优练(人教版2019必修第一册)江苏省南通西藏民族中学2022-2023学年高一上学期阶段测试化学试题(已下线)专题05 氯及其化合物【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)河南省周口恒大中学2023-2024学年高三下学期4月期中考试化学试题
解题方法
2 . 有X、Y、Z三种元素,已知:①X、Y、Z的单质在常温下均为气体;②X的单质可在Z的单质中燃烧,生成XZ,火焰为苍白色;③XZ极易溶于水,电离出X+和Z-,其水溶液可使蓝色石蕊试纸变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体;⑤Z单质溶于X2Y中,所得溶液具有漂白作用。
(1)推断X、Y、Z三种元素的名称为:X___________ ,Y___________ ,Z___________ 。
(2)化合物的化学式XZ为___________ ,X2Y为___________ 。Z的单质的化学式___________ 。
(3)五个过程中涉及的化学反应的方程式及电离方程式为
②___________
③___________
④___________
⑤___________
(1)推断X、Y、Z三种元素的名称为:X
(2)化合物的化学式XZ为
(3)五个过程中涉及的化学反应的方程式及电离方程式为
②
③
④
⑤
您最近一年使用:0次
3 . 某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如图: +H2O=2CuI↓+SO
+H2O=2CuI↓+SO +2H+
+2H+
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_______ 。
(2)反应③中CuI被氧化,还原产物只有NO2,当有95.5gCuI参与反应,产生的NO2在标况下的体积为_______ 。
(3)化合物B中含两种元素,铁元素原子与另一种元素原子的物质的量之比为3:8,则化合物B的化学式为_______ 。
(4)反应⑤中生成黑色固体磁性氧化铁和无色气体,则反应⑤的化学方程式为________ 。
(5)将足量的Cl2通入含12g NaI的溶液中,一段时间后把溶液蒸干、灼烧,得到的固体是______ ,其质量为_______ g。

 +H2O=2CuI↓+SO
+H2O=2CuI↓+SO +2H+
+2H+回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、
(2)反应③中CuI被氧化,还原产物只有NO2,当有95.5gCuI参与反应,产生的NO2在标况下的体积为
(3)化合物B中含两种元素,铁元素原子与另一种元素原子的物质的量之比为3:8,则化合物B的化学式为
(4)反应⑤中生成黑色固体磁性氧化铁和无色气体,则反应⑤的化学方程式为
(5)将足量的Cl2通入含12g NaI的溶液中,一段时间后把溶液蒸干、灼烧,得到的固体是
您最近一年使用:0次
2021-04-29更新
|
381次组卷
|
3卷引用:山东省临沂市临沂第二十四中学2020-2021学年高一下学期期中考试化学试题
21-22高一上·浙江·阶段练习
解题方法
4 . 室温下,单质A、单质B、单质C分别为固体、黄绿色气体、无色气体。在一定条件下,它们之间的转化关系如图所示,已知E溶液是无色的。请回答下列问题:
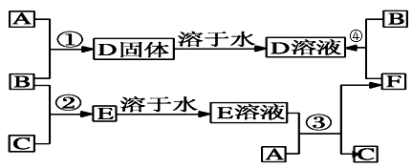
(1)反应①的化学方程式为___ 。
(2)反应③的化学方程式为____ 。
(3)反应④的化学方程式为___ 。

(1)反应①的化学方程式为
(2)反应③的化学方程式为
(3)反应④的化学方程式为
您最近一年使用:0次
解题方法
5 . 铁、铝的混合物进行如下实验:
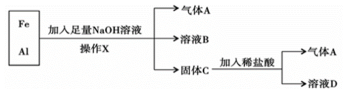
(1)操作X的名称是____ ;
(2)气体A是_____ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成___ (填化学式),A在该反应中作为____ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH-外还有____ (填离子符号),溶液D中存在的金属离子为___ (填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:____ ;

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH-外还有
(5)加入足量NaOH溶液时发生反应的离子方程式为:
您最近一年使用:0次
6 . 已知A、B、C均为单质, A是生产生活中用量最大的金属,室温下B是一种黄绿色气体,C是最轻的无色气体、也是一种良好的高能燃料,在合适的反应条件下,它们可以按下列框图进行反应。又知E溶液是无色的,C在B燃烧有苍白色火焰。

(已知Cl2+2FeCl2=2FeCl3 )请回答:
(1)试写出下列物质的化学式: A___________ ,B___________ 。
(2)反应①的化学反应方程式和现象:___________ ,___________ 。
(3)反应③的化学方程式:___________ 。
(4)工业上用黄绿色气体制备漂白粉的化学方程式:___________ 。

(已知Cl2+2FeCl2=2FeCl3 )请回答:
(1)试写出下列物质的化学式: A
(2)反应①的化学反应方程式和现象:
(3)反应③的化学方程式:
(4)工业上用黄绿色气体制备漂白粉的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,还可以作为贵金属的萃取剂。可由硫和氯气在100-110℃直接化合而成。实验室用如图装置制备S2Cl2,并利用尾气制备漂白粉。已知S2Cl2的熔点:-77℃,沸点:137℃。S2Cl2遇水剧烈反应。

(1)a中所装试剂为_______ 。
A.无水CuSO4 B.无水CaCl2 C.碱石灰 D.P2O5
(2)仪器b的名称为_______ 。
(3)S2Cl2遇水会生成一种黄色单质、一种能使品红褪色的气体(化合物)及酸雾,写出该反应的化学方程式_______ 。
(4)实验前向装置中通入N2的目的是_______ ,A、B装置中的空气可以通过控制K2、K3来去除,具体操作为_______ 。
(5)由于装置存在缺陷,实验制得的二氯化二硫可能不纯,请说明应如何改进_______ 。

(1)a中所装试剂为
A.无水CuSO4 B.无水CaCl2 C.碱石灰 D.P2O5
(2)仪器b的名称为
(3)S2Cl2遇水会生成一种黄色单质、一种能使品红褪色的气体(化合物)及酸雾,写出该反应的化学方程式
(4)实验前向装置中通入N2的目的是
(5)由于装置存在缺陷,实验制得的二氯化二硫可能不纯,请说明应如何改进
您最近一年使用:0次
2021-04-07更新
|
83次组卷
|
2卷引用:广西南宁市第三中学2020-2021学年高二下学期第一次月考化学(理)试题
8 . 常温下,一氧化二氯(C12O)为棕黄色气体,熔点为﹣116℃,浓度过高时易分解爆炸。为降低风险和便于贮存,制出C12O后,一般将其“固化”为固态。某小组按以下两阶段制备C12O。回答下列问题:
第一阶段:制备HgO。
配制15%的NaCl溶液和30%的HgC12溶液,将二者以一定质量比混合得到5%NaCl和20%HgC12的混合液;在室温下,边搅拌边缓慢地向混合液中加入过量NaOH溶液,生成黄色沉淀;将沉淀反复洗涤数次,直至没有氯离子;真空抽滤后将沉淀物在暗处干燥,得到干燥的HgO。
(1)配制15%NaCl溶液,除用到托盘天平和烧杯、玻璃棒外,还需要的玻璃仪器有___________ 。
(2)配制混合液时,15%NaCl溶液和30%HgC12溶液的质量比为___________ 。
(3)检验沉淀已经洗涤至没有氯离子的操作及现象为___________ 。
第二阶段:制备C12O。
制备干燥、纯净的C12;然后在干燥氮气的气流中,用C12和HgO在18~20℃条件下制备C12O;将产生的C12O气体“固化”;最后进行尾气处理。
(4)将干燥、纯净的C12通入下面装置中制备C12O并“固化”。

①制备C12O时还得到了HgC12·HgO固体,则装置I中制备反应的化学方程式为___________ 。干燥氮气的作用除将产生的C12O送入后续装置“固化”外,还有___________ 。
②常用冷却剂的数据如下表。“固化”时装置II中的冷却剂为___________ (填标号)。
A.液氯 B.液氨 C.干冰 D.液氧
第一阶段:制备HgO。
配制15%的NaCl溶液和30%的HgC12溶液,将二者以一定质量比混合得到5%NaCl和20%HgC12的混合液;在室温下,边搅拌边缓慢地向混合液中加入过量NaOH溶液,生成黄色沉淀;将沉淀反复洗涤数次,直至没有氯离子;真空抽滤后将沉淀物在暗处干燥,得到干燥的HgO。
(1)配制15%NaCl溶液,除用到托盘天平和烧杯、玻璃棒外,还需要的玻璃仪器有
(2)配制混合液时,15%NaCl溶液和30%HgC12溶液的质量比为
(3)检验沉淀已经洗涤至没有氯离子的操作及现象为
第二阶段:制备C12O。
制备干燥、纯净的C12;然后在干燥氮气的气流中,用C12和HgO在18~20℃条件下制备C12O;将产生的C12O气体“固化”;最后进行尾气处理。
(4)将干燥、纯净的C12通入下面装置中制备C12O并“固化”。

①制备C12O时还得到了HgC12·HgO固体,则装置I中制备反应的化学方程式为
②常用冷却剂的数据如下表。“固化”时装置II中的冷却剂为
| 物质 | O2 | CO2 | NH3 | Cl2 |
| 熔点/℃ | -218.4 | -78.5 | -77.3 | -101 |
| 沸点/℃ | -183 | 升华 | -33.35 | -34.6 |
您最近一年使用:0次
2021高三·浙江·专题练习
解题方法
9 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是___________________________________ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是_______________________________ 。“滤液”中的溶质主要是____________ 。“调pH”中发生反应的化学方程式为___________________________________ 。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
您最近一年使用:0次
解题方法
10 . 如图为物质转化关系,其中甲是一种金属单质,燃烧时,火焰为黄色。A、C、F常温下为气体;其中C为黄绿色,且A与C点燃时产生苍白色火焰,并且在瓶口有白雾出现。F为温室效应气体,乙为厨房中常用的一种盐,热稳定性强,灼烧时火焰为黄色。
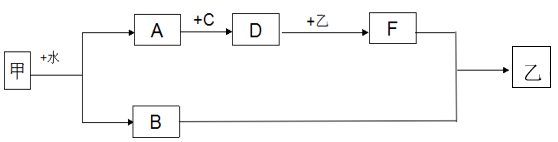
回答下列问题:
(1)写出下列的化学式:A:___ ,B:___ ,D:___ ,F:___ 。
(2)写出甲与水反应的化学方程式:___ 。
(3)写出D与乙反应的化学方程式:___ 。
(4)反应B和F反应的离子方程式:___ 。
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式___ 。

回答下列问题:
(1)写出下列的化学式:A:
(2)写出甲与水反应的化学方程式:
(3)写出D与乙反应的化学方程式:
(4)反应B和F反应的离子方程式:
(5)写出甲与氧气燃烧的产物与二氧化碳反应的化学方程式
您最近一年使用:0次



