名校
解题方法
1 . 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面框图进行反应,又知H是红褐色的沉淀,请回答:
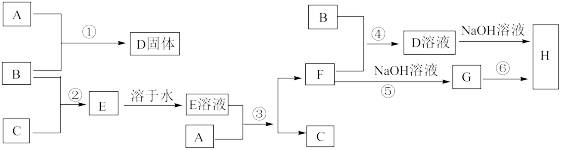
(1)A是_______ ,B是_______ ,C是_______ (填化学式)
(2)反应③的离子方程式为:_______ 。
(3)反应④的离子方程式为:_______ 。
(4)反应⑥的化学方程式为:_______ 。

(1)A是
(2)反应③的离子方程式为:
(3)反应④的离子方程式为:
(4)反应⑥的化学方程式为:
您最近一年使用:0次
解题方法
2 . 有三种金属单质A、B、C,其中A的焰色实验为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间有如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
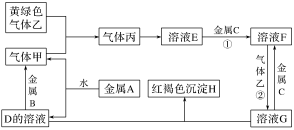
(1)写出下列物质的化学式:乙_______ 、H_______ ;
(2)写出反应②的离子方程式:_______
(3)写出气体甲与乙反应的化学方程式:_______
(4)F与D溶液反应后的产物在空气中转化为H的现象为_______ 。

(1)写出下列物质的化学式:乙
(2)写出反应②的离子方程式:
(3)写出气体甲与乙反应的化学方程式:
(4)F与D溶液反应后的产物在空气中转化为H的现象为
您最近一年使用:0次
3 . 化学无处不在,生活中我们消杀新冠病毒的‘84消毒液’有效成分是次氯酸钠,食盐主要成分是氯化钠、碱面成分碳酸钠、发酵粉碳酸氢钠、味精主要成分谷氨酸钠、洁厕灵主要成分是浓盐酸等,这些用品方面我们的生活。依据所学相关知识,完成下列试题。
I.含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取 的化学方程式为
的化学方程式为_______________ 。
(2)氢气在氯气中燃烧时现象是_______________ ,反应方程式子为_________________ 。该反应可以用于工业上制备盐酸。
(3)实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为_________ 。
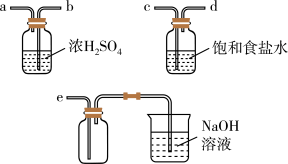
(4)其中饱和食盐水的作用为__________ ,常温下,NaOH溶液中反应的离子方程式为___________________ .
(5)某氯水久置后不能使品红溶液褪色,可推测氯水中________ (填化学式)已分解。检验此久置氯水中 存在的操作及现象是
存在的操作及现象是_____________________________ 。
II.关于 和的热稳定性研究。
和的热稳定性研究。
观察到的实验现象如下表所示:

根据上述实验现象,回答下列问题:
(6)加热 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是_______________________ 。
(7)加热 发生反应的化学方程式为
发生反应的化学方程式为________________________________ 。
(8)将(5)中久制氯水加入NaHCO3固体中反应的离子方程式为______________ 。
I.含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是
 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。(1)实验室沿用舍勒的方法制取
 的化学方程式为
的化学方程式为(2)氢气在氯气中燃烧时现象是
(3)实验室制取干燥
 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
(4)其中饱和食盐水的作用为
(5)某氯水久置后不能使品红溶液褪色,可推测氯水中
 存在的操作及现象是
存在的操作及现象是II.关于
 和的热稳定性研究。
和的热稳定性研究。观察到的实验现象如下表所示:

| 物质 | 装置B中现象 | 装置C中现象 |
 | 无明显变化 | 开始断断续续产生气泡,后没有气泡,溶液保持澄清 |
 | 白色粉末变蓝色 | 开始断断续续产生气泡,后产生连续气泡,溶液变浑浊 |
(6)加热
 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是(7)加热
 发生反应的化学方程式为
发生反应的化学方程式为(8)将(5)中久制氯水加入NaHCO3固体中反应的离子方程式为
您最近一年使用:0次
22-23高一上·全国·课时练习
名校
4 . X、Y、Z、W、R五种元素的性质或结构信息如表,根据表中的信息回答下列问题:
(1)写出元素R在元素周期表中的位置:_______ 。
(2)由X、Z、R三种元素形成的化合物XRZ的分子式为_______ 。
(3)W与Z的单质在加热条件反应的化学方程式是_______ 。
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:_______ ,燃烧片刻后取出燃烧管,迅速将集气瓶倒扣在过量的烧碱溶液中,可能产生的现象是_______ ,所得溶液中存在的溶质除了过量的NaOH外,还含有的是_______ (填化学式)。
| 元素 | X | Y | Z | W | R |
| 性质或 结构信息 | 单质是最轻的气体 | 常见单质为空气中的主要成分之一 | 是海水中质量分数最大的元素 | 原子核内有11个质子 | 原子核外有3个电子层,常见单质为气体 |
(2)由X、Z、R三种元素形成的化合物XRZ的分子式为
(3)W与Z的单质在加热条件反应的化学方程式是
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:
您最近一年使用:0次
5 . (一) 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,还可以作为贵金属的萃取剂。可由硫和氯气在100-110℃直接化合而成。实验室用以下装置制备S2Cl2,并利用尾气制备漂白粉。已知S2Cl2的熔点:-77℃,沸点:137℃。S2Cl2遇水剧烈反应。
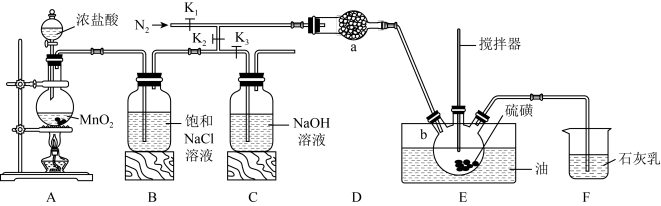
(1)a中所装试剂为_______。(填序号)
(2)仪器b的名称为_______ 。
(3)实验前向装置中通入N2的目的是_______ 。
(二)某研究性学习小组利用草酸溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验设计如下:(假设溶液混合时体积可以加和)
(4)写出草酸与酸性KMnO4溶液反应的离子方程式:_______ 。
(5)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a=_______ ,T=_______ 。若t1<8 s,可以得出的结论是:_______ 。
(6)通过比较实验②、③的结果,可以探究_______ 变化对化学反应速率的影响。

(1)a中所装试剂为_______。(填序号)
| A.无水CuSO4 | B.无水CaCl2 | C.碱石灰 | D.P2O5 |
(3)实验前向装置中通入N2的目的是
(二)某研究性学习小组利用草酸溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验设计如下:(假设溶液混合时体积可以加和)
| 实验序号 | 实验温度(K) | 酸性KMnO4溶液 | 草酸溶液 | 去离子水 | 溶液褪色时间 | ||
| c(mol/L) | V(mL) | c(mol/L) | V(mL) | V(mL) | t(s) | ||
| ① | 298 | 0.02 | 2.0 | 0.10 | 4.0 | 0 | t1 |
| ② | T | 0.02 | 2.0 | 0.10 | 3.0 | a | 8.0 |
| ③ | 343 | 0.02 | 2.0 | 0.10 | 3.0 | a | t2 |
| ④ | 373 | 0.02 | 2.0 | 0.10 | 3.0 | a | t3 |
(5)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a=
(6)通过比较实验②、③的结果,可以探究
您最近一年使用:0次
6 . 氯碱工厂按下面的流程生产:

(1)电解饱和食盐水的化学方程式是_______ ,氯气在_______ 极产生,检验氯气的方法是_______ 。若产生了71g氯气,则阴极产生气体的物质的量为_______ ,同时生成的氢氧化钠的质量为_______ 。
(2)该流程中合成氯化氢的化学方程式为_______ ,燃烧时火焰呈_______ 色。生成的氯化氢溶于水即得盐酸,写出氯化氢的电离方程式_______ 。
某化学兴趣小组欲用下图装置制备氯水并探究其性质。
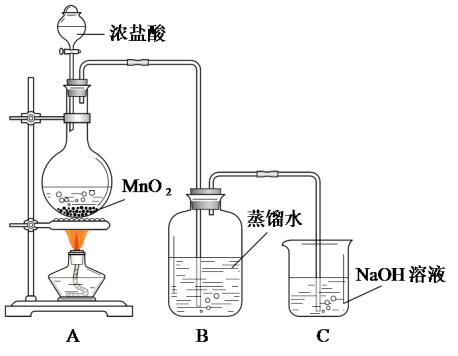
(3)烧瓶内发生的化学反应是_______ (书写化学方程式)。
(4)C装置的作用是_______ ,其中发生的化学反应是_______ (书写化学方程式)。
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:_______ ;化学性质变化:_______ 。
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
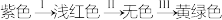
导致变色的微粒I、II、III依次为_______。
(7)某同学从B中取出少量样品,滴在NaHCO3粉末上,有无色气泡产生,由此他认为氯气与水反应产生了酸性强于碳酸的物质。请评价他的观点是否正确并说明理由_______ 。

(1)电解饱和食盐水的化学方程式是
(2)该流程中合成氯化氢的化学方程式为
某化学兴趣小组欲用下图装置制备氯水并探究其性质。

(3)烧瓶内发生的化学反应是
(4)C装置的作用是
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
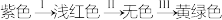
导致变色的微粒I、II、III依次为_______。
| A.H+、HClO、Cl2 | B.H+、ClO-、Cl- | C.HCl、ClO-、Cl- | D.HCl、HClO、Cl2 |
您最近一年使用:0次
名校
解题方法
7 . 二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶的低温硫化剂和粘接剂。
S2Cl2具有下列性质:
实验室可利用硫与少量氯气在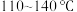 反应制得S2Cl2粗品。
反应制得S2Cl2粗品。

(1)仪器m的名称为_______ ;符合A装置制取氯气的溶液n可以为_______ 溶液。
(2)请补充完整实验装置连接顺序:A→_______→_______→_______→E→D,______ (填写装置标号),其中装置E的作用是_______ ,D装置的作用是_______ 。
(3)实验过程中,实验前和停止加热后,都需通一段时间的氮气,若停止加热后没有继续通入氮气,则S2Cl2的产率将_______ (填“偏高”、“偏低”或“无影响”)。
(4)实验中为了提高S2Cl2的纯度,实验的关键是保持干燥环境,_______ 和_______ 。
(5)S2Cl2遇水强烈反应会产生两种气体和一种沉淀,请写出该反应的化学方程式_______ 。
S2Cl2具有下列性质:
| 物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
| 剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
| 化学性质 | ①300℃以上完全分解 ②氯气过量发生反应: 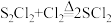 ③受热或遇水分解放热,放出腐蚀性烟气 | ||||
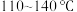 反应制得S2Cl2粗品。
反应制得S2Cl2粗品。
(1)仪器m的名称为
(2)请补充完整实验装置连接顺序:A→_______→_______→_______→E→D,
(3)实验过程中,实验前和停止加热后,都需通一段时间的氮气,若停止加热后没有继续通入氮气,则S2Cl2的产率将
(4)实验中为了提高S2Cl2的纯度,实验的关键是保持干燥环境,
(5)S2Cl2遇水强烈反应会产生两种气体和一种沉淀,请写出该反应的化学方程式
您最近一年使用:0次
2022-07-11更新
|
416次组卷
|
2卷引用:重庆市第一中学校2021-2022学年高一下学期期末考试化学试题
21-22高一·全国·假期作业
解题方法
8 . 现有X、Y、Z三种元素,已知有如下情况:①X、Y、Z的单质在常温下均为气体。②X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。③XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。⑤Z的单质溶于X2Y中,所得溶液具有漂白作用。请完成下列问题:
(1)写出XZ和X2Y的化学式:XZ_______ ;X2Y_______ 。
(2)写出X的单质在Z的单质中燃烧的化学方程式_______ 。
(3)Z的单质能否与氢氧化钠溶液发生反应:_______ (填“能”或“否”),若能,请写出反应的化学方程式:_______ 。(若不能反应,则此空不必填写)。
(1)写出XZ和X2Y的化学式:XZ
(2)写出X的单质在Z的单质中燃烧的化学方程式
(3)Z的单质能否与氢氧化钠溶液发生反应:
您最近一年使用:0次
名校
9 . 已知A、B、C、D、E为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,甲、乙、丙为非金属单质,丁为地壳中含量最多的金属元素所组成的单质,C的焰色反应呈黄色,丙是黄绿色气体,它们之间的转化关系如图所示(有的反应部分反应物或产物已经略去):
已知:NaAlO2+HCl+H2O=NaCl+A1(OH)3↓
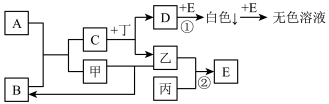
(1)物质A的化学式是________ ,D(填属于或不属于)_______ 电解质;
(2)反应①的离子方程式_______ ;
(3)若反应②的条件是点燃,则其反应现象是________ ;
(4)写出C与丁反应的离子方程式:_________ ;
(5)写出C与丙反应的离子方程式:________ 。
已知:NaAlO2+HCl+H2O=NaCl+A1(OH)3↓

(1)物质A的化学式是
(2)反应①的离子方程式
(3)若反应②的条件是点燃,则其反应现象是
(4)写出C与丁反应的离子方程式:
(5)写出C与丙反应的离子方程式:
您最近一年使用:0次
解题方法
10 . 现有常见金属单质A、F、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________ ;B___________ ;F___________ ;丙___________ 。
(2)写出下列反应离子方程式:
反应⑤:___________ 。
反应⑥:___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应离子方程式:
反应⑤:
反应⑥:
您最近一年使用:0次



