1 . 某小组设计如图装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应得到固体物质的成分。
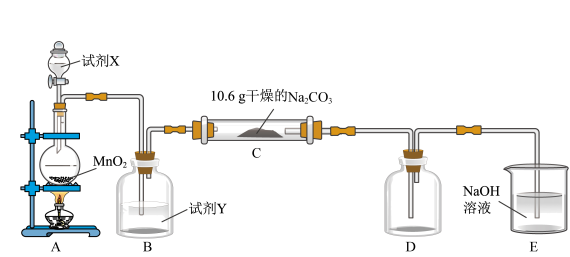
(1)试剂X的化学式________ 。A中制取Cl2的离子方程式____________________ 。
(2)试剂Y的名称为______________ 。
(3)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中除含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和____________________________ ;
假设2:存在三种成分:NaHCO3和__________________________ 。
②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
(4)已知Cl2O与水反应生成次氯酸,则D中Cl2O进入E反应的化学方程式为____________ 。

(1)试剂X的化学式
(2)试剂Y的名称为
(3)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中除含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和
假设2:存在三种成分:NaHCO3和
②设计方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中 | |
| 步骤2:向A试管中滴加BaCl2溶液 | |
| 步骤3: |
您最近一年使用:0次
2020-01-19更新
|
182次组卷
|
9卷引用:2014届广东省惠州市高三第二次调研考试理综化学试卷
(已下线)2014届广东省惠州市高三第二次调研考试理综化学试卷云南省盈江县民族完全中学2019-2020学年高一上学期期末考试化学试题贵州省麻江县第一中学2019-2020学年高一上学期期末考试化学试题云南省红河县第一中学2019-2020学年高一上学期期末考试化学试题云南省镇雄县民族中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区崇左市宁明中学2019-2020学年高一上学期期末考试化学试题(已下线)2.2.2 氯气的实验室制法 氯离子的检验(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)云南省文山州一中2021-2022学年高一下学期3月份考试化学试题云南省玉溪第三中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
2 . 18世纪70年代,瑞典化学家舍勒将软锰矿与浓盐酸混合加热,制得了黄绿色、有刺激性气味的氯气。氯气可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。某研究性学习小组的同学们模拟科学家的研究过程进行了如下实验,制备收集纯净干燥的氯气。

回答下列问题:
(1)仪器a的名称为___________ ,写出装置甲中发生反应的化学方程式___________ ,该反应中,氧化剂和还原剂的物质的量之比为___________ 。
(2)装置乙中的试剂为___________ ,可除去 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是__________ 。
(3)作为气体收集的装置图丁,最合适的是___________ (填标号)。

(4)装置戊中反应的离子方程式为___________ ,这样可以吸收多余的氯气,防止污染空气。

回答下列问题:
(1)仪器a的名称为
(2)装置乙中的试剂为
 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是(3)作为气体收集的装置图丁,最合适的是

(4)装置戊中反应的离子方程式为
您最近一年使用:0次
2023-11-29更新
|
77次组卷
|
2卷引用:广东省揭阳市揭东区2023-2024学年高一上学期期中考试化学试题
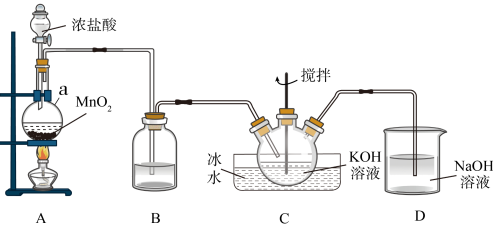
3 . 高铁酸钾(K2FeO4)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,可用于饮用水处理。实验室中可通过如图方法制备K2FeO4。
回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为________ ;装置B中试剂的名称是________ ;装置B的作用是___ 。
(2)装置C中Cl2与KOH反应的离子方程式为____________ 。
(3)若无装置D,可能产生的危害是_______ 。
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为______ 。

回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为
(2)装置C中Cl2与KOH反应的离子方程式为
(3)若无装置D,可能产生的危害是
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为
您最近一年使用:0次
名校
4 . 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
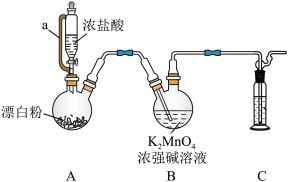
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 下列说法中错误的是
下列说法中错误的是

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
 下列说法中错误的是
下列说法中错误的是A.装置A中制备Cl2的化学方程式为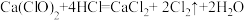 |
| B.装置A中a的作用是平衡压强,使液体顺利滴下 |
| C.在装置A、B之间加装盛有饱和食盐水的洗气瓶,可以提高高锰酸钾的产率 |
| D.装置C中可盛放澄清石灰水,吸收未反应的氯气 |
您最近一年使用:0次
2023-01-14更新
|
220次组卷
|
2卷引用:山东省济南市历城第二中学2022-2023学年高一上学期期末考试化学试题
22-23高一上·全国·课时练习
名校
解题方法
5 . 已知无水FeCl3在空气中遇水易潮解,加热易升华。实验室利用如图所示实验装置制取无水FeCl3。

已知:装置A是制备Cl2,发生反应的化学方程式为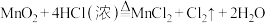 ;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
(1)装置C中的Y是浓硫酸,其作用是_______ 。
(2)装置D发生反应的化学方程式为_______ 。
(3)实验结束时,应先熄灭_______ (慎“A”或“D”)处酒精灯;E中冷水的作用是_______ 。
(4)装置F的作用是_______ 。
(5)图中的实验设计还存在不足,在图中方框内绘制应该补充的装置_______ ,并写出对应的化学方程式_______ 。

已知:装置A是制备Cl2,发生反应的化学方程式为
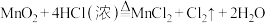 ;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。(1)装置C中的Y是浓硫酸,其作用是
(2)装置D发生反应的化学方程式为
(3)实验结束时,应先熄灭
(4)装置F的作用是
(5)图中的实验设计还存在不足,在图中方框内绘制应该补充的装置
您最近一年使用:0次
2022-10-25更新
|
270次组卷
|
5卷引用:2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)山东省青岛第十七中学2022-2023学年高一上学期10月月考化学试题山东省枣庄市第八中学南校2022-2023学年高一11月疫情返校测试(彩虹班)化学试题山东省枣庄市第八中学南校2022-2023学年高一11月疫情返校测试(2-18班)化学试题山东省东营市胜利第一中学2023-2024学年高一上学期10月考练化学试题
22-23高一·全国·单元测试
6 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是____ ,a中的试剂为_____ 。
(2)b中采用的加热方式是____ ,c中化学反应的离子方程式是____ ,采用冰水浴冷却的目的是_____ 。
(3)d的作用是____ ,可选用试剂____ (填字母)。
A.HCl B.NaCl C.Ca(OH)2 D.H2SO4
(4)反应结束后,取出b中试管,经冷却结晶,_____ ,_____ ,干燥,得到KClO3晶体。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)b中采用的加热方式是
(3)d的作用是
A.HCl B.NaCl C.Ca(OH)2 D.H2SO4
(4)反应结束后,取出b中试管,经冷却结晶,
您最近一年使用:0次
2022高一·上海·专题练习
名校
解题方法
7 . 已知KMnO4与浓HCl在常温下反应能产生Cl2。若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是(不考虑①单元装置)


| A.只有④处 | B.只有②处 | C.只有②和③处 | D.②③④处 |
您最近一年使用:0次
2022-07-22更新
|
932次组卷
|
4卷引用:第1章基础巩固测评卷-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)(已下线)第二章《 海水中的重要元素----钠和氯》基础过关单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)河北省邢台市第二中学2022-2023学年高一上学期期末考试化学试题(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)
解题方法
8 . 某化学小组用“84消毒液”(主要成分是NaClO)制备氯气并探究其性质,进行如图所示的实验(a~d中均为浸有相应试液的棉花,夹持装置省略)。下列说法正确的是
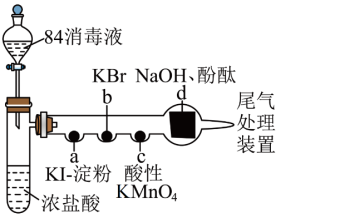

| A.为防止尾气污染空气,应使用饱和食盐水吸收尾气 |
| B.d处褪色,一定是因酚酞被氧化而引起 |
| C.c处褪色,说明Cl2具有还原性 |
| D.a处变为蓝色,b处变为橙色,说明Cl2具有氧化性 |
您最近一年使用:0次
名校
9 .  是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。
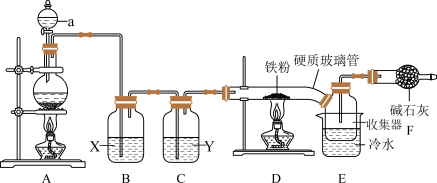
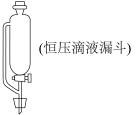
回答下列问题:
(1)A中发生的化学反应方程式是___________ 。为使实验顺利进行,可将仪器a更换为恒压滴液漏斗(如上图),更换后优点是___________ 。
(2)试剂“X”是___________ ,其作用是___________ 。
(3)硬质玻璃管直接连接收集器的优点___________ 。
(4)实验开始时,应先点燃A处酒精灯,当___________ 时,再点燃D处酒精灯。
(5)装置F作用是吸收多余氯气和___________ ,氯气和碱石灰反应时,若有0.71g氯气被氧化成次氯酸盐,1.42g氯气被氧化成氯酸盐,则被还原的氯原子的物质的量为___________ 。
 是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。
是实验室中一种常见的化学试剂,也是生产生活中常用的净水剂。 熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备
熔点为306℃,沸点为315℃,易吸收空气中的水分而潮解。巴中中学某化学兴趣设计以下装置,制备 。
。

回答下列问题:
(1)A中发生的化学反应方程式是
(2)试剂“X”是
(3)硬质玻璃管直接连接收集器的优点
(4)实验开始时,应先点燃A处酒精灯,当
(5)装置F作用是吸收多余氯气和
您最近一年使用:0次
名校
10 . 氯气( )是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等,例如日常生活用品84消毒液.84消毒液是常用消毒剂,某化学兴趣小组在实验室利用氯气制备84消毒液,请回答下列问题:
)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等,例如日常生活用品84消毒液.84消毒液是常用消毒剂,某化学兴趣小组在实验室利用氯气制备84消毒液,请回答下列问题:
Ⅰ.实验室制备84消毒液.

(1)装置甲中盛放高锰酸钾的仪器名称是______ ,装置甲中反应的离子方程式为______ .
(2)装置乙的作用是______ .
(3)装置丙中制备次氯酸钠为放热反应,该反应需要控制温度在40℃以下,写出一种(除搅拌外)控制该反应温度的操作方法______ .
Ⅱ.氯气的应用
(4)可用 和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是
和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是______ .(填化学式)
(5)向KI溶液滴加过量氯水会生成 ,发生反应的离子方程式如下,请补全产物,并将离子方程式配平:
,发生反应的离子方程式如下,请补全产物,并将离子方程式配平:_________

(6) 是次氯酸的酸酐,其制备方法之一是将
是次氯酸的酸酐,其制备方法之一是将 通入HgO中即可制得,同时生成
通入HgO中即可制得,同时生成 .请写出对应的化学方程式并用双线桥表示电子的转移:
.请写出对应的化学方程式并用双线桥表示电子的转移:______ .
 )是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等,例如日常生活用品84消毒液.84消毒液是常用消毒剂,某化学兴趣小组在实验室利用氯气制备84消毒液,请回答下列问题:
)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等,例如日常生活用品84消毒液.84消毒液是常用消毒剂,某化学兴趣小组在实验室利用氯气制备84消毒液,请回答下列问题:Ⅰ.实验室制备84消毒液.

(1)装置甲中盛放高锰酸钾的仪器名称是
(2)装置乙的作用是
(3)装置丙中制备次氯酸钠为放热反应,该反应需要控制温度在40℃以下,写出一种(除搅拌外)控制该反应温度的操作方法
Ⅱ.氯气的应用
(4)可用
 和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是
和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是(5)向KI溶液滴加过量氯水会生成
 ,发生反应的离子方程式如下,请补全产物,并将离子方程式配平:
,发生反应的离子方程式如下,请补全产物,并将离子方程式配平:
(6)
 是次氯酸的酸酐,其制备方法之一是将
是次氯酸的酸酐,其制备方法之一是将 通入HgO中即可制得,同时生成
通入HgO中即可制得,同时生成 .请写出对应的化学方程式并用双线桥表示电子的转移:
.请写出对应的化学方程式并用双线桥表示电子的转移:
您最近一年使用:0次
2023-12-04更新
|
78次组卷
|
3卷引用:湖北省宜昌市三峡高级中学2023-2024学年高一上学期10月月考化学试题



