1 . 人类对氯的认识经历了漫长的过程。回答下列问题:
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是___________ 。
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。___________ ,装置接口的连接顺序是a→______→______→______→______→f。___________
②装置乙中的试剂Y是___________ 。
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”);打开开关K,观察到干燥有色布条___________ (填“褪色”或“不褪色”),证明氯气没有漂白性,但氯气与水反应的产物___________ 具有漂白性。
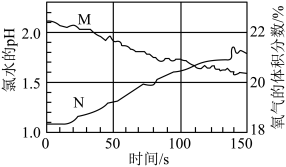
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是___________ (填“M”或“N”),据此分析,此时广口瓶中发生反应的化学方程式是___________ 。___________ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,首次制得Cl2,该反应的离子方程式是
(2)1785年,贝托雷最早利用氯气的水溶液做漂白剂,可以永久性地漂白纸张和鲜花,且在阳光下能够分解产生氧气。某实验小组利用如下实验装置探究氯气是否具有漂白性。

②装置乙中的试剂Y是
③实验开始后,关闭装置乙中的开关K,观察到干燥有色布条
④实验小组利用数字传感器测定广口瓶中的氯水在光照条件下的pH和瓶中氧气的体积分数变化曲线如下图所示,其中表示氯水的pH变化的曲线是
您最近一年使用:0次
2024-01-24更新
|
45次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一上学期期末考试化学模拟试题(一)
名校
2 . 二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入Cl2产生高浓度NaClO溶液,然后与氰尿酸(C3H3N3O3)反应制取二氯异氰尿酸钠:2NaClO+C3H3N3O3=NaC3N3O3Cl2+NaOH+H2O。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为______ (填小写字母)。
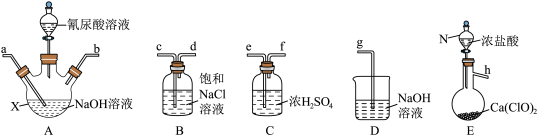
(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为_________ 。
(3)装置A中制备NaClO溶液完成的现象是___________ ,在加氰尿酸溶液过程仍需不断通入Cl2的理由是___________ 。
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为: +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要___________ 。
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品________ 。( 该样品的有效氯  )(写出计算过程)
)(写出计算过程)
③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值______ (填“偏高”或“偏低”)。
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目________ 。___K2FeO4+____H2O=___Fe(OH)3胶体+____O2↑+____KOH,被还原的元素是___________ 。
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:_________ 。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为

(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为
(3)装置A中制备NaClO溶液完成的现象是
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为:
 +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品
 )(写出计算过程)
)(写出计算过程)③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:
您最近一年使用:0次
3 . 有关氯气制备的装置如图所示,下列有关说法不正确的是


| A.图中气体通入浓硫酸时导管连接错误,应该是长管进气,短管出气 |
| B.可用饱和碳酸氢钠溶液代替饱和NaCl溶液 |
| C.制备氯气时,二氧化锰做氧化剂 |
| D.图中采用了向上排空气法收集氯气 |
您最近一年使用:0次
2022-09-19更新
|
1028次组卷
|
6卷引用:安徽省宿州北方中学2021-2022学年高一上学期期中考试化学试题
安徽省宿州北方中学2021-2022学年高一上学期期中考试化学试题(已下线)海水中的重要元素—钠和氯——进阶学习上海市金山中学2022-2023学年高一上学期期中考试化学试题新疆昌吉州行知学校2022-2023学年高一上学期第一次线上月考化学试题河南省开封市新世纪高级中学2022-2023学年高一上学期期末考试化学试题(已下线)【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册
名校
4 . 实验室模拟工业制备 的装置如图所示。
的装置如图所示。

原理: ;
; 与碱可发生反应:
与碱可发生反应: 。
。
下列有关叙述错误的是
 的装置如图所示。
的装置如图所示。
原理:
 ;
; 与碱可发生反应:
与碱可发生反应: 。
。下列有关叙述错误的是
A.装置甲的作用是除去 中的 中的 杂质 杂质 |
B.应先往装置乙中滴加 溶液,再通入气体 溶液,再通入气体 |
C. 在制备原理中是氧化剂 在制备原理中是氧化剂 |
| D.装置丙中会发生倒吸 |
您最近一年使用:0次
2022-08-17更新
|
366次组卷
|
3卷引用:第二章 海水中的重要元素——钠和氯 ★综合拔高练
第二章 海水中的重要元素——钠和氯 ★综合拔高练新疆第二师八一中学2022-2023学年高三上学期第一次月考化学试题 (已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(选择题6-10)
名校
解题方法
5 . 18世纪70年代,瑞典化学家舍勒将软锰矿与浓盐酸混合加热,制得了黄绿色、有刺激性气味的氯气。氯气可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。某研究性学习小组的同学们模拟科学家的研究过程进行了如下实验,制备收集纯净干燥的氯气。

回答下列问题:
(1)仪器a的名称为___________ ,写出装置甲中发生反应的化学方程式___________ ,该反应中,氧化剂和还原剂的物质的量之比为___________ 。
(2)装置乙中的试剂为___________ ,可除去 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是__________ 。
(3)作为气体收集的装置图丁,最合适的是___________ (填标号)。

(4)装置戊中反应的离子方程式为___________ ,这样可以吸收多余的氯气,防止污染空气。

回答下列问题:
(1)仪器a的名称为
(2)装置乙中的试剂为
 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是(3)作为气体收集的装置图丁,最合适的是

(4)装置戊中反应的离子方程式为
您最近一年使用:0次
2023-11-29更新
|
77次组卷
|
2卷引用:广东省揭阳市揭东区2023-2024学年高一上学期期中考试化学试题
22-23高二上·全国·课时练习
6 . 电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2_____ (填“>”“=”或“<”)2L,原因是_____ 。装置改进后,可用于制备NaOH溶液,若测定NaOH溶液的浓度,常用的方法为_____ 。


您最近一年使用:0次
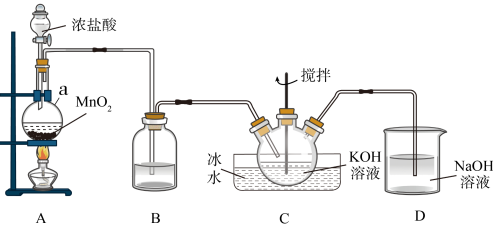
7 . 高铁酸钾(K2FeO4)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,可用于饮用水处理。实验室中可通过如图方法制备K2FeO4。
回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为________ ;装置B中试剂的名称是________ ;装置B的作用是___ 。
(2)装置C中Cl2与KOH反应的离子方程式为____________ 。
(3)若无装置D,可能产生的危害是_______ 。
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为______ 。

回答下列问题:
Ⅰ.制备KClO:
(1)仪器a的名称为
(2)装置C中Cl2与KOH反应的离子方程式为
(3)若无装置D,可能产生的危害是
Ⅱ.制备K2FeO4:
(4)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25°C,充分反应得到含有KCl和KNO3的紫色溶液,反应的离子方程式为
您最近一年使用:0次
名校
8 .  是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
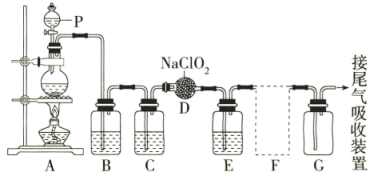
(1)仪器P的名称是________ 。
(2)请写出装置A中烧瓶内发生反应的化学方程式:__________ 。
(3)装置B、C中所盛试剂分别是________ 、__________ 。
(4)F为 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集_______ (填序号),其中与装置E导管相连的导管口是______ (填接口字母)。
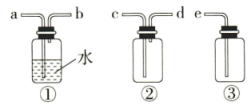
(5)装置D中发生反应的化学方程式为________ 。
(6) 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应:________ 。将 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为_______ (填“酸性氧化物”或“碱性氧化物”)。
 是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用
是一种广谱型消毒剂,它易溶于水而难溶于有机溶剂。实验室用 与
与 反应制得
反应制得 和
和 。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的
。如图是实验室用于制备氯气并用氯气制备和收集一定量纯净的 的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去
的装置(某些夹持装置等省略)。其中E中盛有液体(用于除去 中的未反应的
中的未反应的 ,氯气几乎不溶于饱和食盐水)。
,氯气几乎不溶于饱和食盐水)。
(1)仪器P的名称是
(2)请写出装置A中烧瓶内发生反应的化学方程式:
(3)装置B、C中所盛试剂分别是
(4)F为
 收集装置,应选用下图的哪组装置来收集
收集装置,应选用下图的哪组装置来收集
(5)装置D中发生反应的化学方程式为
(6)
 与
与 反应可以得到以
反应可以得到以 为有效成分的漂白液,请用离子方程式表示该反应:
为有效成分的漂白液,请用离子方程式表示该反应: 通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中
通入冷的石灰乳中即制得漂白粉,漂白粉在使用时会与空气中 反应,
反应, 为
为
您最近一年使用:0次
2022-08-17更新
|
290次组卷
|
2卷引用:第二节 氯及其化合物 第2课时 氯气的实验室制法及氯离子的检验
名校
9 . 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
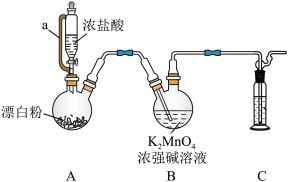
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 下列说法中错误的是
下列说法中错误的是

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
 下列说法中错误的是
下列说法中错误的是A.装置A中制备Cl2的化学方程式为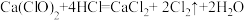 |
| B.装置A中a的作用是平衡压强,使液体顺利滴下 |
| C.在装置A、B之间加装盛有饱和食盐水的洗气瓶,可以提高高锰酸钾的产率 |
| D.装置C中可盛放澄清石灰水,吸收未反应的氯气 |
您最近一年使用:0次
2023-01-14更新
|
220次组卷
|
2卷引用:山东省济南市历城第二中学2022-2023学年高一上学期期末考试化学试题
22-23高一上·全国·课时练习
名校
解题方法
10 . 已知无水FeCl3在空气中遇水易潮解,加热易升华。实验室利用如图所示实验装置制取无水FeCl3。

已知:装置A是制备Cl2,发生反应的化学方程式为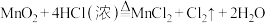 ;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
(1)装置C中的Y是浓硫酸,其作用是_______ 。
(2)装置D发生反应的化学方程式为_______ 。
(3)实验结束时,应先熄灭_______ (慎“A”或“D”)处酒精灯;E中冷水的作用是_______ 。
(4)装置F的作用是_______ 。
(5)图中的实验设计还存在不足,在图中方框内绘制应该补充的装置_______ ,并写出对应的化学方程式_______ 。

已知:装置A是制备Cl2,发生反应的化学方程式为
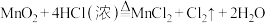 ;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。
;溶液X是饱和食盐水(饱和NaCl溶液),目的是除去Cl2中混有的HCl气体。(1)装置C中的Y是浓硫酸,其作用是
(2)装置D发生反应的化学方程式为
(3)实验结束时,应先熄灭
(4)装置F的作用是
(5)图中的实验设计还存在不足,在图中方框内绘制应该补充的装置
您最近一年使用:0次
2022-10-25更新
|
270次组卷
|
5卷引用:2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)山东省青岛第十七中学2022-2023学年高一上学期10月月考化学试题山东省枣庄市第八中学南校2022-2023学年高一11月疫情返校测试(彩虹班)化学试题山东省枣庄市第八中学南校2022-2023学年高一11月疫情返校测试(2-18班)化学试题山东省东营市胜利第一中学2023-2024学年高一上学期10月考练化学试题



