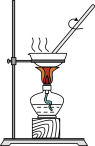
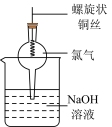
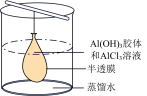
1 . 下图表示在没有通风橱的条件下制备氯气时设计的装置, 图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)

⑴仪器A的名称是____________________ ;水槽中应盛放的是____________________ ;
烧杯中盛放的是______________________ ;烧瓶中反应的化学方程式________________ ;
⑵在收集氯气时,应打开________ ,关闭_________ 。当氯气收集完毕时打开_________ ,关闭___ 。(填a,b)
⑶ 若要制得标准状况下的Cl2 0.672L,理论上需要MnO2的物质的量是__________ ?

⑴仪器A的名称是
烧杯中盛放的是
⑵在收集氯气时,应打开
⑶ 若要制得标准状况下的Cl2 0.672L,理论上需要MnO2的物质的量是
您最近一年使用:0次
2 . 某化学兴趣小组的同学利用下图所示实验装置进行NH3、Cl2的制备、性质等实验(图中夹持装置有省略)。请按要求填空。

供选择的装置:

(1)装置A除可制备NH3外,还可制备其他多种气体,写出制备其中一种气体的化学方程式__________________ 。
(2)为制取干燥氨气,可将装置A与装置________ (填编号,从供选择的装置中选取)连接;装置A中的烧瓶内固体宜选用__________ (选填以下选项的代号)。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(3)若欲制取纯净、干燥的氯气,可从I、II、III装置中选取合适的装置与C依次相连,则连接次序为C、_______ (填编号);
(4)B为探究氯气与氨气反应的装置。实验时先向B通入氨气,然后关闭c活塞,再向B通入氯气。
①实验中装置B的烧瓶内出现浓厚的白烟并在容器内壁凝结,试推测发生反应的化学方程式___________ ,请设计一个实验方案鉴定该固体中的阳离子_________ ;
②实验完毕后观察到B烧瓶内还有黄绿色气体,简述如何处理才能不污染环境________ 。

供选择的装置:

(1)装置A除可制备NH3外,还可制备其他多种气体,写出制备其中一种气体的化学方程式
(2)为制取干燥氨气,可将装置A与装置
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(3)若欲制取纯净、干燥的氯气,可从I、II、III装置中选取合适的装置与C依次相连,则连接次序为C、
(4)B为探究氯气与氨气反应的装置。实验时先向B通入氨气,然后关闭c活塞,再向B通入氯气。
①实验中装置B的烧瓶内出现浓厚的白烟并在容器内壁凝结,试推测发生反应的化学方程式
②实验完毕后观察到B烧瓶内还有黄绿色气体,简述如何处理才能不污染环境
您最近一年使用:0次
3 . 某学生利用以下装置探究氯气与氨气之间的反应。其中C为纯净干燥的氯气与氨气反应的装置。
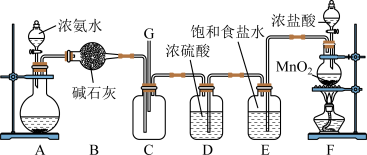
请回答下列问题:
(1)装置A中的烧瓶内固体不能选用___________
(2)装置A中发生反应的化学方程式为___________
(3)B装置的作用___________ ;E装置的作用___________
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一、写出反应的化学方程式:___________
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,需要处理,___________ ,写出离子方程式___________
(6)实验室制备氨气,下列方法中适宜选用的是___________ 。
①固态氯化铵加热分解 ②浓氨水中加入固体氢氧化钠
③加热浓氨水 ④固态氯化铵与氢氧化钙混合加热

请回答下列问题:
(1)装置A中的烧瓶内固体不能选用___________
| A.生石灰 | B.碱石灰 | C.五氧化二磷 | D.烧碱 |
(3)B装置的作用
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一、写出反应的化学方程式:
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,需要处理,
(6)实验室制备氨气,下列方法中适宜选用的是
①固态氯化铵加热分解 ②浓氨水中加入固体氢氧化钠
③加热浓氨水 ④固态氯化铵与氢氧化钙混合加热
您最近一年使用:0次
名校
解题方法
4 . 已知无水AlCl3遇潮湿空气即产生大量白雾,实验室可用如图所示装置制备AlCl3.

(1)装置A中发生反应的化学方程式为________________________________________ .
(2)装置B盛放的试剂是______ ,其作用是_______________________________ ;装置C盛放的试剂是______ ,其作用是____________________________________ .
(3)装置G的作用是________________ ,G中发生反应的化学方程式是_______ .
(4)F中盛放的试剂是______ ,其作用是___________________________________ .

(1)装置A中发生反应的化学方程式为
(2)装置B盛放的试剂是
(3)装置G的作用是
(4)F中盛放的试剂是
您最近一年使用:0次
5 . 高铁酸钾是环保型水处理剂,制备原理如下:

(1)从环保角度考虑,“酸溶”发生的反应中,氧化产物和还原产物的物质的量之比为_______ 。吸收尾气的试剂可能是________ 。
(2)洗涤产品常用75%酒精作洗涤液,不用蒸馏水,其目的是___________ 。
(3)写出“氧化”中化学方程式_______________ 。
(4)已知3KC1O KClO3+2KC1,下列是制备次氧酸钾的装置:
KClO3+2KC1,下列是制备次氧酸钾的装置:
①B装置中试剂可能是_________ (填代号)。
a.饱和碳酸氢钠溶液 b.饱和食盐水 c.浓硫酸 d.稀硫酸
②C装置的水槽中盛装________ (填“热水”或“冰水”)。
(5)为了测定高铁酸钾产品纯度,进行如下实验:5.0000 g K2FeO4样品溶于稀硫酸中,充分反应后,配制成250 mL溶液。准确量取25.00 mL溶液于锥形瓶中,加足量的KI溶液,并滴加指示剂,用0.1000 mol/LNa2S2O3标准溶液滴定至终点消耗Na2S2O3溶液20.00 mL。
已知有关反应:4FeO42-+20 H+=4Fe3++3O2↑+10H2O ,2S2O32-+I2=2I-+S4O62-。
①如果配制的溶液中含少量K2FeO4,会使测得结果_______ (填“偏高”、“偏低”或“无影响”)。
②进行上述实验需要定量仪器有电子天平、滴定管、量筒和________ 。
③该高铁酸钾产品纯度为_______________ 。

(1)从环保角度考虑,“酸溶”发生的反应中,氧化产物和还原产物的物质的量之比为
(2)洗涤产品常用75%酒精作洗涤液,不用蒸馏水,其目的是
(3)写出“氧化”中化学方程式
(4)已知3KC1O
 KClO3+2KC1,下列是制备次氧酸钾的装置:
KClO3+2KC1,下列是制备次氧酸钾的装置:
①B装置中试剂可能是
a.饱和碳酸氢钠溶液 b.饱和食盐水 c.浓硫酸 d.稀硫酸
②C装置的水槽中盛装
(5)为了测定高铁酸钾产品纯度,进行如下实验:5.0000 g K2FeO4样品溶于稀硫酸中,充分反应后,配制成250 mL溶液。准确量取25.00 mL溶液于锥形瓶中,加足量的KI溶液,并滴加指示剂,用0.1000 mol/LNa2S2O3标准溶液滴定至终点消耗Na2S2O3溶液20.00 mL。
已知有关反应:4FeO42-+20 H+=4Fe3++3O2↑+10H2O ,2S2O32-+I2=2I-+S4O62-。
①如果配制的溶液中含少量K2FeO4,会使测得结果
②进行上述实验需要定量仪器有电子天平、滴定管、量筒和
③该高铁酸钾产品纯度为
您最近一年使用:0次
11-12高一上·浙江绍兴·期中
6 . 下图表示在没有通风橱的条件下制备氯气时的装置,图中a、b是可控制的弹簧铁夹。(已知:氯气在饱和氯化钠溶液中的溶解度较小。)

(1)仪器A的名称是_________________ ;烧杯中盛放的是___________________ ;烧瓶中发生的反应化学方程式为__________________________ ;
(2)在收集氯气时,应______________________ 。(填:如何操作a、b止水夹,下同),当氯气收集完毕时应____________________ 。
(3)若制得标准状况下的Cl2为0.672L,则被氧化的HCl的物质的量是_________

(1)仪器A的名称是
(2)在收集氯气时,应
(3)若制得标准状况下的Cl2为0.672L,则被氧化的HCl的物质的量是
您最近一年使用:0次
7 . 现有短周期元素X形成的单质A与NaOH溶液反应,有如下转化关系: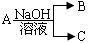 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。
(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为__________________ ,实验室制备A的化学方程式为______________________ ;
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为________________________ ;
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为______________ ;其最高氧化物与NaOH溶液反应的离子方程式为____________________ ;
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下:
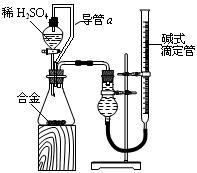
①装置中导管a的作用是_______________________ ;
②实验中准确测得4个数据:实验前该合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL;则通常状况时气体摩尔体积Vm=____________ L·moL-1。
 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下:

①装置中导管a的作用是
②实验中准确测得4个数据:实验前该合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL;则通常状况时气体摩尔体积Vm=
您最近一年使用:0次