名校
1 . I.海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、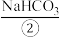 、
、 、
、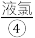 、
、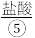 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出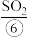 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼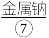 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同),既不属于电解质也不属于非电解质的是___________ 。
(2)写出③溶于水的电离方程式:___________ 。
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是___________ 。(填序号)
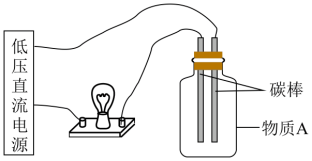
(4) 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于___________ (填“酸性氧化物”、“碱性氧化物”或“不成盐氧化物”)
Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
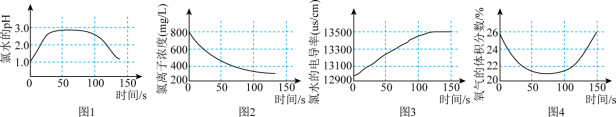
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。
(7)将氯气通入热的NaOH溶液中,反应得到NaCl, 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:___________ 。
 、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、
、MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水用以生产NaOH、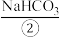 、
、 、
、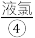 、
、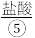 等,苦卤经过氯气氧化,热空气吹出
等,苦卤经过氯气氧化,热空气吹出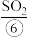 吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼
吸收等一系列操作可获得Br2.电解熔融氯化钠可冶炼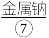 ;海底埋藏大量可燃冰
;海底埋藏大量可燃冰 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出③溶于水的电离方程式:
(3)在下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是

(4)
 能被水吸收制备次氯酸(HClO),从物质分类的角度看,
能被水吸收制备次氯酸(HClO),从物质分类的角度看, 属于
属于Ⅱ.海水中的有丰富的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(5)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
A. | B. | C.Mg2+ | D. |
(6)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能是其检测结果的是___________。

| A.图1表示氯水pH随时间的变化 |
| B.图2表示溶液中氯离子浓度随时间的变化 |
| C.图3表示氯水的电导率随时间的变化 |
| D.图4表示液面上方氧气体积分数随时间的变化 |
(7)将氯气通入热的NaOH溶液中,反应得到NaCl,
 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数之比为4∶1,写出该反应总的离子方程式:
的个数之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
名校
解题方法
2 . 氯及其合氯化合物
人体中钠的主要来源为食盐、酱油、腌制食品、烟熏食品、咸味食品等。氧化钠,也称苛性钠、烧藏、火马、是一种无机化合物,化学式为NaOH,用途非常广泛。烧碱是一种重要的化工原料,工业烧碱中可能含有少量NaCl。
(1)海水晒盐的原理是_____。
(2)电解饱和的食盐水,先要精制盐水,以除去 、Ca2+,可依次加入的溶液是_____。
、Ca2+,可依次加入的溶液是_____。
(3)电解饱和食盐水溶液,下列叙述中,正确的是_____。
(4)下列氯化物中,可以由金属和氯气反应得到的是_____。
(5)下列关于氯气和氯水的叙述正确的是_____。
(6)电解饱和食盐水的化学方程式:_____ 。
(7)工业上用_____ 和_____ (写化学式)作为原料来制取漂粉精,反应的化学方程式为_____ ,漂粉精长期在空气中,会使其失效,主要化学方程式_____ ;_____ ,故其应_____ 保存。
人体中钠的主要来源为食盐、酱油、腌制食品、烟熏食品、咸味食品等。氧化钠,也称苛性钠、烧藏、火马、是一种无机化合物,化学式为NaOH,用途非常广泛。烧碱是一种重要的化工原料,工业烧碱中可能含有少量NaCl。
(1)海水晒盐的原理是_____。
| A.利用热蒸发浓缩海水达到饱和并进一步结晶 |
| B.用过降温降低食盐的溶解度使食盐析出 |
| C.利用加入沉淀剂的方法使食盐沉淀析出 |
| D.利用泥沙使海水到达饱和,然后利用日光使海盐析出 |
 、Ca2+,可依次加入的溶液是_____。
、Ca2+,可依次加入的溶液是_____。| A.Na2CO3、BaCl2、NaOH、HCl |
| B.BaCl2、NaOH、Na2CO3、HCl |
| C.BaCl2、Na2CO3、HCl、NaOH |
| D.Na2CO3、BaCl2、HCl、NaOH |
| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.在阳极附近的溶液中滴入淀粉碘化钾溶液,溶液呈蓝色 |
| C.若在阴极收集气体,能使带火星的木条燃。 |
| D.在阴极的物质只有氢气 |
| A.CuCl | B.FeCl2 | C.FeCl3 | D.HCl |
| A.因氯气有强氧化性,所以氯气本身可用于杀菌、消毒、漂白 |
| B.氯水中起漂白用的是次氯酸 |
| C.氯水长期放置颜色无明显变化 |
| D.光照水有气泡冒出,该气体是氯气 |
(7)工业上用
您最近一年使用:0次
名校
解题方法
3 . 根据信息和要求书写相关反应的方程式
(1)用84消毒液对新冠病毒进行消杀。将 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式___________ 。
(2) 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:_____ 。

(3)以 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:___________ 。
(1)用84消毒液对新冠病毒进行消杀。将
 通入NaOH溶液制备84消毒液,写出反应的离子方程式
通入NaOH溶液制备84消毒液,写出反应的离子方程式(2)
 与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
与炭黑焙烧时所发生的物质转化如图所示,写出该反应的化学方程式:
(3)以
 为原料可在加热熔融条件下制取
为原料可在加热熔融条件下制取 。该反应中包含的所有物质有
。该反应中包含的所有物质有 、
、 、KCl、KOH、
、KCl、KOH、 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至沉淀完全,写出发生反应的离子方程式:
溶液至沉淀完全,写出发生反应的离子方程式:
您最近一年使用:0次
名校
4 . NaCl是一种化工原料,可以制备多种物质,如下图所示。
(1)写出反应①的离子方程式:___________ ,该反应中氧化产物与还原产物的质量比为___________ 。
(2)反应②可用于制取漂白粉,写出化学反应方程式并用双线桥法标出电子转移的方向和数目:___________ ;漂白粉需要密封保存,其原因是___________ (用化学方程式表示)
(3)反应③是侯氏制碱法的核心反应,写出化学反应方程式:___________ ;侯氏制碱法将___________ 和___________ 联合起来,也称联合制碱法。

(1)写出反应①的离子方程式:
(2)反应②可用于制取漂白粉,写出化学反应方程式并用双线桥法标出电子转移的方向和数目:
(3)反应③是侯氏制碱法的核心反应,写出化学反应方程式:
您最近一年使用:0次
2024-01-01更新
|
151次组卷
|
2卷引用:湖北省荆州中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
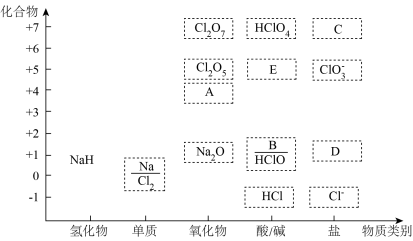
5 . 如图为钠和氯的价类二维图,请据图完成下列问题:___________ 价。可与水反应生成氢气,该反应中氧化产物和还原产物的质量比为___________ 。
(2)A是氯的氧化物,其化学式为___________ 。A可用于自来水消毒。其消毒效率是 的
的___________ 倍(还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。
(3)B属于碱,其水溶液与 反应生成D的离子方程式为
反应生成D的离子方程式为___________ 。
(4)C是高氯酸钠,受热分解可产生 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为___________ 。
(5) 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式___________ 。
(2)A是氯的氧化物,其化学式为
 的
的 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。(3)B属于碱,其水溶液与
 反应生成D的离子方程式为
反应生成D的离子方程式为(4)C是高氯酸钠,受热分解可产生
 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为(5)
 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
2023-12-26更新
|
215次组卷
|
3卷引用:山东省临沂第四中学2023-2024学年高一上学期期中检测化学试卷
山东省临沂第四中学2023-2024学年高一上学期期中检测化学试卷 (已下线)寒假作业05 氯及其化合物-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)山东省临沂市2023-2024学年高一上学期期中考试化学试题
名校
6 . 按要求完成下列题目。
(1)书写对应的化学方程式:
①用氯气制备漂白粉:___________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:___________ 。
③呼吸面具中过氧化钠与二氧化碳反应:___________ 。
④KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(2)书写对应的离子方程式:
⑤制作印刷电路板时氯化铁溶液腐蚀铜:___________ 。
⑥用高锰酸钾酸性溶液检验溶液中的亚铁离子(还原产物为Mn2+):___________ 。
⑦在酸性条件下,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为___________ 。
(1)书写对应的化学方程式:
①用氯气制备漂白粉:
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③呼吸面具中过氧化钠与二氧化碳反应:
④KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)书写对应的离子方程式:
⑤制作印刷电路板时氯化铁溶液腐蚀铜:
⑥用高锰酸钾酸性溶液检验溶液中的亚铁离子(还原产物为Mn2+):
⑦在酸性条件下,向含铬废水中加入FeSO4,可将
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
您最近一年使用:0次
名校
7 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:
①“84”消毒液:② (在水中一部分可以电离出阴、阳离子);③
(在水中一部分可以电离出阴、阳离子);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦过氧乙酸(
;⑤碘酒;⑥75%酒精;⑦过氧乙酸(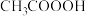 );⑧高铁酸钠(
);⑧高铁酸钠( )。
)。
回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号),“84”消毒液中有效成分的电离方程式为___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长池水变绿。一种可能的原因是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO___________  的(填“>”或“<”)。
的(填“>”或“<”)。
②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是___________ (用离子方程式表示)。
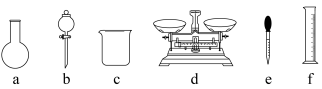
(3)某同学参阅“84”消毒液的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。若配制一定物质的量浓度的上述消毒液480mL,需要选用下图所示的哪些仪器___________ (填序号),除这些仪器以外还需要的玻璃仪器有___________ (填仪器名称)。 来杀菌、消毒,该小组同学欲检验自来水中是否有
来杀菌、消毒,该小组同学欲检验自来水中是否有 残留,需要用到的试剂为
残留,需要用到的试剂为___________ 。
①“84”消毒液:②
 (在水中一部分可以电离出阴、阳离子);③
(在水中一部分可以电离出阴、阳离子);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦过氧乙酸(
;⑤碘酒;⑥75%酒精;⑦过氧乙酸(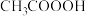 );⑧高铁酸钠(
);⑧高铁酸钠( )。
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长池水变绿。一种可能的原因是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO 的(填“>”或“<”)。
的(填“>”或“<”)。②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是
(3)某同学参阅“84”消毒液的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。若配制一定物质的量浓度的上述消毒液480mL,需要选用下图所示的哪些仪器
 来杀菌、消毒,该小组同学欲检验自来水中是否有
来杀菌、消毒,该小组同学欲检验自来水中是否有 残留,需要用到的试剂为
残留,需要用到的试剂为
您最近一年使用:0次
名校
8 . 新型冠状病毒肺炎疫情在全球多地爆发,“84消毒液”是大规模环境消毒剂。已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(2)该“84消毒液”的物质的量浓度约为__________  。(保留一位小数)
。(保留一位小数)
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。配制一定物质的量浓度的上述消毒液需要选用如图所示的部分仪器,还需要的玻璃仪器是__________ (填仪器名称)。
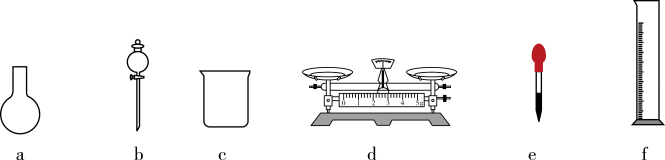
(4)请将下列各操作按正确的顺序将字母代号填写在横线上____________________ 。
A.用托盘天平称取NaClO固体
B.塞好瓶塞,反复颠倒摇匀,装瓶,贴标签
C.加蒸馏水至离容量瓶瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线
D.用适量蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液一并转入容量瓶,并轻摇容量瓶使其混匀
E.待溶液冷却至室温,再将溶液转入容量瓶
F.将已称量的NaClO固体置于烧杯中,加适量蒸馏水溶解完全
(5)若所配制的次氯酸钠溶液的物质的量浓度偏小,则下列可能的原因分析中正确的是__________。

| A.“84消毒液的有效成分是NaClO |
| B.“洁厕灵”(主要成分为盐酸)与“84消毒液”混用效果更好 |
C.检验该消毒液中是否含有 的原理为: 的原理为: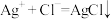 |
| D.盛装“84消毒液”的瓶子瓶盖忘盖,长时间后可能失效 |
(2)该“84消毒液”的物质的量浓度约为
 。(保留一位小数)
。(保留一位小数)(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。配制一定物质的量浓度的上述消毒液需要选用如图所示的部分仪器,还需要的玻璃仪器是

(4)请将下列各操作按正确的顺序将字母代号填写在横线上
A.用托盘天平称取NaClO固体
B.塞好瓶塞,反复颠倒摇匀,装瓶,贴标签
C.加蒸馏水至离容量瓶瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线
D.用适量蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液一并转入容量瓶,并轻摇容量瓶使其混匀
E.待溶液冷却至室温,再将溶液转入容量瓶
F.将已称量的NaClO固体置于烧杯中,加适量蒸馏水溶解完全
(5)若所配制的次氯酸钠溶液的物质的量浓度偏小,则下列可能的原因分析中正确的是__________。
| A.配制前,容量瓶中有少量蒸馏水 | B.洗涤液未转移到容量瓶中 |
| C.未经冷却立即转液 | D.定容时,仰视溶液的凹液面 |
您最近一年使用:0次
名校
解题方法
9 . 对物质进行分类是研究物质性质的重要方法。
I.人们根据分散质粒子的大小,把分散系分为溶液、胶体和浊液等。
(1)清晨的太阳喷薄欲出,霞光万道。与此现象无关 的是___________。
(2)向装有橘红色的硫化锑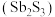 胶体的
胶体的 型管中,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫
型管中,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫___________ ,解释阳极附近橘红色加深的原因___________ 。
II.现有如下含氯元素的物质:①液氯②氯水③盐酸④ ⑤漂白粉
⑤漂白粉
(3)这些物质中,属于纯净物的是(填编号,下同)___________ ,含有 的有
的有___________ 。
(4)对物质进行分类,能够根据类别通性预测物质的性质。 属于酸性氧化物,写出
属于酸性氧化物,写出 与水反应的化学方程式
与水反应的化学方程式___________ 。
(5)上述物质中,漂白粉的有效成分是___________ ,制取漂白粉的化学方程式是___________ ,漂白粉在空气中长时间放置失效的原因是___________ 。(用化学方程式表示)
III.根据物质的分类,得知 为酸性气体,
为酸性气体, 为碱性气体。如图所示,一密闭容器被无摩擦、可自由滑动的两隔板
为碱性气体。如图所示,一密闭容器被无摩擦、可自由滑动的两隔板 分成甲、乙两室;标准状况下,在乙室中充入
分成甲、乙两室;标准状况下,在乙室中充入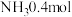 ,甲室中充入的混合气体,静止时隔板位置如图所示。
,甲室中充入的混合气体,静止时隔板位置如图所示。 ;
;
II.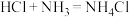 。
。
回答下列问题:
(6)甲室中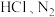 的质量之比为
的质量之比为___________ 。
(7)将隔板 去掉,当
去掉,当 与
与 充分反应生成
充分反应生成 固体后(仅发生此反应),隔板
固体后(仅发生此反应),隔板 将位于刻度“
将位于刻度“___________ ”处(填数字)。
I.人们根据分散质粒子的大小,把分散系分为溶液、胶体和浊液等。
(1)清晨的太阳喷薄欲出,霞光万道。与此现象
| A.云彩属于气溶胶 | B.胶体的聚沉 |
| C.胶体的丁达尔现象 | D.胶粒对光线产生了散射 |
(2)向装有橘红色的硫化锑
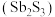 胶体的
胶体的 型管中,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫
型管中,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫II.现有如下含氯元素的物质:①液氯②氯水③盐酸④
 ⑤漂白粉
⑤漂白粉(3)这些物质中,属于纯净物的是(填编号,下同)
 的有
的有(4)对物质进行分类,能够根据类别通性预测物质的性质。
 属于酸性氧化物,写出
属于酸性氧化物,写出 与水反应的化学方程式
与水反应的化学方程式(5)上述物质中,漂白粉的有效成分是
III.根据物质的分类,得知
 为酸性气体,
为酸性气体, 为碱性气体。如图所示,一密闭容器被无摩擦、可自由滑动的两隔板
为碱性气体。如图所示,一密闭容器被无摩擦、可自由滑动的两隔板 分成甲、乙两室;标准状况下,在乙室中充入
分成甲、乙两室;标准状况下,在乙室中充入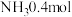 ,甲室中充入的混合气体,静止时隔板位置如图所示。
,甲室中充入的混合气体,静止时隔板位置如图所示。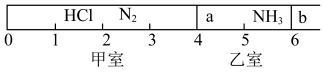
 ;
;II.
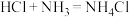 。
。回答下列问题:
(6)甲室中
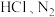 的质量之比为
的质量之比为(7)将隔板
 去掉,当
去掉,当 与
与 充分反应生成
充分反应生成 固体后(仅发生此反应),隔板
固体后(仅发生此反应),隔板 将位于刻度“
将位于刻度“
您最近一年使用:0次
名校
10 . 按要求填空
(1)将含 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每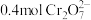 转移
转移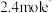 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ (用离子方程式表示)。
(3) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: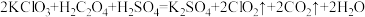 。产生
。产生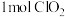 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ ;该反应中的氧化剂是___________ (填化学式)。
(1)将含
 的废水调至
的废水调至 为2~3,再加入
为2~3,再加入 溶液(转化为
溶液(转化为 ),该反应发生时,每
),该反应发生时,每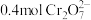 转移
转移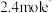 ,该反应的离子方程式为
,该反应的离子方程式为(2)生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
(3)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过反应制得: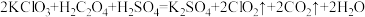 。产生
。产生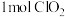 时,转移的电子的物质的量为
时,转移的电子的物质的量为
您最近一年使用:0次



