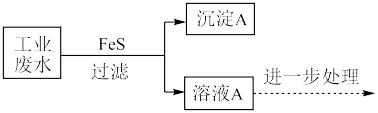
1 . 利用FeS作为沉淀剂除去某工业废水中Pb2+的部分流程如下:
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因___________ 。
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=___________ mol·L-1。(只写计算结果)
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是___________ mg。
| 溶度积(均为18~25℃数据) | |
| Ksp(FeS) | Ksp(PbS) |
| 约为10-18 | 约为10-28 |
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是
您最近一年使用:0次
名校
2 . 请按要求完成下列方程式的书写。
(1) 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)金属钠投入氯化钠溶液_______ 。
(3)酸性条件下 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:_______ 。
(4)氢氧化铁受热分解:_______ 。
(1)
 与
与 反应的化学方程式:
反应的化学方程式:(2)金属钠投入氯化钠溶液
(3)酸性条件下
 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:(4)氢氧化铁受热分解:
您最近一年使用:0次
名校
3 . 完成下列问题
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为_______ ,该反应中氧化剂和还原剂的个数比为_______ ,该反应每生成2个 转移
转移_______ 个电子。
(2)某同学拟用该原理按如下装置制备并收集纯净的 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置_______ (填“甲”“乙”或“丙”)。 中除
中除 外还含有
外还含有_______ (填化学式),试剂X是_______ 。
(4)通过大量实验证明, 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如_______ 所示(图1或图2),氯离子浓度随时间变化如_______ 所示(图1或图2),请在图3中画出氧气的体积随时间变化的趋势图_______ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为
 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为 转移
转移(2)某同学拟用该原理按如下装置制备并收集纯净的
 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置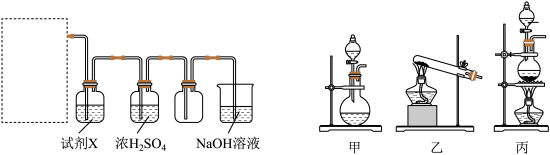
 中除
中除 外还含有
外还含有(4)通过大量实验证明,
 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如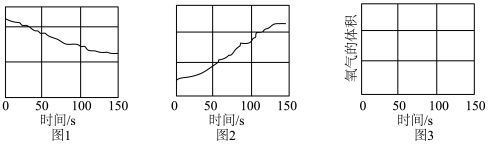
您最近一年使用:0次
名校
解题方法
4 . 结合情景书写化学(离子)方程式。
(1)有研究报道称通过注射器将很少量液态的钠合金注射到目标组织,与组织中的水分发生化学反应,可在局部产生高温,对早期肿瘤可能达到完全消融的效果。其反应的高子方程式为:_______ 。
(2)工业上制备盐酸可通过两种气体燃烧后,将生成物通入水中制得。其反应的化学方程式为:_______ 。
(3)将铁丝灼烧至红热时,铁可与氯气发生反应。其反应的化学方程式为:_______ 。
(4)氯水久置后漂白性减弱,发生的变化可用化学方程式表示为_______ 。
(5)过氧化钠可用于呼吸面具或者潜艇中的供氧剂,其可与人呼出的 发生反应,该反应的化学方程式为:
发生反应,该反应的化学方程式为:_______ 。
(1)有研究报道称通过注射器将很少量液态的钠合金注射到目标组织,与组织中的水分发生化学反应,可在局部产生高温,对早期肿瘤可能达到完全消融的效果。其反应的高子方程式为:
(2)工业上制备盐酸可通过两种气体燃烧后,将生成物通入水中制得。其反应的化学方程式为:
(3)将铁丝灼烧至红热时,铁可与氯气发生反应。其反应的化学方程式为:
(4)氯水久置后漂白性减弱,发生的变化可用化学方程式表示为
(5)过氧化钠可用于呼吸面具或者潜艇中的供氧剂,其可与人呼出的
 发生反应,该反应的化学方程式为:
发生反应,该反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
5 . 有以下几种物质:①食盐晶体;②Fe;③蔗糖;④酒精;⑤醋酸晶体;⑥ ;⑦盐酸;⑧熔融的
;⑦盐酸;⑧熔融的 ;⑨干冰;⑩氨水。填空回答(填序号):
;⑨干冰;⑩氨水。填空回答(填序号):
(1)以上物质可以导电的是_______ ;
(2)以上物质中属于电解质的是_______ ;
(3)以上物质中属于非电解质的是_______ 。
 ;⑦盐酸;⑧熔融的
;⑦盐酸;⑧熔融的 ;⑨干冰;⑩氨水。填空回答(填序号):
;⑨干冰;⑩氨水。填空回答(填序号):(1)以上物质可以导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
您最近一年使用:0次
6 . 与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是___________ ,被氧化的元素是___________ 。
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为___________ 。
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。___________
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
(5)在该反应中转移电子2mol时,生成H3PO4___________ mol。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
| A.氧化性:KClO3 > H3PO4 | B.氧化性:KClO3 > H2O |
| C.还原性:PH3 > X | D.还原性:PH3 > K2SO4 |
您最近一年使用:0次
名校
解题方法
7 . 平衡思想是化学研究的一个重要观念,在电解质溶液中存在电离平衡、水解平衡、溶解平衡等多种平衡。
I.25℃时,三种弱酸的电离平衡常数如下:
回答下列问题:
(1)碳酸二级电离平衡常数的表达式为Ka2=___________ 。
(2)下列四种离子结合质子能力由大到小的顺序是___________ 。
A.CO B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。___________ mol·L-1。
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
I.25℃时,三种弱酸的电离平衡常数如下:
| 弱酸 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | Ka1=4.2×10-7,Ka2=4.8×10-11 | 3.0×10-8 |
(1)碳酸二级电离平衡常数的表达式为Ka2=
(2)下列四种离子结合质子能力由大到小的顺序是
A.CO
 B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
A.CO +2CH3COOH=2CH3COO-+CO2↑+H2O +2CH3COOH=2CH3COO-+CO2↑+H2O |
| B.ClO-+CH3COOH=CH3COO-+HClO |
C.CO +2HClO=CO2↑+H2O+2ClO- +2HClO=CO2↑+H2O+2ClO- |
D.2ClO-+CO2+H2O=CO +2HClO +2HClO |
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。
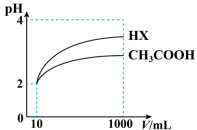
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
| A.大于 | B.等于 | C.小于 | D.无法比较 |
您最近一年使用:0次
名校
解题方法
8 . 写出下列反应的离子方程式。
(1)Ba(OH)2溶液和Na2SO4溶液反应:___________ 。
(2)CaCO3溶液和盐酸溶液反应:___________ 。
(3)CuO和稀硫酸反应:___________ 。
(4)Na2CO3和醋酸溶液反应:___________ 。
(5)Cu(OH)2和稀硝酸反应:___________ 。
(1)Ba(OH)2溶液和Na2SO4溶液反应:
(2)CaCO3溶液和盐酸溶液反应:
(3)CuO和稀硫酸反应:
(4)Na2CO3和醋酸溶液反应:
(5)Cu(OH)2和稀硝酸反应:
您最近一年使用:0次
名校
解题方法
9 . 现有下列物质: 熔融氢氧化钡
熔融氢氧化钡 铜片
铜片 熔融氯化钠
熔融氯化钠 液态氯化氢
液态氯化氢  氢氧化铁胶体
氢氧化铁胶体 硫酸氢钾溶液
硫酸氢钾溶液 乙醇
乙醇 碳酸氢钠粉末
碳酸氢钠粉末  稀硫酸。 回答下列问题:
稀硫酸。 回答下列问题:
(1)以上物质中属于电解质的是___________ ;属于非电解质的是___________ ;属于电解质,但不能导电的是___________ ;能导电的是___________ 。 填序号
填序号
(2) 电离方程式为
电离方程式为___________ ; 电离方程式为
电离方程式为___________ 。
 熔融氢氧化钡
熔融氢氧化钡 铜片
铜片 熔融氯化钠
熔融氯化钠 液态氯化氢
液态氯化氢  氢氧化铁胶体
氢氧化铁胶体 硫酸氢钾溶液
硫酸氢钾溶液 乙醇
乙醇 碳酸氢钠粉末
碳酸氢钠粉末  稀硫酸。 回答下列问题:
稀硫酸。 回答下列问题:(1)以上物质中属于电解质的是
 填序号
填序号
(2)
 电离方程式为
电离方程式为 电离方程式为
电离方程式为
您最近一年使用:0次
名校
解题方法
10 . 氢气在社会发展中有着重要的作用,如新能源的开发,氢能源的储存一直是科学界在研究的方向。利用氨热分解法制氢气是可行方法之一,一定条件下,利用催化剂将氨气分解为氮气和氢气。
(1)已知氨分解的反应的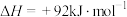 ,
,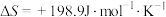 ,在下列哪个温度下反应能自发进行?_____(填标号)
,在下列哪个温度下反应能自发进行?_____(填标号)
(2)已知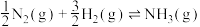 ,
, 该反应化学平衡常数K与温度T的关系如表所示:
该反应化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较 、
、 的大小,
的大小,
_____  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
②400℃时,在 容器中反应
容器中反应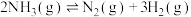 的化学平衡常数为
的化学平衡常数为_____ 。某时刻测得 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的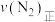
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)如图是合成氨反应平衡混合气中 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强,其中X代表的是
)、X分别代表温度或压强,其中X代表的是_____ (填“温度”或“压强”)。判断 、
、 的大小关系:
的大小关系:
_____  (填“>”、“<或“=”),请说明理由
(填“>”、“<或“=”),请说明理由_____ 。
(1)已知氨分解的反应的
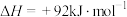 ,
,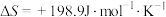 ,在下列哪个温度下反应能自发进行?_____(填标号)
,在下列哪个温度下反应能自发进行?_____(填标号)| A.50℃ | B.100℃ | C.150℃ | D.200℃ |
(2)已知
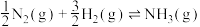 ,
, 该反应化学平衡常数K与温度T的关系如表所示:
该反应化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
①试比较
 、
、 的大小,
的大小,
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);②400℃时,在
 容器中反应
容器中反应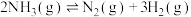 的化学平衡常数为
的化学平衡常数为 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的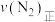
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)如图是合成氨反应平衡混合气中
 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强,其中X代表的是
)、X分别代表温度或压强,其中X代表的是 、
、 的大小关系:
的大小关系:
 (填“>”、“<或“=”),请说明理由
(填“>”、“<或“=”),请说明理由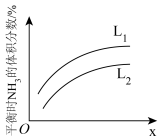
您最近一年使用:0次



