解题方法
1 . 氯的含氧酸盐具有较强的氧化性,能够杀菌消毒,在预防新冠疫情中起到重要作用。某化学兴趣小组用氯气和相应的碱溶液反应制取NaClO和 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。

(1)盛装浓盐酸的仪器名称是_______ 。
(2)装置A烧瓶中反应的化学方程式为_______ 。
(3)装置C中 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为_______ 。
(4)如果缺少装置B,对制取NaClO和 的影响是
的影响是_______ 。
(5)E中可选用试剂有_______ (填标号)。
A.饱和 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液
(6)该小组在探究 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为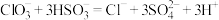 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:
该实验_______ (填“能”或“不能”)达到实验目的,理由是_______ 。
 ,制备装置如图所示(部分加持仪器略去),并研究
,制备装置如图所示(部分加持仪器略去),并研究 的氧化性。已知:氯气与碱反应,温度较高时生成
的氧化性。已知:氯气与碱反应,温度较高时生成 ,温度较低时生成
,温度较低时生成 。
。
(1)盛装浓盐酸的仪器名称是
(2)装置A烧瓶中反应的化学方程式为
(3)装置C中
 与试剂a反应的离子方程式为
与试剂a反应的离子方程式为(4)如果缺少装置B,对制取NaClO和
 的影响是
的影响是(5)E中可选用试剂有
A.饱和
 溶液 B.浓
溶液 B.浓 C.饱和NaCl溶液 D.NaOH溶液
C.饱和NaCl溶液 D.NaOH溶液(6)该小组在探究
 氧化性时,发现
氧化性时,发现 与
与 的反应速率先增大后减小,反应为
的反应速率先增大后减小,反应为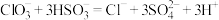 。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究
。小组分析认为,反应生成的离子可能对反应速率产生影响。为了探究 对化学反应速率的影响,设计如下实验:
对化学反应速率的影响,设计如下实验:| 实验序号 | 温度 |  | 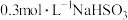 |  盐酸 盐酸 |  |
| ① | 25℃ | 10mL | 10mL | 0mL | 1mL |
| ② | 25℃ | 10mL | 10mL | 1mL | 0mL |
您最近一年使用:0次
2021-06-17更新
|
401次组卷
|
2卷引用:河南省郑州市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
2 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
395次组卷
|
3卷引用:上海市松江二中2021-2022学年高一上学期期末考试化学试题
名校
解题方法
3 . 舍勒制备氯气的方法至今还在实验室使用。按照下图所示装置进行有关实验,打开玻璃活塞F,将A逐滴加入B中。若A中盛放浓盐酸,B中盛放二氧化锰。

回答下列问题:
(1)仪器A的名称是___________ 。
(2)写出当将A滴入B中并加热时发生反应的化学方程式,并用双线桥法表示电子转移的方向和数目___________
(3)当实验进行一段时间后,发现盛装铜粉的硬质玻璃管C中有棕黄色烟产生,则C中发生反应的化学方程式为___________ 。
(4)若将装置Ⅱ换成装置Ⅳ,则可观察到装置Ⅳ的现象为___________
(5)若E中盛有NaOH溶液,此溶液的作用是___________ ,D装置的作用是___________ 。
(6)通过电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式___________ 。

回答下列问题:
(1)仪器A的名称是
(2)写出当将A滴入B中并加热时发生反应的化学方程式,并用双线桥法表示电子转移的方向和数目
(3)当实验进行一段时间后,发现盛装铜粉的硬质玻璃管C中有棕黄色烟产生,则C中发生反应的化学方程式为
(4)若将装置Ⅱ换成装置Ⅳ,则可观察到装置Ⅳ的现象为
(5)若E中盛有NaOH溶液,此溶液的作用是
(6)通过电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式
您最近一年使用:0次
名校
4 . 自来水厂可用氯气对自来水杀菌、消毒,在自来水出厂前,自来水厂的水质检验员利用化学分析仪器等对水中的一些物质(如 )进行检测,并进行数据分析。
)进行检测,并进行数据分析。
(1)氯气的命名由来如图所示,在第一次世界大战中,氯气被用来制作毒气弹,使受害者的身体遭受严重损伤。由此可知Cl2为_______ 气体。
(2)某化学兴趣小组设计实验制备Cl2。
①利用KMnO4与浓盐酸制备氯气,则应选择装置_______ (填标号),发生反应的离子方程式为_______ 。

②①中制得的Cl2中含有少量的HCl,原因是_______ ,通常用_______ (填试剂名称)除去Cl2中的HCl。
(3)将上述制得的Cl2通入水中可得到新制氯水,该过程可选用装置_______ (填标号),其中NaOH溶液的作用是_______ 。

(4)若将氯气通入紫色石蕊溶液中,现象为_______ 。
 )进行检测,并进行数据分析。
)进行检测,并进行数据分析。(1)氯气的命名由来如图所示,在第一次世界大战中,氯气被用来制作毒气弹,使受害者的身体遭受严重损伤。由此可知Cl2为
| 资料卡片 氯气的命名 1810年,英国化学家戴维以大量事实为依据,确认黄绿色气体是一种新元素组成的单质,并将这种元素命名为chlorine。这一名称来自希腊文,有“绿色”的意思。中文译名曾为“绿气”,后改为“氯气”。 |
①利用KMnO4与浓盐酸制备氯气,则应选择装置

②①中制得的Cl2中含有少量的HCl,原因是
(3)将上述制得的Cl2通入水中可得到新制氯水,该过程可选用装置

(4)若将氯气通入紫色石蕊溶液中,现象为
您最近一年使用:0次
2021-11-11更新
|
130次组卷
|
3卷引用:河南省新乡市2021-2022学年高一上学期期中考试化学试题
名校
解题方法
5 . 氯气在生产生活中应用广泛。
(1)实验室可用 与浓盐酸反应制取,反应原理如下:
与浓盐酸反应制取,反应原理如下: ,若制得标准状况下
,若制得标准状况下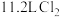 ,则被氧化的
,则被氧化的 为
为_______  。
。
(2)多余的氯气可用 溶液吸收,反应的离子方程式为
溶液吸收,反应的离子方程式为_______ 。工业上也可用 溶液吸收氯气获得
溶液吸收氯气获得 ,
, 广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式
广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式_______ 。
(3)海底蕴藏着丰富的锰结核矿,其主要成分是 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的
。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的 ,其制备过程如图所示:
,其制备过程如图所示:

①步骤1中,试剂甲必须具有的性质是_______ (填序号)。
A. 氧化性 B. 还原性 C. 酸性
②步骤Ⅲ中,以 为氧化剂,当生成
为氧化剂,当生成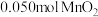 时,消耗
时,消耗 的
的 溶液
溶液 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)已知:① 常温下与浓盐酸反应可制得
常温下与浓盐酸反应可制得 。②
。② 不溶于水。根据如图所示装置回答以下问题。
不溶于水。根据如图所示装置回答以下问题。
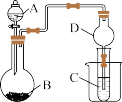
①利用如图装置可以验证元素非金属性的变化规律。图中 装置的名称是
装置的名称是_______ 。干燥管 的作用是
的作用是_______ 。
②实验室中现有药品 、
、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为
,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为_______ 。装置 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为_______ 。
(1)实验室可用
 与浓盐酸反应制取,反应原理如下:
与浓盐酸反应制取,反应原理如下: ,若制得标准状况下
,若制得标准状况下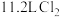 ,则被氧化的
,则被氧化的 为
为 。
。(2)多余的氯气可用
 溶液吸收,反应的离子方程式为
溶液吸收,反应的离子方程式为 溶液吸收氯气获得
溶液吸收氯气获得 ,
, 广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式
广泛应用于电子工业、印染工业等领域。请写出该化学反应的离子方程式(3)海底蕴藏着丰富的锰结核矿,其主要成分是
 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的
。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的 ,其制备过程如图所示:
,其制备过程如图所示:
①步骤1中,试剂甲必须具有的性质是
A. 氧化性 B. 还原性 C. 酸性
②步骤Ⅲ中,以
 为氧化剂,当生成
为氧化剂,当生成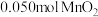 时,消耗
时,消耗 的
的 溶液
溶液 ,该反应的离子方程式为
,该反应的离子方程式为(4)已知:①
 常温下与浓盐酸反应可制得
常温下与浓盐酸反应可制得 。②
。② 不溶于水。根据如图所示装置回答以下问题。
不溶于水。根据如图所示装置回答以下问题。
①利用如图装置可以验证元素非金属性的变化规律。图中
 装置的名称是
装置的名称是 的作用是
的作用是②实验室中现有药品
 、
、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为
,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为
您最近一年使用:0次
名校
6 . 实验室用如下装置制取氯气,并用氯气进行实验,E中为红色湿布条,F中为蘸有NaBr溶液的棉花团,已知溴水为橙黄色。下列说法错误的是
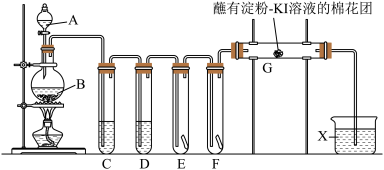

| A.仪器A、B的名称分别为分液漏斗、圆底烧瓶 |
| B.E中布条褪色,F中棉花团变黄,G中棉花团变蓝 |
| C.根据F和G中的实验现象,可证明氧化性:Cl2>Br2>I2 |
| D.试管C、D、X中分别盛有饱和食盐水、浓硫酸、氢氧化钠溶液 |
您最近一年使用:0次
2022-09-21更新
|
435次组卷
|
3卷引用:广东省深圳实验学校2021-2022学年高一上学期第二阶段考试化学试题
7 . 氯及其化合物在工业生产生活中有很重要的作用。图中为实验室通常制取氯气及性质验证的装置图:
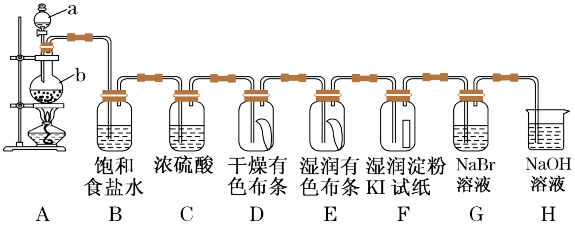
(1)H装置的作用____ ,写出发生的离子反应方程式____ 。
(2)在装置E中可观察到的现象是____ ,通过D、E中的现象说明什么结论____ 。
(3)装置G中发生的离子方程式____ 。
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式_____ 。该反应中氧化剂与还原剂的物质的量之比为____ 。标况下反应生成11.2L的Cl2,则该反应转移的电子的数目为____ ;被氧化的HCl的物质的量为____ 。
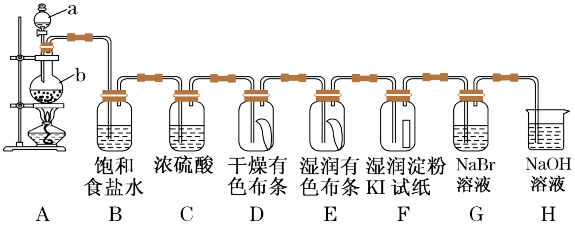
(1)H装置的作用
(2)在装置E中可观察到的现象是
(3)装置G中发生的离子方程式
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式
您最近一年使用:0次
8 . 气体X的主要成分是Cl2(含有少量水蒸气),某学习小组用如图装置研究气体X的性质。请回答下列问题:

(1)C中的现象是___ ;结合化学方程式说明B、C中现象不同的原因___ 。
(2)需要在D处连接如图所示装置,气体应该由___ (填“a”或“b”)管通入。该装置的作用是___ ,用离子方程式表示其原理___ 。


(1)C中的现象是
(2)需要在D处连接如图所示装置,气体应该由

您最近一年使用:0次
2021-11-06更新
|
316次组卷
|
3卷引用:北京市丰台区2021-2022学年高一上学期期中考试化学试题
北京市丰台区2021-2022学年高一上学期期中考试化学试题(已下线)2.2.1 氯气与水、碱的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)【定心卷】2.2.1 氯气的性质随堂练习-人教版2023-2024学年必修第一册
9 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 。
。

请回答下列问题:
(1)写出D的名称___________ ,E的俗称___________ 。Na2FeO4中Fe元素的化合价为___________ 。
(2)写出反应②的离子方程式:___________ 。
(3)反应③,F在A中点燃的反应现象为:___________ 。
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:_____
2 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O
(5)写出反应⑤的化学方程式:___________ 。
 。
。
请回答下列问题:
(1)写出D的名称
(2)写出反应②的离子方程式:
(3)反应③,F在A中点燃的反应现象为:
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:
2
 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O(5)写出反应⑤的化学方程式:
您最近一年使用:0次
2021-11-20更新
|
1461次组卷
|
4卷引用:浙江省温州十校联合体2021-2022学年高一上学期期中考试化学试题
解题方法
10 . X、Y、Z、W、T是原子序数依次增大的五种短周期元素,其中X元素的一种原子中没有中子,Y的一种单质是自然界中最坚硬的物质,Z原子的最外层电子比次外层电子多3个,W与Y同主族,T单质与NaOH溶液反应的产物能杀菌消毒。
(1)X与Y形成的最简单化合物的结构式为___________ 。
(2)Z的最高价氧化对应水化物的稀溶液与铜反应的离子方程式为___________ 。
(3)T单质与NaOH溶液反应的产物中,有杀菌消毒作用的物质为___________ (填化学式)。
(4)利用下图装置可以验证Y、Z、W三种元素性质的递变规律。则:
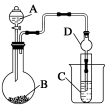
仪器A的名称为___________ ,干燥管D的作用是___________ 。若要证明非金属性:Z>Y>W,则A中应加___________ ,B中应加Na2CO3,C中应加___________ ,观察到C中溶液的现象为___________ 。
(1)X与Y形成的最简单化合物的结构式为
(2)Z的最高价氧化对应水化物的稀溶液与铜反应的离子方程式为
(3)T单质与NaOH溶液反应的产物中,有杀菌消毒作用的物质为
(4)利用下图装置可以验证Y、Z、W三种元素性质的递变规律。则:

仪器A的名称为
您最近一年使用:0次



