19-20高一下·浙江·阶段练习
名校
解题方法
1 . 氮及其化合物的转化关系如下图所示,则下列说法不正确的是
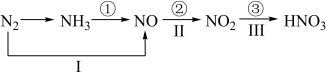
| A.路线①②③是工业生产硝酸的主要途径 | B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.上述所有反应都是氧化还原反应 | D.氮气可在足量的氧气中通过一步反应生成 |
您最近一年使用:0次
2024-03-12更新
|
1150次组卷
|
45卷引用:陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题河北保定市博野县实验中学2020-2021学年高一下学期期中考试化学试题山西省怀仁市大地学校2020-2021学年高一下学期第三次月考化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题江苏省镇江中学2020-2021学年高一下学期期中检测化学试题吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)河北省大名县第一中学2021-2022学年高二上学期开学考试化学试题江苏省常熟市2021-2022学年高二学生暑期自主学习调查化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题广西百色民族高级中学2021-2022学年高二上学期9月月考化学试题陕西省安康市2023-2024学年高二上学期开学考化学试题(已下线)【浙江新东方】双师185高一下(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市晋元高级中学2021-2022学年高一下学期期中考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期中考试化学试题上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)安徽省亳州市第二中学2021-2022学年高一下学期期末考试化学试题湖北省襄阳市第三中学2021-2022学年高一下学期期中考试化学试题江苏省盐城市响水县清源高级中学2021-2022学年高一下学期期中考试化学试题河南省周口经济开发区黄泛区高级中学2021-2022学年高一下学期第一次月考化学试题宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)河南省郑州市第七高级中学2022-2023 学年高一上学期期末考试化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系广东省茂名市电白区2021-2022学年高一下学期期中(选择性)考试化学试题广东省佛山市顺德区罗定邦中学2022-2023学年高一下学期3月第一次月考化学试题贵州省松桃民族中学2022-2023学年高一下学期3月月考化学试题广东省顺德市李兆基中学2022-2023学年高一下学期4月期中考试化学试题浙江省余姚中学2022-2023学年高一下学期期中考试 (选考)化学试题广西钦州市浦北县2022-2023学年高一下学期4月期中考试化学试题(已下线)第6讲 硝酸 含氮化合物之间的转化江苏省徐州市王杰中学2023-2024学年高一下学期第一次月考化学试题宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题14 2024年苏州昆山柏庐高级中学高一3月月考广西南宁一中2023-2024学年高一下学期3月教学质量调研化学试卷福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题天津市实验中学滨海学校2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
2 .  是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示: 在氮肥工业中发生的是
在氮肥工业中发生的是_______ (填“氧化还原”或“非氧化还原”)反应。
(2)实验室制取氨气通常有两种方法:
Ⅰ.用固体氢氧化钙与氯化铵共热;
Ⅱ.在常温下用固体氢氧化钠与浓氨水混合。
①方法Ⅰ制取氨气的化学方程式为_______ 。
②方法Ⅱ应选用图1的_______ (填“A”或“B”)装置进行。_______ (填“甲”、“乙”或“丙”)进行连接。 与
与 反应的化学方程式为
反应的化学方程式为_______ 。制备硝酸过程中,可循环使用的物质是_______ (填化学式)。
(4)工业上制备的浓硝酸可用铝槽车或铁槽车来运输,原因是_______ ,说明浓硝酸具有_______ 性。
 是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
是一种重要的化工产品,是氮肥工业和制造硝酸、铵盐的重要原料。工业流程如图所示:
 在氮肥工业中发生的是
在氮肥工业中发生的是(2)实验室制取氨气通常有两种方法:
Ⅰ.用固体氢氧化钙与氯化铵共热;
Ⅱ.在常温下用固体氢氧化钠与浓氨水混合。
①方法Ⅰ制取氨气的化学方程式为
②方法Ⅱ应选用图1的


 与
与 反应的化学方程式为
反应的化学方程式为(4)工业上制备的浓硝酸可用铝槽车或铁槽车来运输,原因是
您最近一年使用:0次
2023-08-04更新
|
135次组卷
|
2卷引用:陕西省西安市阎良区2020-2021学年高一上学期期末考试化学试题
名校
3 . 在给定条件下,下列物质间的转化过程均能一步实现的是
A.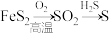 | B.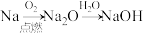 |
C.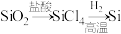 | D. |
您最近一年使用:0次
2023-01-08更新
|
109次组卷
|
2卷引用:陕西省咸阳市秦都区2021-2022学年高一上学期期末考试化学试题
4 . 已知由短周期常见元素形成的纯净物A、B、C、D、E、F、X转化关系如图所示,B、X为单质,D常温下为无色液体,A、B含同一种元素。 某些产物可能略去
某些产物可能略去 请回答下列问题:
请回答下列问题:
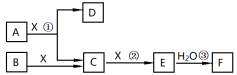
(1)若E是红棕色气体,F是一元强酸,反应①是工业制备F的第一步反应.
① 写出A与X反应的化学方程式:________ 。
② 在常温下,向pH=12的A的水溶液中加入等体积pH=2的盐酸,则反应后溶液的pH_____ 7(填“<”、“=”或“>”)
③ 已知常温下46g气体E与 发生反应③放出46kJ热量,写出气体E与
发生反应③放出46kJ热量,写出气体E与 发生反应③的热化学方程式
发生反应③的热化学方程式_____ 。
(2)若E为无色无味气体, F是二元弱酸:
① 请写出和E互为等电子体的一种分子的分子式:_______ 。
② 将少量气体E通入氢氧化钡溶液中得不溶物H,现将该沉淀放入0.1mol·L-1 的 溶液中,其
溶液中,其 
_____ (填“增大”、“减小”或“不变”),此时组成不溶物H的阴离子在溶液中的浓度为_______ mol·L-1 。(H的
 某些产物可能略去
某些产物可能略去 请回答下列问题:
请回答下列问题: 
(1)若E是红棕色气体,F是一元强酸,反应①是工业制备F的第一步反应.
① 写出A与X反应的化学方程式:
② 在常温下,向pH=12的A的水溶液中加入等体积pH=2的盐酸,则反应后溶液的pH
③ 已知常温下46g气体E与
 发生反应③放出46kJ热量,写出气体E与
发生反应③放出46kJ热量,写出气体E与 发生反应③的热化学方程式
发生反应③的热化学方程式(2)若E为无色无味气体, F是二元弱酸:
① 请写出和E互为等电子体的一种分子的分子式:
② 将少量气体E通入氢氧化钡溶液中得不溶物H,现将该沉淀放入0.1mol·L-1 的
 溶液中,其
溶液中,其 

您最近一年使用:0次
名校
解题方法
5 . 利用 分子筛催化剂,
分子筛催化剂, 可脱除燃煤烟气中的NO和
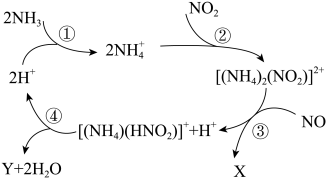
可脱除燃煤烟气中的NO和 ,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
 分子筛催化剂,
分子筛催化剂, 可脱除燃煤烟气中的NO和
可脱除燃煤烟气中的NO和 ,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
,生成两种无毒物质,其反应历程如图所示,下列说法正确的是
A.上述总反应为: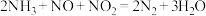 |
B.X是HNO3、Y是 |
| C.阶段②④中都是氧化还原反应 |
D. 、 、 中的化学键形成方式完全相同 中的化学键形成方式完全相同 |
您最近一年使用:0次
2021-04-29更新
|
505次组卷
|
5卷引用:陕西省宝鸡市渭滨区2021届高三适应性训练(一)理综化学试题
陕西省宝鸡市渭滨区2021届高三适应性训练(一)理综化学试题(已下线)押山东卷第13题 陌生反应机理选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)专题14 海水资源的综合利用 环境保护与绿色化学 (限时精炼)-2022年高三毕业班化学常考点归纳与变式演练湖南省常德市桃源县第一中学2022届高三下学期第三次模拟考试化学试题第四章 非金属及其化合物 热点强化10 绿色化学与环境保护
6 . 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。

请回答下列问题:
(1)若A是黄绿色的气体,D是铁单质。则B是_____ (填化学式)。
(2)若A是一种有刺激性气味的气体,其水溶液呈碱性;B和C是常见的氧化物且C是红棕色气体。则反应①的化学方程式为_____ ,A的用途有_____ (任写一种)。
(3)若A、C、D都是气体,B是一种(淡)黄色的固体单质,C是形成酸雨的主要物质。在标准状况下,反应③中消耗6.72L的A,则转移的电子数为_____ 。
(4)若A是钠盐,B俗称小苏打,则反应②的离子方程式为_____ ;配制250mL0.1mol·L-1Na2CO3溶液,需要用托盘天平称量Na2CO3晶体的质量为_____ 克。

请回答下列问题:
(1)若A是黄绿色的气体,D是铁单质。则B是
(2)若A是一种有刺激性气味的气体,其水溶液呈碱性;B和C是常见的氧化物且C是红棕色气体。则反应①的化学方程式为
(3)若A、C、D都是气体,B是一种(淡)黄色的固体单质,C是形成酸雨的主要物质。在标准状况下,反应③中消耗6.72L的A,则转移的电子数为
(4)若A是钠盐,B俗称小苏打,则反应②的离子方程式为
您最近一年使用:0次
名校
7 . 下列各组物质之间不可能实现如图所示转化的是


| 选项 | X | Y | Z | M |
| A |  |  |  |  |
| B |  |  |  |  |
| C | S | SO2 | SO3 | O2 |
| D | NH3 | NO | NO2 | O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-29更新
|
407次组卷
|
3卷引用:陕西省咸阳市2020-2021学年高一上学期期末教学质量检测化学试题
8 . 氮及其化合物的变化关系如图所示:
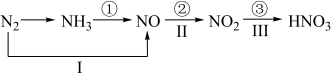
则下列说法不正确的是( )

则下列说法不正确的是( )
| A.路线①②③是工业生产硝酸的主要途径 |
| B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.反应③中,NO2作氧化剂,H2O作还原剂 |
| D.液氨可用作制冷剂,硝酸可用于制化肥、农药、炸药、染料、盐类等 |
您最近一年使用:0次
2020-01-17更新
|
323次组卷
|
8卷引用:陕西省韩城市西庄中学2021-2022学年高三上学期9月月考化学试题
名校
解题方法
9 . 利用元素的化合价推测物质的性质是化学研究的重要手段,氮元素的常见化合价与部分物质类别的对应关系如图所示。

(1)从氮元素化合价的角度分析,X、Y、Z、W中既具有氧化性又具有还原性的有______ (填化学式)。
(2) N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_______________ 。尾气中的NO用酸性NaClO溶液吸收,其原理是HClO氧化NO生成Cl−和NO3-,其离子方程式为______________________________________ 。
(3)将集满红棕色气体Z的试管倒置于盛有水的水槽中,观察到的现象为_______________________ 。
(4)W的稀溶液与铜单质发生反应的离子方程式为__________________________ 。
(5)已知NaNO2能被酸性KMnO4溶液氧化为NaNO3,则50mL0.01 mol·L-1 NaNO2溶液与10mL0.02 mol·L-1 KMnO4溶液恰好完全反应时,还原产物中Mn元素的化合价为__________________________ 。

(1)从氮元素化合价的角度分析,X、Y、Z、W中既具有氧化性又具有还原性的有
(2) N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(3)将集满红棕色气体Z的试管倒置于盛有水的水槽中,观察到的现象为
(4)W的稀溶液与铜单质发生反应的离子方程式为
(5)已知NaNO2能被酸性KMnO4溶液氧化为NaNO3,则50mL0.01 mol·L-1 NaNO2溶液与10mL0.02 mol·L-1 KMnO4溶液恰好完全反应时,还原产物中Mn元素的化合价为
您最近一年使用:0次
2020-01-09更新
|
479次组卷
|
6卷引用:陕西省武功县普集高中2021-2022学年高三上学期第四次月考化学试题



