名校
解题方法
1 . 图1是自然界中硫元素的存在示意图,图2是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:

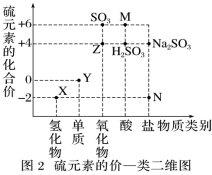
(1)图2中N对应图1中物质的化学式为_______ ,Y与金属铜反应所得产物的化学式为______ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)碳和M的浓溶液反应生成Z的化学方程式为______ 。
(4)为验证(3)中生成的气体产物,化学兴趣小组的同学们在教师指导下设计并进行如图实验:
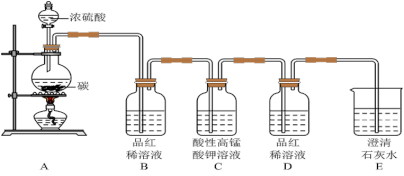
请将能得出对应结论的实验现象填入表中。
(5)从物质分类角度分析判断,下列物质不属于酸性氧化物的是______ (填字母)。
(6)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是______ 。


(1)图2中N对应图1中物质的化学式为
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)碳和M的浓溶液反应生成Z的化学方程式为
(4)为验证(3)中生成的气体产物,化学兴趣小组的同学们在教师指导下设计并进行如图实验:

请将能得出对应结论的实验现象填入表中。
| 验证气体 | 实验现象 | 实验结果 |
| CO2 | ① | 有CO2产生 |
| SO2 | ② | 有SO2产生 |
| A.SO2 | B.SO3 | C.SiO2 | D.NO2 |
您最近一年使用:0次
解题方法
2 . 下列实验操作与实验目的一致的是
| 选项 | 实验操作 | 实验目的 |
| A | 将产生的气体依次通过无水 、品红溶液、高锰酸钾溶液、品红溶液和澄清石灰水 、品红溶液、高锰酸钾溶液、品红溶液和澄清石灰水 | 检验加热条件下木炭与浓硫酸反应后的气体产物 |
| B | 将少量 试样加水溶解,滴加稀 试样加水溶解,滴加稀 酸化,再滴加KSCN溶液 酸化,再滴加KSCN溶液 | 检验 试样是否变质 试样是否变质 |
| C | 测定等浓度的HCl、 两溶液的pH 两溶液的pH | 比较Cl、N的非金属性强弱 |
| D | 向 和 和 混合溶液中,滴加少量 混合溶液中,滴加少量 溶液 溶液 | 比较 与 与 溶度积大小 溶度积大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 硫酸亚铁在农业上可以做杀虫剂,防治大麦的黑穗病,工业上可用于染色和木材防腐。现用以下装置研究硫酸亚铁受热分解的产物。相关固定和加热装置已经省略。左侧试管中的粉末是FeSO4,在实验中用酒精灯对试管进行加热。加热过程中白色粉末逐渐变成红色,在中间U型管中收集到无色透明固体X,右侧集气瓶中收集到少量无色气体Y。实验结束后对相关产物进行了研究。
已知:SO3是无色易挥发的固体,熔点16.8 oC,沸点44.8 oC。
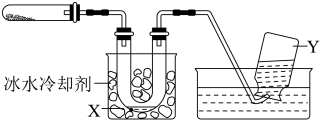
(1)当右侧导管口不再有气泡冒出时,说明反应已经停止,此时合理的操作是___________ 。
(2)为了证明反应后的红色粉末是Fe2O3,而不含Fe3O4和FeO,进行实验:取少量反应后的粉末于试管中,___________ ,证明该粉末中不含Fe3O4和FeO。
(3)实验后将气体Y通入含有品红溶液的试管中,品红褪色,证明集气瓶中收集到的气体Y是___________ 。
(4)根据以上结果,写出FeSO4分解的化学方程式:___________ 。
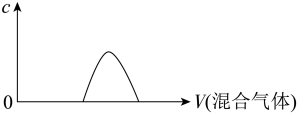
(5)若将反应中产生的SO2和SO3混合气体持续通入到200 mL 0.2 mol/L的NaOH溶液中,溶液中某离子浓度随混合气体体积变化关系如下图所示,写出这种离子的化学式:___________ 。
(6)FeSO4在空气中容易变质为黄褐色碱式硫酸铁,该化合物中含1种阳离子和2种阴离子,且2种阴离子的数目相等,写出由FeSO4生成碱式硫酸铁的化学方程式:___________ 。
已知:SO3是无色易挥发的固体,熔点16.8 oC,沸点44.8 oC。

(1)当右侧导管口不再有气泡冒出时,说明反应已经停止,此时合理的操作是
(2)为了证明反应后的红色粉末是Fe2O3,而不含Fe3O4和FeO,进行实验:取少量反应后的粉末于试管中,
(3)实验后将气体Y通入含有品红溶液的试管中,品红褪色,证明集气瓶中收集到的气体Y是
(4)根据以上结果,写出FeSO4分解的化学方程式:
(5)若将反应中产生的SO2和SO3混合气体持续通入到200 mL 0.2 mol/L的NaOH溶液中,溶液中某离子浓度随混合气体体积变化关系如下图所示,写出这种离子的化学式:

(6)FeSO4在空气中容易变质为黄褐色碱式硫酸铁,该化合物中含1种阳离子和2种阴离子,且2种阴离子的数目相等,写出由FeSO4生成碱式硫酸铁的化学方程式:
您最近一年使用:0次
4 . 某兴趣小组为丰富课本所学的SO2性质,设计了下列系列实验:
(1)用下图装置制取并收集SO2以验证其氧化性
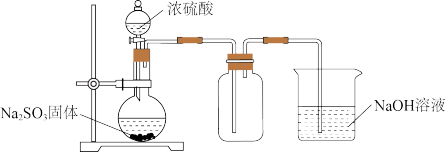
①Na2SO3久置于空气中易变质,体现了Na2SO3具有___________ 性。
②烧杯中NaOH溶液的作用是___________ 。
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为___________ 。
(2)用下图装置验证H2SO3比H2CO3酸性强
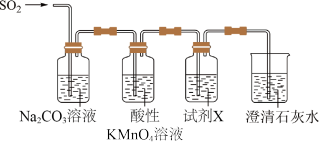
①试剂X是___________ ,其作用是___________ 。
②当观察到___________ ,即证明H2SO3比H2CO3酸性强。
(1)用下图装置制取并收集SO2以验证其氧化性

①Na2SO3久置于空气中易变质,体现了Na2SO3具有
②烧杯中NaOH溶液的作用是
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为
(2)用下图装置验证H2SO3比H2CO3酸性强

①试剂X是
②当观察到
您最近一年使用:0次
2020-12-17更新
|
504次组卷
|
4卷引用:贵州省六盘水市六枝特区2021-2022学年高一下学期期中教学质量检测化学试题
名校
解题方法
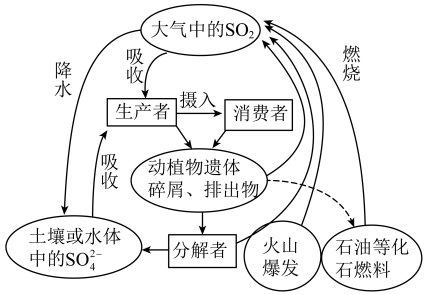
5 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中S的价态变化在-2价至+6价之间,请分析此图并回答有关问题:______ 。
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是___________ (用化学方程式表示)。
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理___________ 。发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入___________ mL SO2.(室温下Vm=24.5L/mol,结果保留3位有效数字,体积变化忽略不计)
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:___________ 。
②关于整个制备过程,下列说法正确的是___________ 。
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
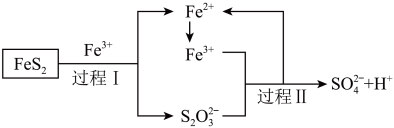
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:___________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式___________ 。
③从氧化还原角度分析,若要制备Na2S2O3应选择___________ (填字母)。
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
| A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
| B.硫化氢通入浓H2SO4中 |
| C.浓H2SO4滴入萤石中,加热 |
| D.向盐酸中加入浓硫酸产生白雾 |
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:

②关于整个制备过程,下列说法正确的是
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:
②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备Na2S2O3应选择
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
您最近一年使用:0次
名校
解题方法
6 . 已知硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O,M=392g/mol](俗称莫尔盐)可溶于水,在100℃~110℃时分解。为探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验,装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ 。_______ →G。
(3)证明含有SO3的实验现象是_______ ,安全瓶H的作用是_______ 。
Ⅱ.为测定硫酸亚铁铵晶体纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000mol/L的酸性KMnO4溶液进行三次滴定。
(4)方案一中发生反应的离子方程式为:_______ 。
(5)方案二中判断所加BaCl2溶液已足量的操作及现象为_______ 。
(6)若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因:_______ 。
(7)乙方案测定出硫酸亚铁铵纯度为_______ (列出计算式即可)。
Ⅰ.探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验,装置C中可观察到的现象是

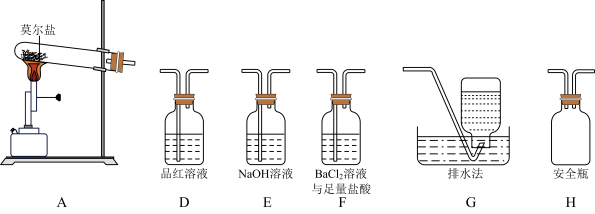
(3)证明含有SO3的实验现象是
Ⅱ.为测定硫酸亚铁铵晶体纯度,称取m g莫尔盐样品,配成500 mL溶液。甲、乙两位同学设计了如下两个实验方案。
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000mol/L的酸性KMnO4溶液进行三次滴定。
(乙)方案二:
(4)方案一中发生反应的离子方程式为:
(5)方案二中判断所加BaCl2溶液已足量的操作及现象为
(6)若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因:
(7)乙方案测定出硫酸亚铁铵纯度为
您最近一年使用:0次
名校
解题方法
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验淀粉是否完全水解 | 将适量样品与稀硫酸共热充分反应,加入足量NaOH溶液后加入碘水,观察现象 | 无明显现象,说明淀粉水解完全 |
| B | 检验CO还原Fe2O3的生成物中是否含有Fe3O4 | 将适量反应后的固体溶于稀盐酸,取少量溶解液于试管中,滴加硫氰化钾溶液 | 溶液变血红色,则证明还原产物中含有Fe3O4 |
| C | 探究FeCl3与KI溶液反应存在限度 | 取2mL0.1mol•L-1KI溶液于试管中,加入5滴等浓度的FeCl3溶液,再加入KSCN溶液 | 若溶液变血红色,则反应存在限度 |
| D | 证明SO2有氧化性 | 将足量的SO2通入BaCl2溶液中,再通入Cl2 | 一开始无沉淀,后出现白色沉淀,说明最后生成的是BaSO4,SO2有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-13更新
|
230次组卷
|
3卷引用:浙江省北斗联盟2022-2023学年高二上学期期中联考化学试题
8 . 如图是铜与浓硫酸反应并验证其产物性质的装置图。请回答下列问题。

(1)试管①中发生反应的化学方程式为_______ 。
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2的水溶液具有_______ 、SO2具有_______ 、漂白性。⑥中反应的离子方程式为_______ 。
(3)下列说法正确的是_______ (填字母)。
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物CuSO4,可立刻向试管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中n(Cu2+)变大的是_______ (填字母)。
a.HCl b.Fe2O3 c.KNO3
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为_______ 。
(6)为了测定尾气中SO2的含量,将尾气样品经过管道通入盛有400mL0.1mol·L-1酸性KMnO4溶液的密闭容器中。若管道中气体流量为aL·min-1,经过8min溶液恰好褪色,假定样品中SO2被充分吸收,该尾气样品中SO2的含量为_______ g·L-1(假设尾气中其他气体不与酸性KMnO4溶液反应)。

(1)试管①中发生反应的化学方程式为
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2的水溶液具有
(3)下列说法正确的是
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物CuSO4,可立刻向试管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中n(Cu2+)变大的是
a.HCl b.Fe2O3 c.KNO3
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为
(6)为了测定尾气中SO2的含量,将尾气样品经过管道通入盛有400mL0.1mol·L-1酸性KMnO4溶液的密闭容器中。若管道中气体流量为aL·min-1,经过8min溶液恰好褪色,假定样品中SO2被充分吸收,该尾气样品中SO2的含量为
您最近一年使用:0次
名校
9 . Ⅰ.某研究小组用如图装置进行 与
与 溶液反应的相关实验(夹持装置已略去)。
溶液反应的相关实验(夹持装置已略去)。
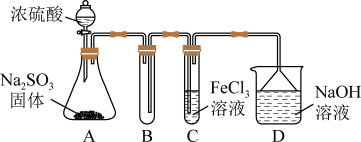
根据以上现象,该小组同学认为 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。
(1)写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(2)为了验证 具有还原性,实验中可以代替
具有还原性,实验中可以代替 的试剂有_______(填序号)。
的试剂有_______(填序号)。
Ⅱ.探究 和
和 的反应
的反应
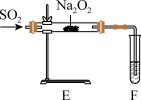
(3)将实验1中制备的 直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为
直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为 和
和 性质相似,其产物应为
性质相似,其产物应为 和
和 ,但是乙同学不赞同,他认为木条复燃可能是
,但是乙同学不赞同,他认为木条复燃可能是 中含有水蒸气的原因,请用化学方程式来解释乙的观点
中含有水蒸气的原因,请用化学方程式来解释乙的观点_______ 。
(4)乙同学认为反应生成的是另外一种盐 ,因为
,因为 具有
具有_______ 性。
(5)为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的300mL 0.100mol/L的酸性高锰酸钾溶液。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的300mL 0.100mol/L的酸性高锰酸钾溶液。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可以被溶液充分吸收,则该样品中的
可以被溶液充分吸收,则该样品中的 含量是
含量是_______ g/L。
 与
与 溶液反应的相关实验(夹持装置已略去)。
溶液反应的相关实验(夹持装置已略去)。
根据以上现象,该小组同学认为
 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。(1)写出
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:(2)为了验证
 具有还原性,实验中可以代替
具有还原性,实验中可以代替 的试剂有_______(填序号)。
的试剂有_______(填序号)。A.酸性 溶液 溶液 | B.浓硫酸 |
| C.NaCl溶液 | D.碘水 |
Ⅱ.探究
 和
和 的反应
的反应
(3)将实验1中制备的
 直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为
直接通入E中,将带火星的木条靠近F的试管口,发现木条复燃,据此现象甲同学认为 和
和 性质相似,其产物应为
性质相似,其产物应为 和
和 ,但是乙同学不赞同,他认为木条复燃可能是
,但是乙同学不赞同,他认为木条复燃可能是 中含有水蒸气的原因,请用化学方程式来解释乙的观点
中含有水蒸气的原因,请用化学方程式来解释乙的观点(4)乙同学认为反应生成的是另外一种盐
 ,因为
,因为 具有
具有(5)为测定空气中
 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的300mL 0.100mol/L的酸性高锰酸钾溶液。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的300mL 0.100mol/L的酸性高锰酸钾溶液。若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可以被溶液充分吸收,则该样品中的
可以被溶液充分吸收,则该样品中的 含量是
含量是
您最近一年使用:0次
名校
解题方法
10 . 研究小组为探究 在空气中变质后的产物,进行如下实验并记录现象。
在空气中变质后的产物,进行如下实验并记录现象。
实验①:取 样品加水溶解,得到澄清溶液a。
样品加水溶解,得到澄清溶液a。
实验②:取少量溶液a,向其中加入过量盐酸,有臭鸡蛋气味的气体生成,且出现淡黄色浑浊。
实验③:将实验②中的浊液过滤,向滤液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
已知信息:i. 溶液能溶解S,并生成
溶液能溶解S,并生成 ,
, 与酸反应生成S和
与酸反应生成S和 (臭鸡蛋气味);ii.
(臭鸡蛋气味);ii. 易溶于水。
易溶于水。
下列说法不正确的是
 在空气中变质后的产物,进行如下实验并记录现象。
在空气中变质后的产物,进行如下实验并记录现象。实验①:取
 样品加水溶解,得到澄清溶液a。
样品加水溶解,得到澄清溶液a。实验②:取少量溶液a,向其中加入过量盐酸,有臭鸡蛋气味的气体生成,且出现淡黄色浑浊。
实验③:将实验②中的浊液过滤,向滤液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。已知信息:i.
 溶液能溶解S,并生成
溶液能溶解S,并生成 ,
, 与酸反应生成S和
与酸反应生成S和 (臭鸡蛋气味);ii.
(臭鸡蛋气味);ii. 易溶于水。
易溶于水。下列说法不正确的是
A.实验②中淡黄色浑浊可能是 与 与 反应产生的 反应产生的 |
B.实验①和实验②说明 样品中一定含有S 样品中一定含有S |
C.实验③中产生的白色沉淀是 |
D. 样品中可能含有 样品中可能含有 |
您最近一年使用:0次
2023-02-09更新
|
685次组卷
|
12卷引用:黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题
黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题北京市西城区2021~2022学年高三上学期期末考试化学试题河北省五校联盟(保定市第一中学等)2021-2022学年高三下学期3月模拟考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)化学-2022年高考押题预测卷01(北京卷)安徽省示范高中培优联盟 2022-2023学年高二上学期联赛化学试题巩固训练7北京市第二中学2022-2023学年高二下学期3月月考化学试题北京交通大学附属中学2023-2024学年高三上学期开学考试化学试题北京市第二中学2023-2024学年高三上学期12月月考化学试题北京市第一○一中学2023-2024学年高三下学期开学考试化学试题(已下线)北京市第四中学2023-2024学年高三下学期一模模拟化学试题



