名校
解题方法
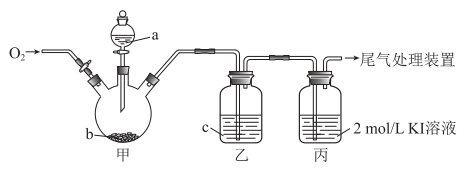
1 . 某小组利用下图装置进行实验(加热、夹持装置略去,已检查气密性),探究CO2、SO2分别通入KI溶液中对反应4I-+4H++O2=2I2+2H2O的影响。
①甲是实验室制CO2的装置,b为石灰石,则c为_______ ,其作用是_______ 。
②实验发现:若仅向丙中通入O2,1小时后丙中溶液颜色未发生明显变化;若同时向丙中通入CO2与O2,1小时后,丙中溶液变为浅黄色,生成了可使淀粉变蓝的物质,该物质是_______ (写化学式)。依据实验现象,可得结论:_______ 。
(2)探究通入SO2的影响。
①若试剂b为Na2SO3,试剂a为70%的硫酸,甲中加热反应的化学方程式是_______ 。
②向丙中同时通入O2和SO2,1小时后,溶液中出现浑浊。查资料可知,O2未参与反应,SO2与水在I-催化下生成了硫单质和硫酸。化学方程式是_______ 。
①甲是实验室制CO2的装置,b为石灰石,则c为
②实验发现:若仅向丙中通入O2,1小时后丙中溶液颜色未发生明显变化;若同时向丙中通入CO2与O2,1小时后,丙中溶液变为浅黄色,生成了可使淀粉变蓝的物质,该物质是
(2)探究通入SO2的影响。
①若试剂b为Na2SO3,试剂a为70%的硫酸,甲中加热反应的化学方程式是
②向丙中同时通入O2和SO2,1小时后,溶液中出现浑浊。查资料可知,O2未参与反应,SO2与水在I-催化下生成了硫单质和硫酸。化学方程式是
您最近一年使用:0次
2022-07-10更新
|
422次组卷
|
6卷引用:北京市西城区2021-2022学年高一下学期期末化学试题
北京市西城区2021-2022学年高一下学期期末化学试题北京市第五十中学2022-2023学年高一下学期期中考试化学试题北京市西城外国语学校2022-2023学年高一下学期期中考试化学试题(已下线)2023年北京卷高考真题变式题(实验探究题)北京市育才学校2023-2024学年高一下学期期中考试化学(选考)试题(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
2 . 铜丝和浓硫酸反应的装置图如下。
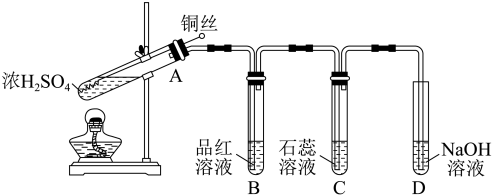
(1)A中反应的化学方程式是_______ 。
(2)A中反应开始后,B中的现象是_______ ,C中的现象是_______ 。
(3)D中NaOH溶液的作用是_______ 。

(1)A中反应的化学方程式是
(2)A中反应开始后,B中的现象是
(3)D中NaOH溶液的作用是
您最近一年使用:0次
2022-07-10更新
|
215次组卷
|
2卷引用:北京市西城区2021-2022学年高一下学期期末化学试题
名校
解题方法
3 . 实验室利用下面装置制取气体。
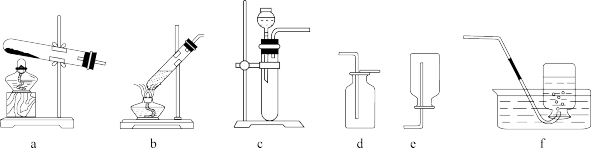
(1)实验室制备NH3的化学方程式为_______ ,反应装置选用_______ (填字母,下同)。
(2)用Cu和稀硝酸制备NO的化学方程式为_______ ,选用装置_______ 收集NO。
(3)用Cu和浓硫酸制备SO2的化学方程式为_______ ,检验SO2的方法是_______ 。

(1)实验室制备NH3的化学方程式为
(2)用Cu和稀硝酸制备NO的化学方程式为
(3)用Cu和浓硫酸制备SO2的化学方程式为
您最近一年使用:0次
解题方法
4 . 某同学用下图所示装置进行 的相关实验。
的相关实验。

请回答:
(1)实验室用铜和浓硫酸反应制取 ,化学方程式为
,化学方程式为___________ 。
(2)装置①中紫色石蕊试剂变红,发生反应的化学方程式为___________ 。
(3)装置②中高锰酸钾溶液褪色,说明 具有
具有___________ 性。
(4)碱石灰的作用是___________ 。
 的相关实验。
的相关实验。
请回答:
(1)实验室用铜和浓硫酸反应制取
 ,化学方程式为
,化学方程式为(2)装置①中紫色石蕊试剂变红,发生反应的化学方程式为
(3)装置②中高锰酸钾溶液褪色,说明
 具有
具有(4)碱石灰的作用是
您最近一年使用:0次
名校
解题方法
5 . 实验室探究NaHSO3溶液与Cu2+的反应。
I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是____ 。
(2)写出C中制备NaHSO3的离子方程式____ 。
II.探究NaHSO3溶液与Cu2+的反应,过程如图所示:
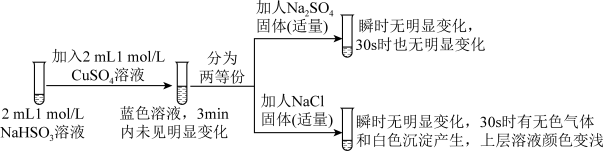
已知:硫酸亚铜易溶于水。
回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因。
a.Cl-改变了HSO 的还原性
的还原性
b.Cl-改变了Cu2+的氧化性
用原电池原理进行试验,探究上述现象可能的原因。
①由实验1、2可知原因a不合理,依据是_____ 。
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。
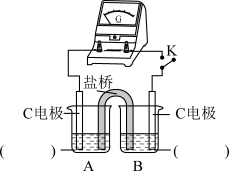
ⅰ.补全电化学装置示意图____ 。
ⅱ.写出B中的电极反应方程式____ 。
ⅲ.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,____ ,使HSO 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。
III.金能与浓硝酸发生微弱反应生成Au3+,短时间几乎观察不到金溶解。金易溶于“王水”[浓硝酸与浓盐酸按体积比1∶3混合]
已知:Au3++4Cl-+H+ HAuCl4
HAuCl4
(4)利用(3)中实验探究的结论,分析“王水”溶金的原理:____ 。
I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是
(2)写出C中制备NaHSO3的离子方程式
II.探究NaHSO3溶液与Cu2+的反应,过程如图所示:

已知:硫酸亚铜易溶于水。
回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因。
a.Cl-改变了HSO
 的还原性
的还原性b.Cl-改变了Cu2+的氧化性
用原电池原理进行试验,探究上述现象可能的原因。
| 编号 | 实验1 | 实验2 |
| 实验 | 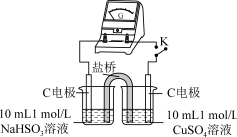 | 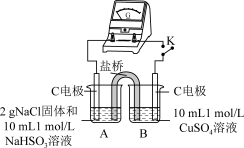 |
| 现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 |
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。

ⅰ.补全电化学装置示意图
ⅱ.写出B中的电极反应方程式
ⅲ.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,
 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。III.金能与浓硝酸发生微弱反应生成Au3+,短时间几乎观察不到金溶解。金易溶于“王水”[浓硝酸与浓盐酸按体积比1∶3混合]
已知:Au3++4Cl-+H+
 HAuCl4
HAuCl4(4)利用(3)中实验探究的结论,分析“王水”溶金的原理:
您最近一年使用:0次
6 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。

(1)装置A中反应的化学方程式为_______ 。
(2)装置B、C中的现象分别是溶液紫色褪去和溶液中出现淡黄色浑浊,这些现象分别说明SO2具有的性质是_______ 和_______
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_______ 。
(4)尾气吸收SO2可采用(填写字母序号)_______

(1)装置A中反应的化学方程式为
(2)装置B、C中的现象分别是溶液紫色褪去和溶液中出现淡黄色浑浊,这些现象分别说明SO2具有的性质是
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(4)尾气吸收SO2可采用(填写字母序号)_______
| A.烧碱溶液 | B.纯碱溶液 | C.氨水 | D.饱和NaHCO3溶液 |
您最近一年使用:0次
名校
解题方法
7 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
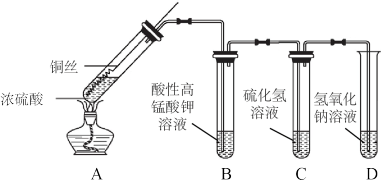
回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是_______ 。
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是_______ 。
(3)用化学方程式表示氢氧化钠溶液的作用是_______ 。
(4)装置A中反应的化学方程式是_______ 。
(5)装置B和装置C分别验证了二氧化硫的_______ 性质。
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。

回答下列问题:
(1)将铜丝下端卷成螺旋状的理由是
(2)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(3)用化学方程式表示氢氧化钠溶液的作用是
(4)装置A中反应的化学方程式是
(5)装置B和装置C分别验证了二氧化硫的
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是_______(填字母)。已知:Cu2S、CuS不溶于稀硫酸。
| 硫酸浓度/(mol· L-1) | 黑色物质出现的温度/°C | 黑色物质消失的温度/°C |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
| B.黑色物质消失过程中有SO2、H2S生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16mol/L时,先升温至250°C以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近一年使用:0次
2022-04-27更新
|
230次组卷
|
2卷引用:北京市第八中学2022-2023学年高一下学期期中考试(选考班)化学试题
8 . 化学小组实验探究SO2与AgNO3溶液的反应。用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。(已知:浓硫酸沸点338°C,酒精灯外焰温度400-500°C)
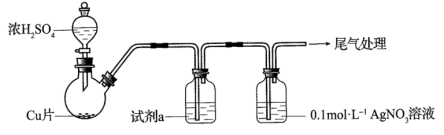
(1)浓H2SO4与Cu反应的化学方程式是_______ 。
(2)试剂a是饱和NaHSO3溶液,目的是为了除去SO2中混有的_______ 杂质。
(3)①白色沉淀B为Ag2SO3,写出生成Ag2SO3的离子方程式_______ 。(反应a)
②无色溶液A放置一段时间后,生成含Ag的灰黑色粉末,写出反应的离子方程式_______ 。(反应b)按照氧化还原思想分析,产物中应该含有SO ,实验证明所需试剂为
,实验证明所需试剂为_______ 。
③根据以上描述,判断反应速率:反应a_______ 反应b(填><或=)

(1)浓H2SO4与Cu反应的化学方程式是
(2)试剂a是饱和NaHSO3溶液,目的是为了除去SO2中混有的
(3)①白色沉淀B为Ag2SO3,写出生成Ag2SO3的离子方程式
②无色溶液A放置一段时间后,生成含Ag的灰黑色粉末,写出反应的离子方程式
 ,实验证明所需试剂为
,实验证明所需试剂为③根据以上描述,判断反应速率:反应a
您最近一年使用:0次
9 . 实验室中用下图装置(夹持装置已略去)研究不同价态硫元素之间的转化。
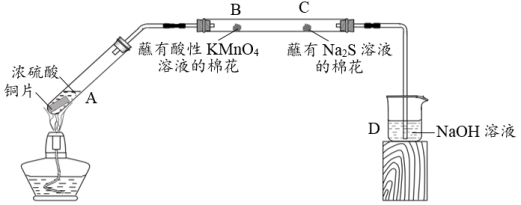
(1)A中产生的气体能使品红溶液褪色,该气体是____ ,A中反应的化学方程式为____ 。
(2)B处实验现象是________ ,由此推测硫元素从+4价变为+6价。
(3)C处观察到蘸有Na2S溶液的棉花上出现淡黄色的固体,可推测此反应过程中硫元素的价态变化分别是________ ,________ 。
(4)D装置的作用是________ ,发生反应的离子方程式为________ 。

(1)A中产生的气体能使品红溶液褪色,该气体是
(2)B处实验现象是
(3)C处观察到蘸有Na2S溶液的棉花上出现淡黄色的固体,可推测此反应过程中硫元素的价态变化分别是
(4)D装置的作用是
您最近一年使用:0次
2022-01-14更新
|
349次组卷
|
2卷引用:北京市海淀区2021-2022学年高一上学期期末参考样题化学试题
名校
解题方法
10 . 某小组同学采用以下装置验证SO2的性质:
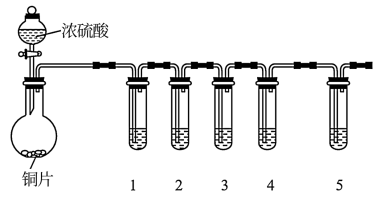
(夹持及加热装置略,试管1:紫色石蕊溶液,试管2:H2S溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5:BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式___________ 。
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象___________ 。
②试管2中现象___________ ,写出反应的化学方程式:___________ 。
③试管3中现象___________ ,说明SO2具有漂白性,证明该漂白的可逆性的实验操作是___________ 。
A.溶液变为红色 B.溶液变为白色 C.溶液变为无色 D.溶液先变为红色后变为无色 E.出现淡黄色沉淀 F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是___________ ,反应离子方程式___________ 。
(4)试管5中无明显现象,将其分成两份,分别加入下列物质,均产生沉淀。将产生的沉淀的化学式填入下表相应位置。
(5)实验的尾气SO2可以用NaOH溶液吸收,反应的离子方程式是___________ 。

(夹持及加热装置略,试管1:紫色石蕊溶液,试管2:H2S溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5:BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象
②试管2中现象
③试管3中现象
A.溶液变为红色 B.溶液变为白色 C.溶液变为无色 D.溶液先变为红色后变为无色 E.出现淡黄色沉淀 F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是
(4)试管5中无明显现象,将其分成两份,分别加入下列物质,均产生沉淀。将产生的沉淀的化学式填入下表相应位置。
| 加入的物质 | H2O2 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次



