解题方法
1 . 氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。
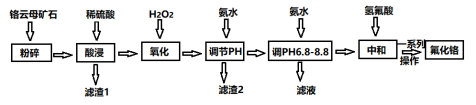
下表列出了相关金属离子生成氢氧化物沉淀的pH:
(1)将铬云母矿石粉碎的目的是___________ 。
(2)滤渣1主要成分的用途是___________ 。(写一种)
(3)“氧化”步骤能否省略___________ (填“是”或“否”),你的依据是___________ 。
(4)Cr2O3与稀硫酸反应的离子方程式为___________ 。
(5)第一次滴加氨水调节pH范围为___________ 。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是___________ ;Cr(OH)3与Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:___________ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
| 沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
(1)将铬云母矿石粉碎的目的是
(2)滤渣1主要成分的用途是
(3)“氧化”步骤能否省略
(4)Cr2O3与稀硫酸反应的离子方程式为
(5)第一次滴加氨水调节pH范围为
(6)第二次滴加氨水调节pH为6.8~8.8的目的是
您最近一年使用:0次
解题方法
2 . 如图,通过工业联产可有效解决多晶硅(Si)生产中副产物SiCl4。所带来的环境问题。
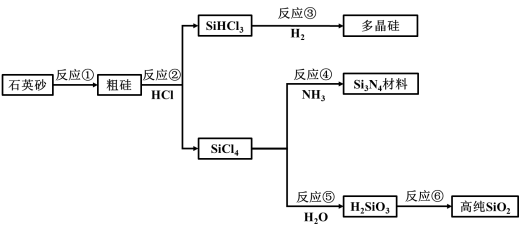
(1)Si在元素周期表中的位置是____________________ 。
(2)反应①的化学方程式为_______________________ 。
(3)流程中涉及的化学反应属于氧化还原反应的有________________ (填反应序号)。
(4)高温下,反应④的化学方程式为_________________ 。
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光是纤维的是__________ 。
(6)Si和Ge属于同主族元素。下列预测合理的是____ (填选项序号)。
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料

(1)Si在元素周期表中的位置是
(2)反应①的化学方程式为
(3)流程中涉及的化学反应属于氧化还原反应的有
(4)高温下,反应④的化学方程式为
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光是纤维的是
(6)Si和Ge属于同主族元素。下列预测合理的是
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料
您最近一年使用:0次
2020-08-12更新
|
1043次组卷
|
2卷引用:福建省厦门市2019-2020学年高一下学期期末考试化学试题
3 . 某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

(1)实验室制备氨气的化学方程式为_________ 。
(2)用装置 B 收集氨气时,应选择氨气的进气口是_________ (选填“a”或“b”),并说明选择的理由是_________ 。
(3)打开装置B 中的止水夹 c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是_____ ,请用方程式表示:_______________________________ ;氨气催化氧化可用于制硝酸,请写出氨气催化氧化的化学方程式 _______________________________ 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
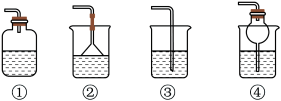
(5)SiO2在自然界中广泛存在,它是制备现代通讯材料________ (写该材料名称)的主要原料;以 SiO2为原料, 在工业上制备单质硅的化学方程式为________

(1)实验室制备氨气的化学方程式为
(2)用装置 B 收集氨气时,应选择氨气的进气口是
(3)打开装置B 中的止水夹 c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

(5)SiO2在自然界中广泛存在,它是制备现代通讯材料
您最近一年使用:0次
名校
4 . 氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有___ 种。
(2)将铬云母矿石粉碎的目的是___ 。
(3)滤渣1主要成分的用途是___ 。(写一种)
(4)Cr2O3与稀硫酸反应的化学方程式为___ 。
(5)第一次滴加氨水调节pH范围为___ 。
(6)第二次滴加氨水调节pH为6.8~8.8的目的是___ ,Cr(OH)3与Al(OH)3一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:___ 。

下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
| 沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)Fe2O3、MgO、FeO、SiO2中属于碱性氧化物的有
(2)将铬云母矿石粉碎的目的是
(3)滤渣1主要成分的用途是
(4)Cr2O3与稀硫酸反应的化学方程式为
(5)第一次滴加氨水调节pH范围为
(6)第二次滴加氨水调节pH为6.8~8.8的目的是
您最近一年使用:0次
2019-11-29更新
|
380次组卷
|
8卷引用:山东省临沂市第一中学2020届高三10月月考化学试题
5 . (1)X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。请回答下列问题:
①X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_______________ 。
②科学家发现,Z在催化剂条件下能与W反应,写出该反应的化学方程式_________________ 。其产物中的单质的结构式为:______________ 。
③检验W气体的方法是_________________________________________________ 。
(2)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质硅的化学方程式为____________________________________ ;在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为____________________________ 。
①X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为
②科学家发现,Z在催化剂条件下能与W反应,写出该反应的化学方程式
③检验W气体的方法是
(2)SiO2在自然界中广泛存在,它是制备现代通讯材料
您最近一年使用:0次
名校
解题方法
6 . 设计如下实验探究橄榄石(仅含三种短周期元素)的组成和性质。

(1)橄榄石的组成元素是O和____ 、____ (填元素符号),化学式为__________ 。
(2)写出白色粉末A的一种用途:__________________________ 。
(3)白色粉末A溶于NaOH溶液的离子方程式是_________________________________ 。

(1)橄榄石的组成元素是O和
(2)写出白色粉末A的一种用途:
(3)白色粉末A溶于NaOH溶液的离子方程式是
您最近一年使用:0次
解题方法
7 . 已知A、B、C、D、E是中学常见的五种化合物。且A、B、C均含有同一种元素,A可用于呼吸面具中的氧气来源,B是制备普通玻璃的主要成分之一,D在常温下是一种常见液体,E是一种两性氢氧化物,F是一种非金属单质。它们之间有如下关系:A+D→C+F,C+E→盐+D。
(1)写出下列物质的化学式:A_____ 、B_____ 、D_____ 、F_______
(2)写出C+E→盐+D的离子方程式_____________________________ ;
(3)E中某元素的单质可与氧化铁发生铝热反应,写出其反应的化学方程式__________________________________ 。
(1)写出下列物质的化学式:A
(2)写出C+E→盐+D的离子方程式
(3)E中某元素的单质可与氧化铁发生铝热反应,写出其反应的化学方程式
您最近一年使用:0次
8 . 为探究固体X(仅含两种常见短周期元素)的组成和性质,设计并完成如下实验:
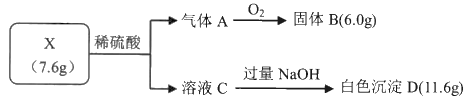
已知:气体A是一种纯净物,在标准状况下的密度为1.429 g/L;固体B是光导纤维的主要成分。请回答:
(1)气体A分子的电子式_____________ ,白色沉淀D的化学式_____________ 。
(2)固体X与稀硫酸反应的离子方程式是_______________________________________ 。
(3)已知NH3与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为140 g/mol)和H2,写出该反应的化学方程式_______________________________________ 。

已知:气体A是一种纯净物,在标准状况下的密度为1.429 g/L;固体B是光导纤维的主要成分。请回答:
(1)气体A分子的电子式
(2)固体X与稀硫酸反应的离子方程式是
(3)已知NH3与气体A在一定条件下反应后可得到一种耐高温陶瓷材料(仅含两种元素,摩尔质量为140 g/mol)和H2,写出该反应的化学方程式
您最近一年使用:0次
2018-03-19更新
|
703次组卷
|
3卷引用:浙江省宁波市2018年3月新高考选考适应性考试化学试题
浙江省宁波市2018年3月新高考选考适应性考试化学试题【全国市级联考】浙江省温州市共美联盟2017-2018学年高二下学期期末模拟化学试题(已下线)2019年1月浙江省普通高中学业水平考试化学仿真模拟试题03
9 . 含A元素的一种单质是一种重要的半导体材料,含 A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)A的原子结构示意图为________ ,A与碳在原子的电子层结构上的相同点是________________________________________________________ 。
(2)易与C发生化学反应的酸是_________ (写名称),反应的化学方程式是_______________________________ 。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D
①写出该反应的化学方程式:___________________________________________ 。
②要将纯碱高温熔化,下列坩埚中可选用的是________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________ 。
(1)A的原子结构示意图为
(2)易与C发生化学反应的酸是
(3)将C与纯碱混合高温熔融时也发生化学反应生成D
①写出该反应的化学方程式:
②要将纯碱高温熔化,下列坩埚中可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是
您最近一年使用:0次
名校
解题方法
10 . (1)用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:光导纤维的主要成分是___________ ;目前应用最多的太阳能电池的光电转化材料是______________ ;
(2)某气态氧化物的化学式为XO2,在标准状况下,1.92 g 该氧化物的体积为672 mL,则该氧化物的摩尔质量为______ 。
(3)某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32-、SO42-中的若干种离子组成,取该溶液进行如下实验:

①白色沉淀甲是________ 。
②试写出实验过程中生成气体B的离子方程式__________________________
③通过上述实验,可确定X溶液中一定存在的离子是_______________________
(2)某气态氧化物的化学式为XO2,在标准状况下,1.92 g 该氧化物的体积为672 mL,则该氧化物的摩尔质量为
(3)某无色溶液X,由K+、NH4+、Ba2+、Al3+、Fe3+、CO32-、SO42-中的若干种离子组成,取该溶液进行如下实验:

①白色沉淀甲是
②试写出实验过程中生成气体B的离子方程式
③通过上述实验,可确定X溶液中一定存在的离子是
您最近一年使用:0次



