解题方法
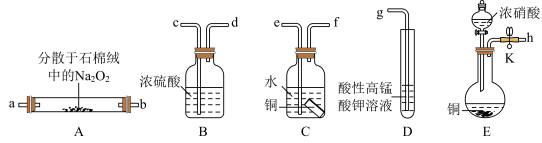
1 . 亚硝酸钠(NaNO2)外观酷似食盐且有成味,是一种常用防腐剂。某化学兴趣小组设计如图所示装置(省略夹持装置)制备NaNO2并探究其性质。
已知:①2NO+Na2O2=2NaNO2;
②NaNO2易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ;
;
③HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O。
回答下列问题:
(1)装置E中盛放铜片仪器名称是_______ ,其中发生反应的化学方程式_______ ,为检查E装置气密性的方法是_______ 。
(2)上述实验装置中,依次连接的合理顺序为h→_______ →bcdg。
(3)装置D中酸性KMnO4溶液的作用是_______ (用离子方程式表示)。
(4)装置C中水的作用是_______ 。
(5)根据题中信息,设计实验方案,用简单的方法区别亚硝酸钠和氯化钠两种固体_______ (写出操作、现象、结论)。

已知:①2NO+Na2O2=2NaNO2;
②NaNO2易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
 ;
;③HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O。
回答下列问题:
(1)装置E中盛放铜片仪器名称是
(2)上述实验装置中,依次连接的合理顺序为h→
(3)装置D中酸性KMnO4溶液的作用是
(4)装置C中水的作用是
(5)根据题中信息,设计实验方案,用简单的方法区别亚硝酸钠和氯化钠两种固体
您最近一年使用:0次
解题方法
2 . 根据所学知识回答下列问题:
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有_______ ,发生反应的化学方程式为_______
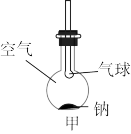
(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是_______
②能证明钠的熔点低的现象是_______
③能证明有氢氧化钠生成的现象是_______
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:_______ ,该反应中被还原的元素是_______ (填元素符号),氧化产物是_______ (填化学式)。
(1)将一小块新切的金属钠迅速放入平底烧瓶底部,按图甲所示塞紧瓶塞。过一段时间后可观察到的现象有

(2)按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。

①能证明钠的密度比水的小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
(3)向Na2O2中滴加浓盐酸,试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
3 . 为了探究过氧化钠的强氧化性,某小组设计了如图所示的实验装置。实验步骤及现象如图:
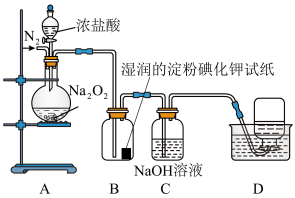
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N2,直至装置中气体变为无色。
回答下列问题:
(1)装置A中盛装浓盐酸的仪器是____ 。
(2)装置C的作用是____ 。
(3)装置D中收集到的无色气体能使带火星的木条复燃,解释产生该气体的原因是____ (用化学方程式表示)。
(4)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学根据A中气体的颜色推测试纸变蓝时发生的反应可能是____ (写离子方程式)。

①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N2,直至装置中气体变为无色。
回答下列问题:
(1)装置A中盛装浓盐酸的仪器是
(2)装置C的作用是
(3)装置D中收集到的无色气体能使带火星的木条复燃,解释产生该气体的原因是
(4)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学根据A中气体的颜色推测试纸变蓝时发生的反应可能是
您最近一年使用:0次
4 . 某同学想通过如图装置实验,探究SO2与Na2O2反应的产物。
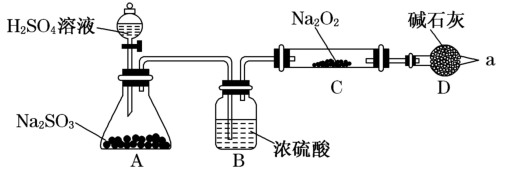
(1)检验反应中是否有O2生成的方法是____ ;若有O2生成,请写出装置C中的化学方程式____ 。
(2)A中盛装H2SO4溶液的仪器名称是____ ;D装置除起了防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应作用外,还可以____ 。
(3)①C中固体产物可能只有Na2SO3、只有____ 、Na2SO3和Na2SO4两种都有。
②若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如表,请您利用限选试剂和仪器帮助他完成该探究过程。
限选试剂和仪器:0.1mol•L-1KMnO4酸性溶液、0.01mol•L-1KMnO4酸性溶液、0.1mol•L-1Ba(NO3)2溶液、0.1mol•L-1BaCl2、1mol•L-1HNO3溶液、1mol•L-1盐酸、试管、胶头滴管。

(1)检验反应中是否有O2生成的方法是
(2)A中盛装H2SO4溶液的仪器名称是
(3)①C中固体产物可能只有Na2SO3、只有
②若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如表,请您利用限选试剂和仪器帮助他完成该探究过程。
限选试剂和仪器:0.1mol•L-1KMnO4酸性溶液、0.01mol•L-1KMnO4酸性溶液、0.1mol•L-1Ba(NO3)2溶液、0.1mol•L-1BaCl2、1mol•L-1HNO3溶液、1mol•L-1盐酸、试管、胶头滴管。
| 实验操作 | 预期现象和结论 |
| 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水、搅拌溶解,分别取少量于A、B试管中 | 固体完全溶解,得到无色透明溶液 |
| 步骤二:取试管A,向溶液中加入 | 若 |
| 步骤三:取试管B,向其中先加入 | 产生 |
您最近一年使用:0次
名校
5 . 化学实验是研究物质组成和探究物质性质的重要途径。
I.某澄清透明溶液(忽略水的电离),可能含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示:

请你根据上述实验推断:
(1)实验③产生的无色无味气体为_______ 、白色沉淀为_______ 。(填物质化学式)
(2)原溶液中一定存在的离子有_______ ,一定不存在的离子有_______ 。
(3)向该溶液中加入硫酸酸化,再通入 气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式(已知该反应中氧化剂和还原剂的个数比为2∶5):
气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式(已知该反应中氧化剂和还原剂的个数比为2∶5):_______ 。
II. 具有强氧化性,
具有强氧化性, 具有还原性,某同学根据氧化还原反应的知识推测
具有还原性,某同学根据氧化还原反应的知识推测 与
与 能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A中用锌和稀盐酸制取氢气。
能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A中用锌和稀盐酸制取氢气。

(4)装置B的名称_______ ,作用是_______ 。
(5)下面是实验过程中的重要操作,正确的顺序是_______。
(6)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出 与
与 反应生成的产物为
反应生成的产物为_______ 。
I.某澄清透明溶液(忽略水的电离),可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示:
请你根据上述实验推断:
(1)实验③产生的无色无味气体为
(2)原溶液中一定存在的离子有
(3)向该溶液中加入硫酸酸化,再通入
 气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式(已知该反应中氧化剂和还原剂的个数比为2∶5):
气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式(已知该反应中氧化剂和还原剂的个数比为2∶5):II.
 具有强氧化性,
具有强氧化性, 具有还原性,某同学根据氧化还原反应的知识推测
具有还原性,某同学根据氧化还原反应的知识推测 与
与 能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A中用锌和稀盐酸制取氢气。
能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A中用锌和稀盐酸制取氢气。
(4)装置B的名称
(5)下面是实验过程中的重要操作,正确的顺序是_______。
A.加热至 逐渐熔化,反应一段时间 逐渐熔化,反应一段时间 | B.用小试管收集气体并检验其纯度 |
C.打开 、 、 ,通入氢气 ,通入氢气 | D.停止加热,充分冷却,关闭 、 、 |
 与
与 反应生成的产物为
反应生成的产物为
您最近一年使用:0次
2022-10-12更新
|
590次组卷
|
3卷引用:辽宁省实验中学2022-2023学年高一上学期10月月考化学试题
6 . 在实验室中,用如下图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入②中,则预测的现象正确的是


| 选项 | ①中的物质 | ②中的物质 | 预测②中的现象 |
| A | 酚酞溶液 | 过氧化钠 | 溶液始终为红色 |
| B | 稀硫酸 | 苏打溶液 | 立即产生气泡 |
| C | 浓盐酸 | 二氧化锰 | 产生黄绿色气体 |
| D | 浓氨水 | 氯化银 | 固体溶解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-24更新
|
455次组卷
|
2卷引用:辽宁省协作体2021-2022学年下学期高三第一次模拟考试化学试题
名校
7 . 某研究性学习小组的同学在学习了 与过氧化钠的反应后,对过钒化钠与
与过氧化钠的反应后,对过钒化钠与 的反应进行实验探究。
的反应进行实验探究。
Ⅰ.提出假设:
假设1:固体产物是 ;
;
(1)假设2:_________ ;
假设3:固体产物是 和
和 的混合物。
的混合物。
Ⅱ.实验验证:用如图所示的装置(图中夹持仪器已略去)对上述假设进行实验。
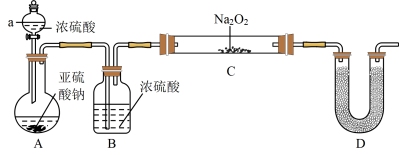
(2)装置A中发生反应的化学方程式为_________ 。
(3)装置B的作用是_________ ;装置D中试剂的名称为________ 。
(4)装置C中固体完全反应后,得到白色固体,为了对 与
与 的反应产物进行实验探究,做如下实验。
的反应产物进行实验探究,做如下实验。
通过实验探究发现.上述两个实验现象均有,则说明假设3正确。
 与过氧化钠的反应后,对过钒化钠与
与过氧化钠的反应后,对过钒化钠与 的反应进行实验探究。
的反应进行实验探究。Ⅰ.提出假设:
假设1:固体产物是
 ;
;(1)假设2:
假设3:固体产物是
 和
和 的混合物。
的混合物。Ⅱ.实验验证:用如图所示的装置(图中夹持仪器已略去)对上述假设进行实验。

(2)装置A中发生反应的化学方程式为
(3)装置B的作用是
(4)装置C中固体完全反应后,得到白色固体,为了对
 与
与 的反应产物进行实验探究,做如下实验。
的反应产物进行实验探究,做如下实验。| 实验操作 | 预期现象与结论 |
| 步骤1.取少量白色固体于试管中,加入足量的稀盐酸,将生成的气体通入品红溶液。 | 若出现 |
| 步骤2.在步骤1反应后的溶液中加入 | 若出现 |
您最近一年使用:0次
8 . Na2O2具有强氧化性,可以用来漂白纺织类物品、麦秆、羽毛等,也可做呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:
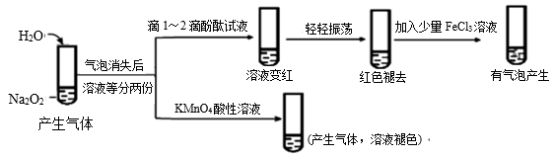
①依据实验现象推测红色褪去的原因是_________________ 。
②加入FeCl3反应的化学方程式为________________________ 。
③用离子方程式解释加入高锰酸钾溶液褪色的原因___________________ 。
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO2,将带余烬的木条插入试管C中,木条复燃。
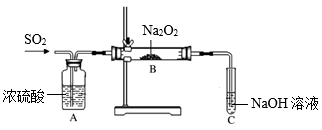
请回答下列问题:
①甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,检验有Na2SO3生成的实验方法是___________ 。
②乙同学认为反应的后B中有Na2SO3还会有Na2SO4。乙同学猜想的理由是__________ 。
③为检验产物中Na2SO4的存在,乙同学设计并实施了如下实验方案:
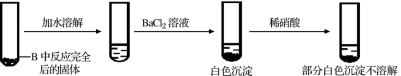
甲同学认为该实验方案的现象不能证明有Na2SO4生成,用反应方程式解释其原因_______ ;改进的方法为______________________ 。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:

①依据实验现象推测红色褪去的原因是
②加入FeCl3反应的化学方程式为
③用离子方程式解释加入高锰酸钾溶液褪色的原因
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO2,将带余烬的木条插入试管C中,木条复燃。

请回答下列问题:
①甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,检验有Na2SO3生成的实验方法是
②乙同学认为反应的后B中有Na2SO3还会有Na2SO4。乙同学猜想的理由是
③为检验产物中Na2SO4的存在,乙同学设计并实施了如下实验方案:

甲同学认为该实验方案的现象不能证明有Na2SO4生成,用反应方程式解释其原因
您最近一年使用:0次
2021-01-16更新
|
358次组卷
|
3卷引用:山西省临汾市2022-2023学年高一上学期9月月考化学试题
山西省临汾市2022-2023学年高一上学期9月月考化学试题河南省新蔡县2021届高三上学期期末调研考试化学试题(已下线)第06讲 钠及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
名校
9 . 利用以下装置制备、纯化CO,并探究CO和Na2O2的反应(CO+Na2O2=Na2CO3)。下列说法正确的是
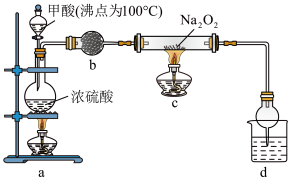

| A.装置b中的试剂可选用无水CaCl2 |
| B.装置d中的试剂可选用NaOH溶液 |
| C.实验开始时,依次点燃a、c处酒精灯 |
| D.加热一段时间后,硬质玻璃管中粉末由白色变为淡黄色 |
您最近一年使用:0次
2022-11-26更新
|
347次组卷
|
4卷引用:广东省广州市2022-2023学年高三上学期11月调研测试化学试题
2017·江西·一模
名校
10 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
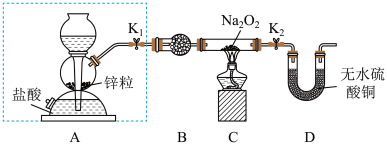
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________ 。
(2)B装置中所盛放的试剂是_____ ,其作用是_______ 。
(3)步骤3中的必要操作为打开K1、K2,_______ (请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________ 。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____ 。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____ (填“偏大”“偏小”或“不变”)
I.实验探究

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:
(2)B装置中所盛放的试剂是
(3)步骤3中的必要操作为打开K1、K2,
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
2017-10-30更新
|
1131次组卷
|
9卷引用:第06讲 钠及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)
(已下线)第06讲 钠及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)江西省百所名校2018届高三第一次联合考试化学试题湖南省衡阳市第八中学2017-2018学年高一(理科实验班)上学期第一次月考理综化学试题河北省承德市各县第一中学2018届高三上学期期末考试化学试题山西省大同市2020届高三第一次联合考试(县区)化学试题(已下线)第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测河北省廊坊市2018-2019学年高二下学期期末考试化学试题甘肃省天水市第一中学2021届高三上学期第一学段考试化学试题(已下线)第1讲 钠及其重要化合物



