名校
解题方法
1 . Na2CO3和NaHCO3是两种常见的钠盐。
(1)某小组研究Na2CO3和NaHCO3的性质,实验如下。
①室温下,Na2CO3的溶解度大于NaHCO3的实验证据是________________________ 。
②根据两试管中的温度变化情况,可得出的结论是_______________ 。
③该实验不能说明Na2CO3溶液的碱性强于NaHCO3溶液,理由是_____________ 。
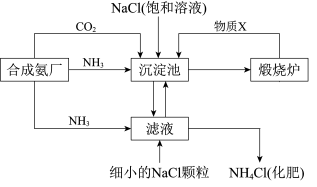
(2)
资料:
i.沉淀池中的反应为NaCl+CO2+NH3+H2O = NaHCO3↓+NH4Cl
ii.溶解度
①煅烧炉中反应的化学方程式是______________ ,物质X是_______ (填化学式)。
②下列说法正确的是________ (填字母)。
A.沉淀池中有NaHCO3析出,因为一定条件下NaHCO3的溶解度最小
B.滤液中主要含有NaCl、Na2CO3和NH4Cl
C.设计循环的目的是提高原料的利用率
③工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与Cl2反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是____________________________________________ 。
(1)某小组研究Na2CO3和NaHCO3的性质,实验如下。
| 序号 | 操作 | Na2CO3 | NaHCO3 |
| I | 在两支试管中加入1g Na2CO3或1g NaHCO3,再加入5mL水,振荡;将温度计分别插入其中。 | 温度由17.6℃变为23.2℃,放置到室温时,试管内无固体 | 温度由17.6℃变为17.2℃,放置到室温时,试管内有少量固体残留 |
| Ⅱ | 室温时,分别向I所得溶液中滴入2滴酚酞溶液 | 溶液变红 | 溶液微红 |
②根据两试管中的温度变化情况,可得出的结论是
③该实验不能说明Na2CO3溶液的碱性强于NaHCO3溶液,理由是
(2)

资料:
i.沉淀池中的反应为NaCl+CO2+NH3+H2O = NaHCO3↓+NH4Cl
ii.溶解度
| 物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 20℃溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
②下列说法正确的是
A.沉淀池中有NaHCO3析出,因为一定条件下NaHCO3的溶解度最小
B.滤液中主要含有NaCl、Na2CO3和NH4Cl
C.设计循环的目的是提高原料的利用率
③工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与Cl2反应可制得一种在生产生活中常用于漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
2 . 下列对应关系不正确 的是
| A | B | C | D |
| 碳酸氢钠 | 碳酸钠 | 氢氧化钙 | 氢氧化钠 |
| 苏打 | 纯碱 | 熟石灰 | 烧碱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-02更新
|
66次组卷
|
3卷引用:北京市育才学校2023-2024学年高一上学期期中考试化学试题
名校
3 . 补齐物质与其用途之间的连线______ 。
| 物质 用途 A.二氧化氯  a.调味品 a.调味品B.氯化钠 b.焙制糕点 C.碳酸氢钠 c.自来水消毒 |
您最近一年使用:0次
名校
解题方法
4 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)金属与水的反应
①Na的原子结构示意图是___________ 。
②钠与水反应的化学方程式是___________ 。
③钠与水的反应放出热量的现象是___________ 。
④钠、镁与水均能反应,通过比较反应的难易程度,可知钠的金属性强于镁。
(2)钠、钾失火时,可用不同的灭火剂灭火。如金属钠失火,可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因___________ 。
(3)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3的说法中,正确的是___________ (填字母)。
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
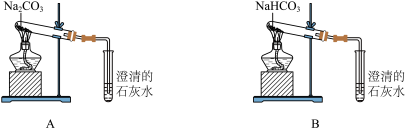
(4)按下图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是________ 。
(1)金属与水的反应

①Na的原子结构示意图是
②钠与水反应的化学方程式是
③钠与水的反应放出热量的现象是
④钠、镁与水均能反应,通过比较反应的难易程度,可知钠的金属性强于镁。
(2)钠、钾失火时,可用不同的灭火剂灭火。如金属钠失火,可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因
(3)Na2CO3和NaHCO3是两种常见的钠盐。下列关于Na2CO3和NaHCO3的说法中,正确的是
a.Na2CO3和NaHCO3的溶液均显碱性
b.相同温度下,NaHCO3的溶解度大于Na2CO3
c.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
(4)按下图所示装置实验,可得到“Na2CO3的热稳定性比NaHCO3强”的结论,证据是

您最近一年使用:0次
名校
解题方法
5 . 碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式_______ ,俗称_______ ,其水溶液显_______ (填“酸”、“碱”或“中”)性。
(2)碳酸氢钠与盐酸反应的离子方程式为_______ 。等质量的碳酸钠和碳酸氢钠与足量盐酸反应时剧烈程度,前者_______ 后者(填“>”、“<”或“=”)。
(1)碳酸氢钠的化学式
(2)碳酸氢钠与盐酸反应的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . A、B、C、D四种化合物均由前三周期元素组成,其中A含有四种元素,A、B、C的焰色反应均为黄色,D为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。

请回答:
(1)反应①的化学方程式为___________ 。
(2)反应②的离子方程式为___________ 。
(3)向B溶液中加入熟石灰可制烧碱,该反应的化学方程式为___________ 。
(4)A含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体,该气体能使带余烬的木条复燃。

反应Ⅱ中发生反应的化学方程式为___________ 。

请回答:
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)向B溶液中加入熟石灰可制烧碱,该反应的化学方程式为
(4)A含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体,该气体能使带余烬的木条复燃。

反应Ⅱ中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 下列关于钠的化合物的叙述不正确的是
| A.碳酸钠俗称纯碱,水溶液显碱性 |
B. 中阴、阳离子的个数比为1:2 中阴、阳离子的个数比为1:2 |
C.热稳定性: |
D. 与 与 都能和水反应生成碱,它们都是碱性氧化物 都能和水反应生成碱,它们都是碱性氧化物 |
您最近一年使用:0次
8 . 下列物质性质与用途的对应关系不正确 的是
选项 | 性质 | 用途 |
A | 次氯酸有强氧化性 | 用作漂白剂 |
B | 小苏打有碱性 | 用作抗酸药物 |
C | 氯化钠具有碱性 | 用于制造氢氧化钠 |
D | 硫酸有酸性 | 用于金属加工前的酸洗除锈 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列解释实验现象的反应方程式正确的是
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗: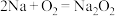 |
B.84消毒液(主要成分:NaClO)与洁厕灵(主要成分:HCl)混用产生 : : |
C. 在潮湿的空气中放置一段时间,变成白色粘稠物: 在潮湿的空气中放置一段时间,变成白色粘稠物: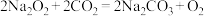 |
D.向 溶液中加入过量的澄清石灰水,出现白色沉淀: 溶液中加入过量的澄清石灰水,出现白色沉淀: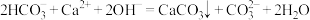 |
您最近一年使用:0次
名校
10 . 实验小组探究Na2CO3和NaHCO3的性质
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
【分析与解释】
(1)实验Ⅰ中,溶解时吸收热量的物质是___________ 。
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式___________ ,OH-未参与该反应的实验依据是___________ 。
(3)实验Ⅱ中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有___________ 。
(4)实验Ⅲ中,能够证明Na2CO3的热稳定性强于NaHCO3的证据是___________ ,请用化学方程式解释现象的差异___________ 。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验Ⅰ | 测量下述实验过程的温度变化 |  |
| 实验Ⅱ | 测量下述实验过程的pH变化 | 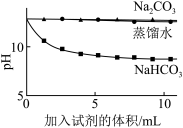 |
| 实验Ⅲ |  |
(1)实验Ⅰ中,溶解时吸收热量的物质是
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式
(3)实验Ⅱ中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有
(4)实验Ⅲ中,能够证明Na2CO3的热稳定性强于NaHCO3的证据是
您最近一年使用:0次



