解题方法
1 . 化学在生产、生活中有着重要用途,下列物质的用途或成分正确的有
①过氧化钠可作潜水艇供氧剂②铁红常用作红色油漆③ 可制造耐火材料④
可制造耐火材料④ 水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
①过氧化钠可作潜水艇供氧剂②铁红常用作红色油漆③
 可制造耐火材料④
可制造耐火材料④ 水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药
水溶液俗称水玻璃可用作木材防火剂⑤硅单质可用作计算机芯片⑥二氧化硅可用作光导纤维⑦明矾可用于净水⑧青铜主要成分是铜锌合金⑨小苏打可作发酵粉⑩烧碱可用作治疗胃酸过多的药| A.7个 | B.8个 | C.9个 | D.10个 |
您最近半年使用:0次
2 . 下列有关Na2CO3和NaHCO3的性质,叙述错误的是
A.鉴别Na2CO3和NaHCO3可以用BaCl2溶液,不可用 溶液 溶液 |
| B.Na2CO3比NaHCO3更稳定 |
| C.NaHCO3可以用于泡沫灭火器的反应物质 |
| D.除去NaHCO3溶液中混有的少量Na2CO3,用加热法 |
您最近半年使用:0次
名校
解题方法
3 . 下列离子方程式书写错误的是
| A.石灰石与稀盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.过氧化钠与稀硫酸反应:2Na2O2+4H+=4Na++O2↑+2H2O |
C.澄清石灰水与过量碳酸氢钠溶液反应:Ca2++2HCO +2OH﹣=CaCO3↓+CO +2OH﹣=CaCO3↓+CO +2H2O +2H2O |
D.氢氧化钡溶液中滴加稀硫酸:Ba2++OH﹣+H++SO =BaSO4↓+H2O =BaSO4↓+H2O |
您最近半年使用:0次
名校
4 . 下列有关物质性质和用途的说法中错误的是
| A.ClO2除了杀菌、消毒外,还广泛地用于环保、灭藻、漂白、保鲜、除臭等方面 |
| B.小苏打是焙制糕点所用的发酵粉主要成分之一 |
| C.Fe2O3是红棕色粉末,常用作油漆、涂料、油墨的红色颜料 |
| D.红酒中添加SO2做抗氧化剂,是因为SO2具有氧化性 |
您最近半年使用:0次
名校
5 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
A. 溶液( 溶液( ):通入过量的 ):通入过量的 |
B.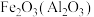 :加入NaOH溶液再过滤 :加入NaOH溶液再过滤 |
C. 溶液( 溶液( ):加入足量铁粉再过滤 ):加入足量铁粉再过滤 |
D.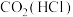 :将气体通过盛有饱和 :将气体通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
您最近半年使用:0次
名校
解题方法
6 . 某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为___________ 。
(2)称取两种固体各2g,分别加入烧杯甲、乙中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①烧杯甲中的固体完全溶解,而烧杯乙中的固体有剩余,由此得出结论:___________ 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是
的烧杯中出现的现象是___________ (填字母序号)。
a.溶液温度升高 b.溶液温度下降 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
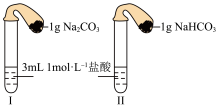
①两试管中均产生气体,___________ 的反应程度更为剧烈。(填“I”或“Ⅱ”)
②反应结束后,恢复至室温,下列说法正确的是___________ 。
a.装置I的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作1的现象与预测有差异:产生白色沉淀和二氧化碳气体。则该条件下, 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
(2)称取两种固体各2g,分别加入烧杯甲、乙中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①烧杯甲中的固体完全溶解,而烧杯乙中的固体有剩余,由此得出结论:
②同学们在两烧杯中还观察到以下现象。其中,盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度升高 b.溶液温度下降 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,恢复至室温,下列说法正确的是
a.装置I的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成
 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向2mL 溶液中滴加1mL 溶液中滴加1mL  溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
操作2:向2mL 溶液中滴加1mL 溶液中滴加1mL  溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近半年使用:0次
名校
解题方法
7 . Ⅰ. 和
和 是两种常见的钠盐。
是两种常见的钠盐。
向 和
和 的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
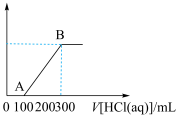
(1)OA段发生反应的离子方程式:________ 。
(2)原溶液中碳酸钠和碳酸氢钠的物质的量之比为_______ 。
Ⅱ.实验室中需0.2 mol/L的 溶液80 mL,请回答下列问题。
溶液80 mL,请回答下列问题。
(3)配制上述溶液所需的玻璃 仪器有:玻璃棒、烧杯和______ ,用托盘天平称取 固体,其质量是
固体,其质量是_______ g。
(4)实验时下图所示操作的先后顺序为______ (填编号)。
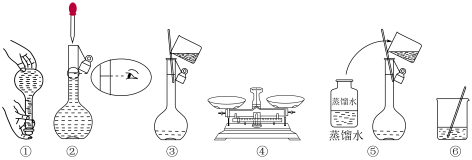
(5)取用任意体积的该 溶液时,下列物理量不随所取体积的多少而变化的是
溶液时,下列物理量不随所取体积的多少而变化的是______ 。
a.溶液中 的物质的量 b.溶液的浓度
的物质的量 b.溶液的浓度
c.溶液中 的数目 d.溶液的密度
的数目 d.溶液的密度
(6)下列操作中,会造成溶液浓度有何变化(填偏高,偏低,无影响)。
①定容时,俯视刻度线________ 。
②没有洗涤烧杯和玻璃棒_______ 。
③配制前容量瓶中残留少量蒸馏水______ 。
④摇匀后,发现液面低于刻度线_______ 。
⑤用天平称量时, 和砝码位置放颠倒了
和砝码位置放颠倒了_____ 。
⑥未冷却至室温就开始定容________ 。
(7)若需要0.05mol/L的 ,可用量筒量取
,可用量筒量取____ mL所配 溶液。
溶液。
 和
和 是两种常见的钠盐。
是两种常见的钠盐。向
 和
和 的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
(1)OA段发生反应的离子方程式:
(2)原溶液中碳酸钠和碳酸氢钠的物质的量之比为
Ⅱ.实验室中需0.2 mol/L的
 溶液80 mL,请回答下列问题。
溶液80 mL,请回答下列问题。(3)配制上述溶液所需的
 固体,其质量是
固体,其质量是(4)实验时下图所示操作的先后顺序为

(5)取用任意体积的该
 溶液时,下列物理量不随所取体积的多少而变化的是
溶液时,下列物理量不随所取体积的多少而变化的是a.溶液中
 的物质的量 b.溶液的浓度
的物质的量 b.溶液的浓度c.溶液中
 的数目 d.溶液的密度
的数目 d.溶液的密度(6)下列操作中,会造成溶液浓度有何变化(填偏高,偏低,无影响)。
①定容时,俯视刻度线
②没有洗涤烧杯和玻璃棒
③配制前容量瓶中残留少量蒸馏水
④摇匀后,发现液面低于刻度线
⑤用天平称量时,
 和砝码位置放颠倒了
和砝码位置放颠倒了⑥未冷却至室温就开始定容
(7)若需要0.05mol/L的
 ,可用量筒量取
,可用量筒量取 溶液。
溶液。
您最近半年使用:0次
2024-02-14更新
|
63次组卷
|
2卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一上学期1月期末化学试题
名校
8 . 下列物质的俗名与化学成份一致的是
| A.碱石灰-CaO | B.重晶石-CaSO4 |
| C.熟石膏-2CaSO4•H2O | D.王水-V(浓盐酸):V(浓硝酸)=1:3 |
您最近半年使用:0次
名校
解题方法
9 . 下列有关NaHCO3、Na2CO3的性质比较中,正确的是
| A.热稳定性Na2CO3<NaHCO3,常温时水溶性Na2CO3<NaHCO3 |
| B.溶于水时,Na2CO3有吸热现象,NaHCO3有放热现象。 |
| C.可用BaCl2溶液区分NaHCO3固体和Na2CO3固体 |
| D.等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多 |
您最近半年使用:0次
2024-01-18更新
|
217次组卷
|
3卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
10 . 为除去括号内的杂质,下列各选项中所选用的试剂或方法错误的是
A. 固体( 固体( ):加热 ):加热 |
B.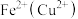 :加入过量NaOH后过滤 :加入过量NaOH后过滤 |
C.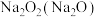 :将混合物在氧气中加热 :将混合物在氧气中加热 |
| D.Mg固体(Al):加入足量的NaOH溶液,过滤 |
您最近半年使用:0次
2024-01-17更新
|
136次组卷
|
4卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高一上学期1月期末化学试题



