名校
1 . I.实验室需要480 mL0.2mol•L-1Na2CO3溶液。
(1)除烧杯和玻璃棒、胶头滴管外,还需要的玻璃仪器有______ 。
(2)用Na2CO3•10H2O固体配置,所需固体的质量______ 。
(3)下列错误操作可使所配制碳酸钠溶液浓度偏低的是______。
II.我国化工专家侯德榜对索尔维制碱法进行了改进,将合成氨工业与纯碱工业联合,发明了联合制碱法,实验室模拟工业上联合制碱法原理制备纯碱
(4)如图1操作未涉及的是______。
生产流程可简要表示如图2:
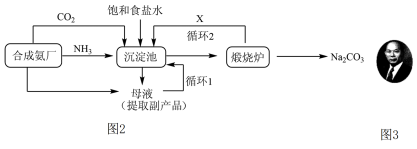
(5)沉淀池中总反应的化学方程式为______ 。
(6)ag含碳酸氢钠杂质的碳酸钠,充分加热至固体质量保持不变,所得固体的质量为bg,用字母表示碳酸氢钠的质量分数______ 。
(1)除烧杯和玻璃棒、胶头滴管外,还需要的玻璃仪器有
(2)用Na2CO3•10H2O固体配置,所需固体的质量
(3)下列错误操作可使所配制碳酸钠溶液浓度偏低的是______。
| A.容量瓶洗净后残留了部分的水 |
| B.转移时溶液溅到容量瓶外面 |
| C.定容时俯视容量瓶的刻度线 |
| D.摇匀后见液面下降,再加水至刻度线 |
II.我国化工专家侯德榜对索尔维制碱法进行了改进,将合成氨工业与纯碱工业联合,发明了联合制碱法,实验室模拟工业上联合制碱法原理制备纯碱
(4)如图1操作未涉及的是______。
A.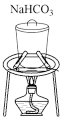 | B.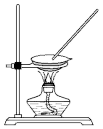 | C. | D. |
生产流程可简要表示如图2:

(5)沉淀池中总反应的化学方程式为
(6)ag含碳酸氢钠杂质的碳酸钠,充分加热至固体质量保持不变,所得固体的质量为bg,用字母表示碳酸氢钠的质量分数
您最近一年使用:0次
名校
解题方法
2 . 以下四个实验中,实验装置符合规范且能达到实验目的有
| 装置 | 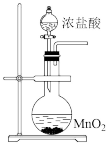 |  |
| 目的 | 制取氯气的发生装置 | 鉴别等物质的量浓度的NaHCO3和Na2CO3溶液 |
| 装置 | 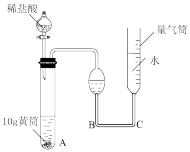 | 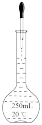 |
| 目的 | 测定黄铜(铜锌合金)中铜的质量分数 | 定容 |
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
名校
解题方法
3 . 以下各组除杂试剂的选择和实验操作均正确的是
| 选项 | 物质(括号内为杂质) | 除杂操作 |
| A | FeCl3溶液(FeCl2) | 加入铁粉充分反应后过滤 |
| B | CO2 (HCl) | 气体依次通过盛有饱和NaCl溶液、浓硫酸的洗气瓶 |
| C | NaHCO3溶液(Na2CO3) | 加热 |
| D | Fe2O3(Al2O3) | 加入过量氢氧化钠,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列生活中的物质与其有效成分的化学式用途的对应关系中,不正确的是
| 选项 | A | B | C | D |
| 生活中的物质 | 不锈钢 | 漂白粉 | 小苏打 | 复方氢氧化铝片 |
| 有效成分 | Fe、Cr、Ni | Ca(ClO)2 | Na2CO3 | Al(OH)3 |
| 用途 | 医疗器械及餐具 | 做消毒剂 | 做发酵粉 | 做抗酸药 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 侯德榜是我国近代化学工业奠基人之一,为我国化工事业发展做出了卓越贡献,侯氏制碱享誉国际,侯氏制碱法使用的主要原料是食盐、氨、二氧化碳,如图是模拟“侯氏制碱法”制取 的部分装置(已知:氨气水溶液呈碱性,1体积水能溶解700体积氨气)。下列操作正确的是
的部分装置(已知:氨气水溶液呈碱性,1体积水能溶解700体积氨气)。下列操作正确的是

 的部分装置(已知:氨气水溶液呈碱性,1体积水能溶解700体积氨气)。下列操作正确的是
的部分装置(已知:氨气水溶液呈碱性,1体积水能溶解700体积氨气)。下列操作正确的是
A.b通入 ,然后a通入 ,然后a通入 ,c中放蘸NaOH的脱脂棉 ,c中放蘸NaOH的脱脂棉 |
B.a通入 ,然后b通入 ,然后b通入 ,c中放蘸稀硫酸的脱脂棉 ,c中放蘸稀硫酸的脱脂棉 |
C.a通入 ,然后b通入 ,然后b通入 ,c中放氧化钙 ,c中放氧化钙 |
D.b通入 ,然后a通入 ,然后a通入 ,c中放碱石灰 ,c中放碱石灰 |
您最近一年使用:0次
名校
解题方法
6 . 下列除去物质中含少量杂质的方法正确的是
| 选项 | 物质(括号内为杂质) | 实验方法 |
| A |  | 加入足量铁粉,过滤 |
| B |  溶液 溶液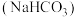 | 加热 |
| C | 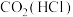 | 通入烧碱溶液充分反应 |
| D | 铝粉(铁粉) | 加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 许多化学物质在日常生活中有俗名。下列物质的俗名与化学式对应正确的是
A.纯碱— | B.小苏打—NaOH |
C.干冰— | D.胆矾— |
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、W四种常见化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去):

请回答:
(1)画出X、Y、Z中焰色试验呈黄色的元素原子结构示意图_______ ,W的名称是_______ 。
(2)X与Y在溶液中反应的离子方程式是_______ 。
(3)①将132克W通入到含160克Y的的水溶液中,该反应的总离子方程式为_______ 。
②自然界中存在X、Z和H2O按一定比例结晶而成的固体。取m克该固体测得所含金属阳离子的质量为1.15克, 若取相同质量的固体加热至恒重,剩余固体的质量为_______ g。
(4)Ⅰ和Ⅱ中为X所含有的四种元素中的两种或三种组成的化合物,并利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色助燃性气体。

①装置Ⅱ中物质的化学式是_______ 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集干燥的装置Ⅴ中气体,该化合物的化学式是_______ ,所需仪器装置是_______ (从上图选择必要装置,填写装置下方的编号)。

请回答:
(1)画出X、Y、Z中焰色试验呈黄色的元素原子结构示意图
(2)X与Y在溶液中反应的离子方程式是
(3)①将132克W通入到含160克Y的的水溶液中,该反应的总离子方程式为
②自然界中存在X、Z和H2O按一定比例结晶而成的固体。取m克该固体测得所含金属阳离子的质量为1.15克, 若取相同质量的固体加热至恒重,剩余固体的质量为
(4)Ⅰ和Ⅱ中为X所含有的四种元素中的两种或三种组成的化合物,并利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色助燃性气体。

①装置Ⅱ中物质的化学式是
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集干燥的装置Ⅴ中气体,该化合物的化学式是
您最近一年使用:0次
名校
解题方法
9 . 2011年是国际化学年,中国的宣传口号是“化学——我们的生活,我们的未来”。生活中处处有化学。钠是一种极活泼的金属,其化合物种类繁多,在生活中应用非常广泛,请回答下列问题:
(1)生理盐水的主要成分_______ (写化学式)。
(2)下列说法正确的是_______
a.将Na2O2投入紫色石蕊溶液中,溶液变蓝
b.Na2O2中阴、阳离子的个数比为1:2
c.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应时,产生CO2的个数相等
d.将一小块钠投入装有硫酸铜溶液的试管中,试管底部有红色物质生成
e.区别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
f.NaHCO3固体可以做干粉灭火剂,金属钠着火可以用它来灭火
g.NaHCO3粉末中混有Na2CO3杂质,可配制成溶液,然后通入过量的CO2,再降温结晶得NaHCO3固体
(3)纯碱属于_______ 类物质(填“酸”“碱”或“盐”,后同),其水溶液呈_______ 性。
(4)汽车安全气囊中气体发生剂主要成分是NaN3等物质,当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2↑。从氧化还原反应的角度分析该反应中Na是_______ 。
(1)生理盐水的主要成分
(2)下列说法正确的是
a.将Na2O2投入紫色石蕊溶液中,溶液变蓝
b.Na2O2中阴、阳离子的个数比为1:2
c.质量相等的NaHCO3与Na2CO3分别与足量盐酸完全反应时,产生CO2的个数相等
d.将一小块钠投入装有硫酸铜溶液的试管中,试管底部有红色物质生成
e.区别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液
f.NaHCO3固体可以做干粉灭火剂,金属钠着火可以用它来灭火
g.NaHCO3粉末中混有Na2CO3杂质,可配制成溶液,然后通入过量的CO2,再降温结晶得NaHCO3固体
(3)纯碱属于
(4)汽车安全气囊中气体发生剂主要成分是NaN3等物质,当汽车发生较严重的碰撞时,引发NaN3分解:2NaN3 = 2Na + 3N2↑。从氧化还原反应的角度分析该反应中Na是
您最近一年使用:0次
名校
解题方法
10 . 在溶液中能大量共存,加入OH﹣有沉淀析出,加入H+有气体放出的是
A.H+、Cu2+、Cl﹣、CO | B.Fe3+、K+、SO 、NO 、NO |
C.Ca2+、Al3+、MnO 、SO 、SO | D.Na+、Ba2+、Cl﹣、HCO |
您最近一年使用:0次



