解题方法
1 . 下列实验方案或实验结论不正确的是

A.装置①可以用于实验室制 | B.装置④可用于比较 和 和 的热稳定性 的热稳定性 |
C.装置③验证 与水反应的热量变化 与水反应的热量变化 | D.装置②可以用于除去 中混有的少量HCl 中混有的少量HCl |
您最近半年使用:0次
解题方法
2 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。
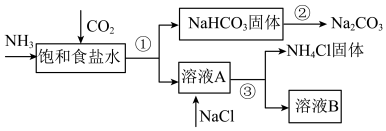
联合制碱法的主要流程如下(部分物质已略去):___________ (填序号)。
(2)纯碱属于___________ (填“酸”“碱”或“盐”)。
(3)根据上述流程图,将化学方程式补充完整:___________ 。
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通___________ (填“ ”或“
”或“ ”)。
”)。
(5)煅烧 固体的化学方程式是
固体的化学方程式是___________ 。
(6)下列联合制碱法流程说法正确的是___________ (填字母)。
a.副产物 可用作肥料
可用作肥料
b.溶液B中一定含有 、
、 、
、
c.①中 析出是因为
析出是因为 不溶于水
不溶于水
(7)②这个步骤生成的产物可以循环使用的是___________ (填化学式)。
联合制碱法的主要流程如下(部分物质已略去):
(2)纯碱属于
(3)根据上述流程图,将化学方程式补充完整:
 +___________+___________=___________↓+
+___________+___________=___________↓+
(4)向饱和食盐水中应先通
 ”或“
”或“ ”)。
”)。(5)煅烧
 固体的化学方程式是
固体的化学方程式是(6)下列联合制碱法流程说法正确的是
a.副产物
 可用作肥料
可用作肥料b.溶液B中一定含有
 、
、 、
、
c.①中
 析出是因为
析出是因为 不溶于水
不溶于水(7)②这个步骤生成的产物可以循环使用的是
您最近半年使用:0次
3 . 下列反应的离子方程式正确的是
A. 与过量的 与过量的 反应: 反应: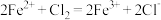 |
B.食醋去除水垢中的 : :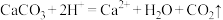 |
C.过量 通入饱和碳酸钠溶液: 通入饱和碳酸钠溶液: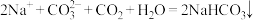 |
D. 溶液与 溶液与 溶液反应至溶液呈中性: 溶液反应至溶液呈中性: |
您最近半年使用:0次
2024-04-16更新
|
361次组卷
|
2卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
名校
4 . 回答下列问题
(1)过氧化钠与二氧化碳反应的化学方程式_____________ ,并用单线桥标出电子转移的方向和数目__________________ 。
(2)漂白粉的有效成分是______ (填化学式),制取漂白粉的化学方程式__________________ 。
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)__________________ ;__________________ 。
(4)实验室用 制氯气的离子方程式
制氯气的离子方程式_______________ 。
(5)将钠投入到 溶液中,写出化学方程式
溶液中,写出化学方程式______________ 。
(6)除去碳酸钠中混有的碳酸氢钠应加入______ (填化学式)溶液,涉及到的反应的离子方程式为__________________ 。
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式_________________ 。
(1)过氧化钠与二氧化碳反应的化学方程式
(2)漂白粉的有效成分是
(3)漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式)
(4)实验室用
 制氯气的离子方程式
制氯气的离子方程式(5)将钠投入到
 溶液中,写出化学方程式
溶液中,写出化学方程式(6)除去碳酸钠中混有的碳酸氢钠应加入
(7)厨房里常用小苏打做糕点的发泡剂,写出其受热分解的化学方程式
您最近半年使用:0次
名校
解题方法
5 . 下列有关 和
和 的性质比较正确的是
的性质比较正确的是
A.相同温度下,在水中的溶解性 |
B.相同温度下,等物质的量浓度的溶液中分别滴入酚酞,红色较深的是 |
C.1g碳酸钠和1g碳酸氢钠固体中分别加入几滴水后,测得温度较高的是 |
D.相同条件下,等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应产生 量较多的是Na2CO3 量较多的是Na2CO3 |
您最近半年使用:0次
名校
解题方法
6 . 化学与生活、科技密切相关。下列说法正确的是
| A.青运会参赛运动员剧烈运动后,需要及时补充的生理盐水是电解质 |
| B.硬铝是制造飞机和宇宙飞船的理想合金材料 |
| C.食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是防止食品氧化变质 |
| D.碳酸钠溶液呈碱性,是治疗胃酸过多的一种药剂 |
您最近半年使用:0次
名校
解题方法
7 . 碳酸钠是一种重要的无机化工原料,主要用于玻璃制品和陶瓷釉的生产,还广泛用于生活洗涤、酸类中和以及食品加工等。工业制碱法大致经历了如图所示的三个阶段。

Ⅰ.路布兰是开创化学工业的先驱者,路布兰制碱法是化工史上的一个里程碑。路布兰制碱法的反应原理如下:
①
②
③
(1)上述反应属于氧化还原反应的是_______ (填序号),该反应的还原产物为_______ (填化学式)。
(2)路布兰制碱法的缺点有_______ (写出一点即可)。
Ⅱ.1861年,比利时人欧内斯特·索尔维发明了以食盐、石灰石、氨气为原料制取碳酸钠的索尔维制碱法(又称氨碱法),其工业生产的简单流程如图所示。
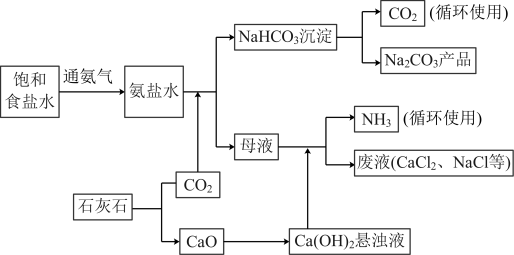
(3)上述流程涉及的物质中,属于酸性氧化物的是_______ (填化学式)。
(4)往饱和 溶液中持续通入
溶液中持续通入 ,写出其反应的离子方程式
,写出其反应的离子方程式_______ 。
Ⅲ.1943年左右我国著名科学家侯德榜先生克服困难,把合成氨工业和氨碱法制碱工业结合起来,发明了联合制碱法,也被人们称为“侯氏制碱法”,该方法大大提高了原料的利用率,其流程如图所示。

(5)已知氨气极易溶于水,该工艺中若先通入 后通入
后通入 和,可能造成的后果是
和,可能造成的后果是_______ 。
(6)煅烧时,发生反应的化学方程式为_______ 。
(7)提取的 产品中含有少量
产品中含有少量 ,将
,将 产品溶解,加入适量的稀盐酸和
产品溶解,加入适量的稀盐酸和 充分反应,煮沸、过滤、浓缩结晶,即可得到纯净的
充分反应,煮沸、过滤、浓缩结晶,即可得到纯净的 固体。加入稀盐酸和
固体。加入稀盐酸和 时发生反应的离子方程式为
时发生反应的离子方程式为_______ 。

Ⅰ.路布兰是开创化学工业的先驱者,路布兰制碱法是化工史上的一个里程碑。路布兰制碱法的反应原理如下:
①

②

③

(1)上述反应属于氧化还原反应的是
(2)路布兰制碱法的缺点有
Ⅱ.1861年,比利时人欧内斯特·索尔维发明了以食盐、石灰石、氨气为原料制取碳酸钠的索尔维制碱法(又称氨碱法),其工业生产的简单流程如图所示。

(3)上述流程涉及的物质中,属于酸性氧化物的是
(4)往饱和
 溶液中持续通入
溶液中持续通入 ,写出其反应的离子方程式
,写出其反应的离子方程式Ⅲ.1943年左右我国著名科学家侯德榜先生克服困难,把合成氨工业和氨碱法制碱工业结合起来,发明了联合制碱法,也被人们称为“侯氏制碱法”,该方法大大提高了原料的利用率,其流程如图所示。

(5)已知氨气极易溶于水,该工艺中若先通入
 后通入
后通入 和,可能造成的后果是
和,可能造成的后果是(6)煅烧时,发生反应的化学方程式为
(7)提取的
 产品中含有少量
产品中含有少量 ,将
,将 产品溶解,加入适量的稀盐酸和
产品溶解,加入适量的稀盐酸和 充分反应,煮沸、过滤、浓缩结晶,即可得到纯净的
充分反应,煮沸、过滤、浓缩结晶,即可得到纯净的 固体。加入稀盐酸和
固体。加入稀盐酸和 时发生反应的离子方程式为
时发生反应的离子方程式为
您最近半年使用:0次
2024-03-14更新
|
51次组卷
|
2卷引用:2024年广西南宁、柳州等地示范性高中高一下学期3月开学考调研测试 化学试题
8 . 已知 为一种常见的金属单质,B、C、D、E是含
为一种常见的金属单质,B、C、D、E是含 元素的常见化合物,它们的焰色均为黄色。根据下图的转化关系,回答下列问题。
元素的常见化合物,它们的焰色均为黄色。根据下图的转化关系,回答下列问题。
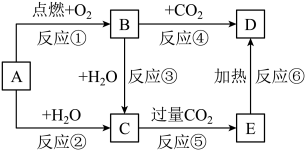
(1)写出下列物质的化学式:B________ ;C________ ;
(2)物质B的颜色为________ ;
(3)写出下列转化的化学方程式:
①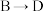 :
:________ ;
②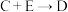 :
:________ ;
(4)写出 的离子方程式:
的离子方程式:________ ;
(5)加热 和
和 的固体混合物,使
的固体混合物,使 完全分解,固体混合物的质量减少了
完全分解,固体混合物的质量减少了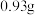 ,则混合物中
,则混合物中 的质量为
的质量为________ 。
 为一种常见的金属单质,B、C、D、E是含
为一种常见的金属单质,B、C、D、E是含 元素的常见化合物,它们的焰色均为黄色。根据下图的转化关系,回答下列问题。
元素的常见化合物,它们的焰色均为黄色。根据下图的转化关系,回答下列问题。
(1)写出下列物质的化学式:B
(2)物质B的颜色为
(3)写出下列转化的化学方程式:
①
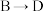 :
:②
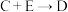 :
:(4)写出
 的离子方程式:
的离子方程式:(5)加热
 和
和 的固体混合物,使
的固体混合物,使 完全分解,固体混合物的质量减少了
完全分解,固体混合物的质量减少了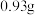 ,则混合物中
,则混合物中 的质量为
的质量为
您最近半年使用:0次
9 . 向下列溶液中分别逐滴加入 和
和 两种溶液,出现不同现象的是
两种溶液,出现不同现象的是
 和
和 两种溶液,出现不同现象的是
两种溶液,出现不同现象的是A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近半年使用:0次
名校
解题方法
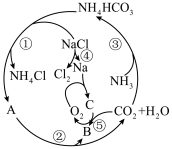
10 . 某些化合物具有如图所示的转化关系,其中A、B、C均为含有钠元素的化合物,部分转化的条件省略。 极易溶于水。
极易溶于水。
回答下列问题:
(1)A为___________ (填化学式,下同),B为___________ ,C为___________
(2) 的摩尔质量为
的摩尔质量为___________ ;要获得高浓度的 溶液,需向水中先通入
溶液,需向水中先通入___________ (填“ ”或“
”或“ ”)。
”)。
(3)反应④中氧化产物和还原产物的质量之比为___________ (填最简整数比);反应⑤中转移 电子时,生成
电子时,生成___________  (换算成标准状况下)
(换算成标准状况下) 。
。
(4)现有 由A、B形成的混合物,加入
由A、B形成的混合物,加入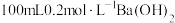 溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为
溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为 。
。
①配制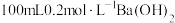 溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、
溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、___________ ;配制过程中,下列情况会导致配制结果偏低的是___________ 。(填标号)。
a.称量的 中含有少量
中含有少量
b.定容时未冷却至室温
c.定容时溶液超过刻度线,迅速用胶头滴管吸出多余液体
d.将配制好的溶液倒入试剂瓶中时有少量液体溅到试剂瓶外
② 原混合物中,A与B的物质的量之比
原混合物中,A与B的物质的量之比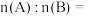
___________ (填最简整数比)。
 极易溶于水。
极易溶于水。回答下列问题:
(1)A为
(2)
 的摩尔质量为
的摩尔质量为 溶液,需向水中先通入
溶液,需向水中先通入 ”或“
”或“ ”)。
”)。(3)反应④中氧化产物和还原产物的质量之比为
 电子时,生成
电子时,生成 (换算成标准状况下)
(换算成标准状况下) 。
。(4)现有
 由A、B形成的混合物,加入
由A、B形成的混合物,加入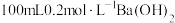 溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为
溶液(过量),充分反应后,过滤、洗涤、干燥,称量所得固体质量为 。
。①配制
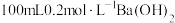 溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、
溶液需要的玻璃仪器有烧杯、量筒、玻璃棒、a.称量的
 中含有少量
中含有少量
b.定容时未冷却至室温
c.定容时溶液超过刻度线,迅速用胶头滴管吸出多余液体
d.将配制好的溶液倒入试剂瓶中时有少量液体溅到试剂瓶外
②
 原混合物中,A与B的物质的量之比
原混合物中,A与B的物质的量之比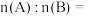
您最近半年使用:0次
2024-02-28更新
|
39次组卷
|
2卷引用:广西桂林市恭城瑶族自治县民族高级中学2023-2024学年高一下学期开学考试化学试题



