1 . 下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是
 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg |
| D.取ag混合物与足量澄清石灰水充分反应,所得沉淀经过滤、洗涤、干燥,得到bg固体 |
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
| D.取ag混合物与足量NaOH溶液充分反应,得到bg固体 |
您最近一年使用:0次
解题方法
3 . 化学与科学、技术、社会、生活、环境密切相关。下列有关说法中错误的是
| A.焰火中呈现的绚丽色彩,是金属元素焰色反应形成的 |
| B.医用生理盐水中氯化钠的质量分数为75% |
| C.小苏打既是制作糕点的膨松剂,又是治疗胃酸过多的一种药剂 |
| D.明矾净水利用了胶体的吸附作用 |
您最近一年使用:0次
名校
解题方法
4 . 某食品膨松剂起作用物质为NaHCO3,某兴趣小组研究加热情况下该膨松剂放出气体的量,设计实验的装置图如图。
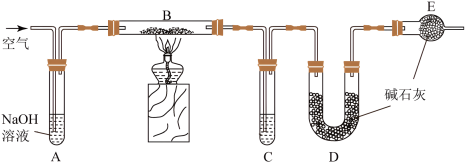
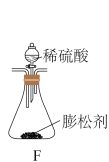
回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的_______ ,C装置内所盛试剂是_______ ,E装置的作用是_______ ,若没有E装置,测定的结果_______ (填“偏高”、“偏低”或“无影响”);若没有A装置,B装置左侧用橡皮塞封闭,实验结果将_______ (填“偏高”、“偏低”或“无影响”)。
(2)分解产物Na2CO3是重要化工原料,研究其性质:分别取少量Na2CO3溶液。
①与碱反应:滴加澄清石灰水,现象为_______ 。
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为_______ (写其中一种的名称)。
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式_______ 。
(3)取a克Na2CO3与NaHCO3混合物进行下列三组实验,其中能测定Na2CO3质量分数的是_______ (填序号)。
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
任选上述合理方案中的一种,计算Na2CO3的质量分数为_______ 。


回答下列问题:
(1)A装置中NaOH溶液的作用是除去空气中的
(2)分解产物Na2CO3是重要化工原料,研究其性质:分别取少量Na2CO3溶液。
①与碱反应:滴加澄清石灰水,现象为
②与盐反应:滴加X溶液,产生白色沉淀,则X可能为
③与酸反应:滴加盐酸,开始没有气泡,反应产生两种盐,推测两种盐的化学式
(3)取a克Na2CO3与NaHCO3混合物进行下列三组实验,其中能测定Na2CO3质量分数的是
A.充分加热,质量减少b克
B.与足量稀盐酸充分反应,加热、蒸干,灼烧,得b克固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙吸收,增重b克
任选上述合理方案中的一种,计算Na2CO3的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
Ⅰ.在常温下,某兴趣小组模拟“侯氏制碱法”制取碳酸钠,流程如下:

在常温下,有关物质的溶解度为:
(1)纯碱样品中阳离子的焰色是:___________ 。操作Ⅲ中的实验操作名称为:___________ 。操作Ⅰ和Ⅱ___________ (“能”或“不能”)颠倒。
(2)操作Ⅰ和操作Ⅱ总反应的化学方程式为___________ 。
Ⅱ.制得的纯碱 中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中
中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中 的质量分数。
的质量分数。

(3)确定 溶液是否过量的方法是:向溶液M中滴加
溶液是否过量的方法是:向溶液M中滴加 溶液,如果
溶液,如果___________ (填“有”或“无”)沉淀,则过量。
(4)若沉淀A没有洗涤烘干,导致 的质量分数
的质量分数___________ (填“偏大”、“偏小”或“不变”)。判断沉淀A洗净的方法是:取最后一次洗涤所得滤液,滴加 溶液,若
溶液,若___________ (填“有”或“无”)白色沉淀,则洗涤干净。
(5)样品中 的质量分数为
的质量分数为___________ (用字母m、n的代数式表示)。
Ⅰ.在常温下,某兴趣小组模拟“侯氏制碱法”制取碳酸钠,流程如下:

在常温下,有关物质的溶解度为:
| 物质 |  |  |  |  |
| 溶解度/g | 37.2 | 9.6 | 21.5 | 36.0 |
(1)纯碱样品中阳离子的焰色是:
(2)操作Ⅰ和操作Ⅱ总反应的化学方程式为
Ⅱ.制得的纯碱
 中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中
中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中 的质量分数。
的质量分数。
(3)确定
 溶液是否过量的方法是:向溶液M中滴加
溶液是否过量的方法是:向溶液M中滴加 溶液,如果
溶液,如果(4)若沉淀A没有洗涤烘干,导致
 的质量分数
的质量分数 溶液,若
溶液,若(5)样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-08-16更新
|
276次组卷
|
2卷引用:黑龙江省齐齐哈尔市部分学校2022-2023学年高一上学期11月期中考试化学试题
名校
解题方法
6 . 钠是一种非常活泼、具有广泛应用的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式是_______ ;可观察到的实验现象是_______ (填字母序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积_______ L;原混合气体的中CO2和H2O的分子数比为_______ 。
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
(1)将一小块金属钠投入水中,发生反应的离子方程式是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
| A.取a g混合物充分加热,质量减少b g |
| B.取a g混合物与足量NaOH溶液充分反应,得到b g溶液 |
| C.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体 |
| D.取a g混合物与足量稀硫酸反应,逸出气体经干燥后用碱石灰吸收,质量增加b g |
您最近一年使用:0次
2022-11-29更新
|
532次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高一上学期期中考试化学试题
名校
解题方法
7 . 下列试验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量CaCl2溶液反应,过滤、洗涤、烘干得到bg固体 |
| C.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg |
| D.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
您最近一年使用:0次
名校
8 . 钠及其化合物在人类生产生活中有着重大的作用。某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
Ⅰ. 制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3
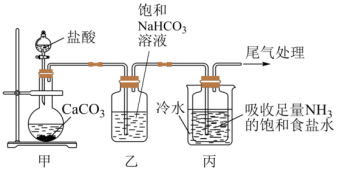
(1)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中反应的化学方程式为_________ 。
(2)用装置丙中产生的固体制取Na2CO3时,需要进行的实验操作有过滤、洗涤、灼烧,最后一步发生反应的化学方程式为_________ 。
Ⅱ. 测定产品纯度
用下图所示装置测定Na2CO3与NaHCO3固体混合物中Na2CO3的质量分数。
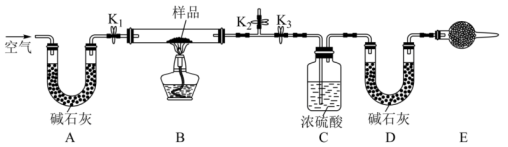
实验步骤如下:
a. 按图组装好实验装置并检查气密性;
b. 称取50g混合物放入硬质玻璃管中;称量装有碱石灰的形管的质量;
c. 打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟;
d. 关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体;
e. 打开活塞K1,缓缓鼓入空气数分钟后拆下装置,再次称量形管的质量。
(3)经测量,反应前后U形管D质量增重1.32g,样品中Na2CO3的质量分数为_________ ,若无E装置,则测得的Na2CO3的质量分数将_________ (填“偏大”“偏小”或“无影响”)。
(4)产品纯度也可以通过B装置的质量变化进行计算,称取m1g混合物放入硬质玻璃管中充分加热,反应后硬质玻璃管中固体质量为m2g,样品中Na2CO3的质量分数为_________ 。(用含m1、m2的式子表示)。
Ⅰ. 制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3

(1)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中反应的化学方程式为
(2)用装置丙中产生的固体制取Na2CO3时,需要进行的实验操作有过滤、洗涤、灼烧,最后一步发生反应的化学方程式为
Ⅱ. 测定产品纯度
用下图所示装置测定Na2CO3与NaHCO3固体混合物中Na2CO3的质量分数。

实验步骤如下:
a. 按图组装好实验装置并检查气密性;
b. 称取50g混合物放入硬质玻璃管中;称量装有碱石灰的形管的质量;
c. 打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟;
d. 关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体;
e. 打开活塞K1,缓缓鼓入空气数分钟后拆下装置,再次称量形管的质量。
(3)经测量,反应前后U形管D质量增重1.32g,样品中Na2CO3的质量分数为
(4)产品纯度也可以通过B装置的质量变化进行计算,称取m1g混合物放入硬质玻璃管中充分加热,反应后硬质玻璃管中固体质量为m2g,样品中Na2CO3的质量分数为
您最近一年使用:0次
解题方法
9 . 加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g,则混合物中碳酸钠的质量分数
| A.42% | B.58% | C.29% | D.50% |
您最近一年使用:0次
2022-09-19更新
|
288次组卷
|
3卷引用:黑龙江省齐齐市拜泉县第一中学2021-2022学年高一上学期期中考试化学试题
黑龙江省齐齐市拜泉县第一中学2021-2022学年高一上学期期中考试化学试题广东省惠州市博罗县2022-2023学年高一上学期期中考试化学试题(已下线)【2022】【高一上】【期中考】【杭九】【高中化学】【赵优萍收集】
名校
解题方法
10 . 计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含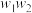 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为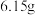 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为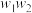 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
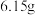 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次



