解题方法
1 . 某汽车安全气囊的气体发生剂主要含有叠氮化钠、三氧化二铁、高氯酸钾、碳酸氢钠等物质。
(1)叠氮化钠是气体发生剂,受热分解产生氮气和金属钠。反应的化学方程式为_____ 。
(2)高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。氧化钠中化学键的类型为_____ 。
(3)碳酸氢钠的作用是_____ 。
(1)叠氮化钠是气体发生剂,受热分解产生氮气和金属钠。反应的化学方程式为
(2)高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。氧化钠中化学键的类型为
(3)碳酸氢钠的作用是
您最近半年使用:0次
2 . 膨松剂反应产生气体的量是检验膨松剂品质的一项重要指标。某膨松剂中起蓬松作用的物质为碳酸氢钠和碳酸氢铵。
(1)某学校兴趣小组为研究该膨松剂在加热情况下发生的反应和放出的气体的量,设计了以下实验。
实验Ⅰ:将一定质量的固体样品置于试管中,用酒精灯加热片刻,在试管口立即可以闻到刺激性气味;加热足够长时间后,试管中仍有固体残留。
①结合以上实验现象,请写出加热时试管中所发生反应的化学方程式:_______ 。
②结合运用物质的量的相关计算,说明在碳酸氢钠中添加一定量碳酸氢铵的好处:_______ 。
实验Ⅱ:测定二氧化碳的质量
按下图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
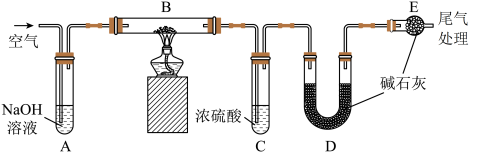
【资料】
a.浓硫酸常用于吸收水蒸气和氨气。
b.碱石灰是固体氢氧化钠和氧化钙的混合物,不与氨气反应。
将一定质量的膨松剂样品装入装置B中,测定实验前后装置_______ (填装置对应的字母符号)的质量,其质量差即为样品产生的二氧化碳的质量。加热前,先对已连接好的装置A、B和C通入一段时间的空气,再连接上装置D、E;停止加热后,应继续通入一段时间的空气。这样做的目的是_______ 。
实验Ⅲ:测定氨气的质量
调整上图装置的连接顺序为_______ 。取相同质量的膨松剂装入装置B中,测定实验前后装置C的质量,其质量差即为样品产生的氨气的质量。
(2)实验Ⅱ中,若没有装置E,可能会造成测定结果_______ (填“偏大”“偏小”或“不变”)。
(3)若实验Ⅱ和实验Ⅲ所取的膨松剂样品的质量一致,实验Ⅱ测得二氧化碳的质量为6.6g,实验Ⅲ测得氨气的质量为1.7g:
①通过计算分析该样品中碳酸氢钠和碳酸氢铵的物质的量之比_______ 。
②计算生成的氨气和二氧化碳的体积(STP),体会该膨松剂在加热情况下的体积膨胀效果_______ 。
(1)某学校兴趣小组为研究该膨松剂在加热情况下发生的反应和放出的气体的量,设计了以下实验。
实验Ⅰ:将一定质量的固体样品置于试管中,用酒精灯加热片刻,在试管口立即可以闻到刺激性气味;加热足够长时间后,试管中仍有固体残留。
①结合以上实验现象,请写出加热时试管中所发生反应的化学方程式:
②结合运用物质的量的相关计算,说明在碳酸氢钠中添加一定量碳酸氢铵的好处:
实验Ⅱ:测定二氧化碳的质量
按下图所示连接装置(气密性良好,各装置中的试剂皆为足量)。

【资料】
a.浓硫酸常用于吸收水蒸气和氨气。
b.碱石灰是固体氢氧化钠和氧化钙的混合物,不与氨气反应。
将一定质量的膨松剂样品装入装置B中,测定实验前后装置
实验Ⅲ:测定氨气的质量
调整上图装置的连接顺序为
(2)实验Ⅱ中,若没有装置E,可能会造成测定结果
(3)若实验Ⅱ和实验Ⅲ所取的膨松剂样品的质量一致,实验Ⅱ测得二氧化碳的质量为6.6g,实验Ⅲ测得氨气的质量为1.7g:
①通过计算分析该样品中碳酸氢钠和碳酸氢铵的物质的量之比
②计算生成的氨气和二氧化碳的体积(STP),体会该膨松剂在加热情况下的体积膨胀效果
您最近半年使用:0次
解题方法
3 . 现有某碳酸钠和碳酸氢钠的混合物样品,请设计两种实验方案测定其中碳酸钠的质量分数_______ 。
您最近半年使用:0次
解题方法
4 . 某学校化学兴趣小组从文献资料上获得如下信息: 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:
(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是_______ (填化学式)。
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于_______ mL。(设实验在标准状况下进行)
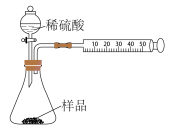
(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是_______ 。
 在潮湿空气中会缓慢分解成
在潮湿空气中会缓慢分解成 、
、 和
和 。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的
。为了验证这一信息,该兴趣小组将一瓶在潮湿空气中久置的 样品混合均匀后,进行如下实验:
样品混合均匀后,进行如下实验:(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是
(2)另取相同质量的样品放入锥形瓶中,实验装置如下图所示。为了保证实验成功,所选用针筒的最大刻度值应大于

(3)打开活塞逐滴加入稀硫酸,直至没有气泡产生为止。针筒中收集到的气体体积折算成标准状况下的体积为
 (滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中
(滴入稀硫酸的体积及针筒活塞与内壁的摩擦力忽略不计)。该兴趣小组设称取的每份样品中 、
、 的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式,
的物质的量分别为x、y,且没有利用化学方程式进行计算,就列出算式, ,他们依据的原理是
,他们依据的原理是
您最近半年使用:0次
解题方法
5 . 碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物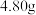 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为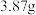 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数_______ 。
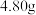 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为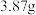 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数
您最近半年使用:0次
解题方法
6 . 下列有关 和
和 的叙述中,错误的是
的叙述中,错误的是
 和
和 的叙述中,错误的是
的叙述中,错误的是A.热稳定性: |
B.可以用澄清石灰水来鉴别 和 和 |
C.在一定的条件下, 与 与 之间可以相互转化 之间可以相互转化 |
D.等质量的 和 和 与足量盐酸反应, 与足量盐酸反应, 放出的 放出的 更多 更多 |
您最近半年使用:0次
名校
解题方法
7 . 下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3的质量分数的是
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| C.取ag混合物与足量稀盐酸反应,加热、蒸干、灼烧,得到bg固体 |
| D.取ag混合物与足量稀盐酸反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
您最近半年使用:0次
2022-09-14更新
|
1605次组卷
|
41卷引用:辽宁省大连市长兴岛经济区长兴岛高级中学2019-2020学年高一上学期第二次月考化学试题
辽宁省大连市长兴岛经济区长兴岛高级中学2019-2020学年高一上学期第二次月考化学试题(已下线)【浙江新东方】28湖南省长沙市长郡教育集团2020-2021学年高一上学期期中考试化学试题浙江省温州新力量联盟2020-2021学年高一上学期期中联考化学试题湖南省长沙市长郡中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】在线化学 (9).湖南省湘潭电机子弟中学2020-2021学年高一上学期段考化学试题广东省广州市广雅中学2020-2021学年高一上学期期中考试化学试题湖北省随州市第一中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw68浙江省湖州市2020-2021学年高一上学期期末考试化学试题湖南省平江县第一中学2020-2021学年高一上学期期末考试化学试题河北省石家庄市第十七中学2020-2021学年高一上学期期中考试化学试题浙江省余姚中学2020-2021 学年高一上学期期中考试化学试题(已下线)【浙江新东方】在线化学57高一上(已下线)【浙江新东方】高中化学20210429—007【2021】【高一下】河北省石家庄精英中学2020-2021学年高二下学期期末考试化学试题第2章第一节第3课时碳酸钠和碳酸氢钠(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)(已下线)第二章 海水中的重要元素——钠和氯(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)黑龙江省大庆实验中学2021-2022学年高一上学期10月月考化学试题广东省惠州市2020-2021学年高一上学期期末质量检测化学试题广东省广州市三校2021-2022学年高一上学期期中联考化学试题河北师范大学附属中学2021-2022学年高一上学期期中考试化学试题河北省石家庄市第二十八中学2021-2022学年高一上学期期中考试化学试题人教2019版必修第一册第二章第一节 钠及其化合物课后习题浙江省宁波市咸祥中学2021-2022学年高一上学期期中考试化学试题湖南省岳阳县一中 汨罗市一中2021-2022学年高一上学期期中联考化学试题辽宁省六校协作体2021-2022学年高一上学期第三次月考化学试题安徽省马鞍山第二中学2021-2022学年高一上学期期中考试化学试题 湖南省长沙市雨花区2021-2022学年高一上学期期末考试化学试题湖北省巴东一中2020-2021学年高一上学期第五次月考化学试题河北省石家庄市2021-2022学年高一上学期期末考试化学试题湖南省长郡中学2021-2022学年高一上学期期末考试化学试题云南省昆明市第一中学2021-2022学年高一上学期期末考试化学试题河南省兰考县第一高级中学2021-2022学年高一上学期期末考试化学试题河南省焦作市武陟县第一中学东校区2021-2022学年高一下学期4月月考化学试题 山东省济宁市兖州区2021-2022学年高一下学期期中考试化学试题广东省深圳市盐田高级中学2021-2022学年高一下学期期中考试化学试题湖南省邵阳市隆回县2021-2022学年高一上学期期末考试化学试题湖南省常德市汉寿县第一中学2022-2023学年高三上学期第一次月考化学试题课时2 钠的几种化合物
解题方法
8 . 碳酸钠和碳酸氢钠在食品工业中均可用作食品添加剂,它们也是生活中常见的日用化学品。
(1)为了解碳酸钠和碳酸氢钠的性质,请根据以下提示设计实验并完成实验报告。___________
①观察二者的颜色和状态;
②观察其在冷水和热水中的溶解情况;
③测定其饱和溶液的pH;
④向其溶液中分别逐滴加入盐酸,观察现象。
(2)根据以上实验的结果和已学过的知识,列表比较碳酸钠和碳酸氢钠性质的异同。___________
(3)举例说明碳酸钠和碳酸氢钠在日常生活或食品工业中的用途,根据二者的性质进行解释,并与同学讨论。___________
(1)为了解碳酸钠和碳酸氢钠的性质,请根据以下提示设计实验并完成实验报告。
①观察二者的颜色和状态;
②观察其在冷水和热水中的溶解情况;
③测定其饱和溶液的pH;
④向其溶液中分别逐滴加入盐酸,观察现象。
(2)根据以上实验的结果和已学过的知识,列表比较碳酸钠和碳酸氢钠性质的异同。
(3)举例说明碳酸钠和碳酸氢钠在日常生活或食品工业中的用途,根据二者的性质进行解释,并与同学讨论。
您最近半年使用:0次
9 . 某小组同学探究Na2CO3的性质,请你与他们一起完成,并回答问题。
(1)观察:描述Na2CO3的颜色、状态:___________ 。
(2)预测:从物质的类别来看,Na2CO3属于___________ 类,可以与___________ 等类别的物质发生反应。
(3)设计实验并得出结论:
(4)问题和讨论:
①该组同学在探究Na2CO3的性质时,思路是什么?运用了哪些方法?___________
②在实验室中,如何鉴别NaHCO3和Na2CO3?___________
(1)观察:描述Na2CO3的颜色、状态:
(2)预测:从物质的类别来看,Na2CO3属于
(3)设计实验并得出结论:
| 实验步骤 | 实验现象 | 结论或解释 (用离子方程式表示) |
| ①向盛有Na2CO3溶液的试管中滴加澄清石灰水 | ||
| ②向盛有Na2CO3溶液的试管中滴加CaCl2溶液 | ||
| ③向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ① ② |
①该组同学在探究Na2CO3的性质时,思路是什么?运用了哪些方法?
②在实验室中,如何鉴别NaHCO3和Na2CO3?
您最近半年使用:0次
2019高一·浙江·专题练习
解题方法
10 . 为除去下列物质中的杂质(括号内),请写出所加的试剂或操作,并写出相应的化学方程式,是离子反应的,请写出离子方程式。
(1)Na2CO3固体(NaHCO3)___________ 。
(2)NaHCO3溶液(Na2CO3)___________ 。
(3)NaOH溶液(Na2CO3)___________ 。
(4)NaCl溶液(Na2CO3)___________ 。
(1)Na2CO3固体(NaHCO3)
(2)NaHCO3溶液(Na2CO3)
(3)NaOH溶液(Na2CO3)
(4)NaCl溶液(Na2CO3)
您最近半年使用:0次



