名校
1 . 下列说法不正确的是
| A.二氧化硫可以使石蕊试液褪色 |
B.雷雨天气有助于空气中的N2转化为可供植物吸收的 |
| C.氧化镁熔点高,是一种优良的耐火材料 |
| D.配制Hg(NO3)2溶液时,将Hg(NO3)2溶于较浓硝酸中,然后加水稀释 |
您最近一年使用:0次
名校
2 . 图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。下列说法错误的是
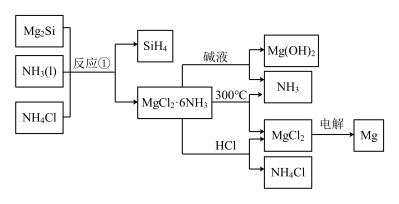

| A.电解熔融MgCl2制Mg |
| B.该流程中可以循环使用的物质是NH3和NH4Cl |
| C.利用MgCl2·6NH3制取镁的过程中发生了化合反应、分解反应 |
| D.分别将MgCl2溶液和Mg(OH)2悬浊液加热、灼烧,最终得到的固体相同 |
您最近一年使用:0次
解题方法
3 . 加热蒸干氯化镁溶液时因水解不完全会得到一种灰白色沉淀一一碱式氯化镁,化学式可表示为Mgx(OH)yClz•nH2O.设计如图装置验证其化学式。下列有关实验说法不正确的是( )


| A.碱式氯化镁受热分解可以产生氧化镁,氯气和水 |
| B.结束反应时,先停止加热,通一段时间N2后再关闭活塞K |
| C.①②中依次盛装氢氧化钠溶液、浓硫酸 |
| D.只需称取原样品质量、反应结束后硬质玻璃管中剩余固体质量以及装置①增重的质量即可推出其化学式 |
您最近一年使用:0次
2020-04-01更新
|
293次组卷
|
3卷引用:四川省成都市2020届高三上学期第二次统考检测化学试题
名校
解题方法
4 . 海水中Mg元素只要以MgCl2的形式存在,海水提镁的主要流程如下:
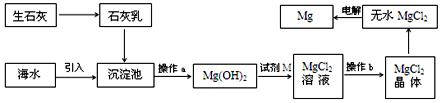
(1)下列说法不正确的是___________ 。
A.试剂M是盐酸 B.生石灰在食品工业中常用于防潮剂
C.操作b只是过滤 D.MgCl2电解为Mg时,Mg2+得到的电子数为2NA
(2)沉淀池中的主要反应化学方程式为________________________________ 。
(3)为了得到纯净的Mg(OH)2,操作a是___________ ,实验室洗涤沉淀的操作是____________ 。
(4)已知常温下Ca(OH)2溶解度为0.15g,饱和石灰水密度约为1g/mL,物质的量浓度约为___ 。

(1)下列说法不正确的是
A.试剂M是盐酸 B.生石灰在食品工业中常用于防潮剂
C.操作b只是过滤 D.MgCl2电解为Mg时,Mg2+得到的电子数为2NA
(2)沉淀池中的主要反应化学方程式为
(3)为了得到纯净的Mg(OH)2,操作a是
(4)已知常温下Ca(OH)2溶解度为0.15g,饱和石灰水密度约为1g/mL,物质的量浓度约为
您最近一年使用:0次
5 . 下列说法不正确的是( )
| A.氯化钠可用于配制生理盐水 | B.二氧化硅可用于制造玻璃 |
| C.海水中的钠元素以单质存在 | D.氧化镁(熔点2 800 ℃)是优良的耐高温材料 |
您最近一年使用:0次
2017-08-12更新
|
2087次组卷
|
6卷引用:西藏林芝市第二高级中学2021-2022学年高三上学期第三次月考理综化学试题
西藏林芝市第二高级中学2021-2022学年高三上学期第三次月考理综化学试题浙江省2018版考前特训(2017年10月)学考70快练:7 元素及其化合物浙江省宁波诺丁汉大学附属中学2017-2018学年高一上学期期中考试化学试题2016年10月浙江省普通高校招生选考科目考试化学试题(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)
名校
6 . 下列有关常见的几种金属氧化物的性质和用途的说法不正确的是
| A.氧化钙可用作干燥剂 | B.Fe2O3可用于制作红色油漆和涂料 |
| C.MgO和Al2O3可用作耐高温材料 | D.Na2O2、CuO、FeO都能溶于水,且与水反应都生成相应的碱 |
您最近一年使用:0次
7 . 化学与生活密切相关,下列说法错误的是
| A.氧化镁可制做耐火材料 |
| B.药皂中含苯酚具有杀菌、消毒作用 |
| C.甲醛的水溶液可用于蔬菜防腐 |
| D.醋酸用来除水垢 |
您最近一年使用:0次
8 . 将一定质量由镁和铝组成的合金投入200 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加6 mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如下图所示:
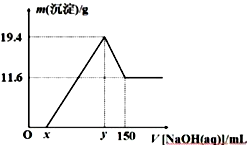
下列说法不正确的是

下列说法不正确的是
| A.镁铝合金中,Mg与Al的物质的量之比为 2∶1 |
| B.所用盐酸的物质的量浓度为4 mol/L |
| C.图象中的x=20 |
| D.图象中,Ox 段的离子方程式为:H++OH-= H2O;y~150 段的离子方程式为:Al(OH)3+OH-=AlO2-+ 2H2O |
您最近一年使用:0次
2018-01-21更新
|
615次组卷
|
3卷引用:四川省成都市第七中学2017-2018学年度上学期高一1月阶段性测试化学试题
9 . 下列有关物质性质的应用的说法正确的是
| A.金属活泼性铜比铁弱.可在铁船闸上装铜块减缓其腐蚀 |
| B.MgO的熔点很高,可用于制作耐高温材料 |
| C.铝能置换出氧化铁中的铁,可用于钢铁工业中大量冶炼铁 |
| D.二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
您最近一年使用:0次
10 . 无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:


步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5 MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是____________ 。
实验中不能用干燥空气代替干燥N2,原因是___________ 。
(2)如将装置B改为装置C(图2),可能会导致的后果是___________ 。
(3)步骤3中,第一次过滤除去的物质是___________ 。
(4)有关步骤4的说法,正确的是___________ 。
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++ Y4-="===Mg" Y2-
①滴定前润洗滴定管的操作方法是__________ 。
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________________________ (以质量分数表示)。


步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5
 MgBr2·3C2H5OC2H5
MgBr2·3C2H5OC2H5请回答:
(1)仪器A的名称是
实验中不能用干燥空气代替干燥N2,原因是
(2)如将装置B改为装置C(图2),可能会导致的后果是
(3)步骤3中,第一次过滤除去的物质是
(4)有关步骤4的说法,正确的是
| A.可用95%的乙醇代替苯溶解粗品 | B.洗涤晶体可选用0℃的苯 |
| C.加热至160℃的主要目的是除去苯 | D.该步骤的目的是除去乙醚和可能残留的溴 |
Mg2++ Y4-="===Mg" Y2-
①滴定前润洗滴定管的操作方法是
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是
您最近一年使用:0次
2016-12-09更新
|
1505次组卷
|
6卷引用:2017届四川省成都树德中学高三10月月考化学卷
2017届四川省成都树德中学高三10月月考化学卷四川省雅安中学2018届高三上学期第一次月考化学试题【全国百强校】湖南省长沙市第一中学2019届高三下学期第七次月考理科综合化学试题2016年全国普通高等学校招生统一考试化学(浙江卷精编版)2016年全国普通高等学校招生统一考试化学(浙江卷参考版)(已下线)专题22.综合实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)



