名校
1 . 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的进程,铁是应用最广泛的金属,被人类誉为金属之王;而铝在地壳中的含量比铁更高,居于榜首。
(1)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。常用如图所示装置,下列叙述错误的是

(2)写出上述反应的化学方程式________ ,其中铝作________ 。(填“氧化剂”或“还原剂”)
(1)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。常用如图所示装置,下列叙述错误的是

| A.该反应属于置换反应 |
| B.有“熔融铁珠”生成说明该反应为放热反应 |
| C.该反应的化学能全部转化为热能 |
| D.该反应中生成物的总能量小于反应物的总能量 |
您最近一年使用:0次
名校
解题方法
2 . 下图中甲是演示金属钠与水反应的实验装置,为收集并检验气体产物,某兴趣小组将甲装置改进成如图中乙或丙所示的装置,请根据要求回答下列问题。
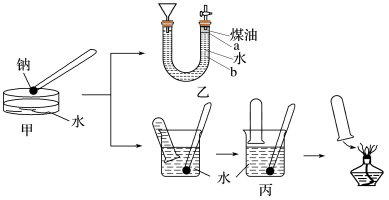
(1)写出钠与水反应的离子方程式:___________ 。和铝相比,钠与水反应更剧烈的原因是___________ (从原子结构的角度进行解释说明)。
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
(3)用乙装置实验,点燃气体产物时,是否需要检验纯度?___ (填“是“或“否”)。
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是________ 。
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大

(1)写出钠与水反应的离子方程式:
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
| A.钠块始终保持在煤油中的a处,直至完全消失 |
| B.钠处于煤油和水的交界处上下浮动 |
| C.随反应的进行煤油与胶塞处液面下降,漏斗中液面上升 |
| D.最终钠块在煤油中燃烧起来 |
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大
您最近一年使用:0次
名校
解题方法
3 . 铝分别与足量的稀硫酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的H2SO4和NaOH物质的量之比为
| A.1∶1 | B.2∶1 | C.3∶2 | D.1∶3 |
您最近一年使用:0次
名校
解题方法
4 . 某溶液中有 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
5 . 能正确表达下列反应的离子方程式为
A.将 通入过量 通入过量 溶液: 溶液: |
B.在 溶液中加入过量石灰水: 溶液中加入过量石灰水: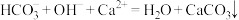 |
C.向硫酸铝溶液中加入过量氨水: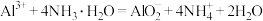 |
D.少量氯水滴入 溶液: 溶液: |
您最近一年使用:0次
名校
解题方法
6 . 人类的生产和生活都离不开金属。金属材料的使用作为一个时代的标志,见证了人类文明发展的过程,历史上人类冶炼不同金属的大致年代如图所示:
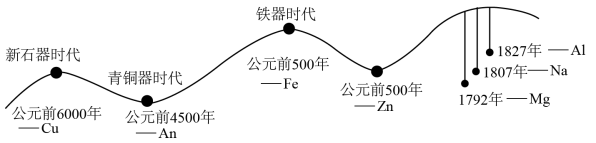
(1)由图可知:人类最早使用的合金是________ ,通过敲打可将金属材料打制成不同的形状,是利用了金属的________ 性。含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是________ (填字母)。
A.铝合金 B.镁合金 C.生铁 D,钢
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾,熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是________ (填字母)。
A.“苦泉”的溶质之一: ;
;
B.“挹其水熬之”:蒸发溶剂;
C.“熬胆矾铁釜,久之亦化为铜”:发生分解反应。
(3)铝的使用距今仅200年左右,现如今铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是________ (用化学方程式表示)。
(4)某溶液中含有 、
、 、
、 、
、 等离子,向其中加入过量
等离子,向其中加入过量 后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是________ (填字母),大量增加的离子有________ (填化学式)。
A. B.
B. C.
C. D.
D.
工业上用废铁皮制取铁红 的部分流程示意图如下:
的部分流程示意图如下:
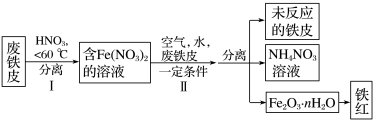
(5)步骤II中发生反应: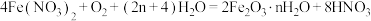 ,反应产生的
,反应产生的 又可将废铁皮中的铁转化为
又可将废铁皮中的铁转化为 ,该反应的化学方程式为:
,该反应的化学方程式为:________ 。
 可制取新型、高效水处理剂——高铁酸钾
可制取新型、高效水处理剂——高铁酸钾 。
。
________ ________
________ ________
________ ________
________ (高铁酸钾)+________
(高铁酸钾)+________ ________
________
(6)配平上述反应,并用单线桥法表示反应过程中的电子转移方向和数目________ 。
(7)此过程中氧化剂是________ (填化学式)。
(8)高铁酸钾 是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有
是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有________ 、________
工业上常用铝质容器盛装冷浓酸,为研究铝质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(9)将铝片放入氢氧化钠溶液中可去除表面氧化膜,反应的离子方程式为:________ 。
(10)将已除去表面氧化膜的铝片继续置于氢氧化钠溶液中,迅速产生大量气泡,反应的化学方程式为:________ 。反应过程中氧化剂与还原剂的物质的量之比为________ 。
(11)另取一同样已除去表面氧化膜的铝片放入冷浓硫酸中,10分钟后,移入硫酸铜溶液中,片刻后取出观察,铝片表面无明显变化,其原因是________ 。
(12)另称取铝片6.0g放入15.0mL浓硫酸中,加热,充分应后收集到气体X;甲同学取448mL(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量 溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中
溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中 的体积分数为
的体积分数为________ 。
分析上述实验中 体积分数的结果,丙同学认为气体X中还可能含量有
体积分数的结果,丙同学认为气体X中还可能含量有 ;为此设计了下列探究实验装置(图中央持仪器省略)。
;为此设计了下列探究实验装置(图中央持仪器省略)。
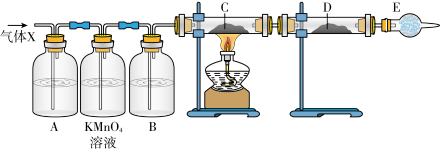
(13)丙同学认为还可能产生氢气的理由是________ 。
(14)A中试剂可选用________。
(15)B中加入的试剂是________ ,E的作用是________ 。
(16)可以证明气体X中含有氢气的实验现象是:________ 。

(1)由图可知:人类最早使用的合金是
A.铝合金 B.镁合金 C.生铁 D,钢
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾,熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是
A.“苦泉”的溶质之一:
 ;
;B.“挹其水熬之”:蒸发溶剂;
C.“熬胆矾铁釜,久之亦化为铜”:发生分解反应。
(3)铝的使用距今仅200年左右,现如今铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是
(4)某溶液中含有
 、
、 、
、 、
、 等离子,向其中加入过量
等离子,向其中加入过量 后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是A.
 B.
B. C.
C. D.
D.
工业上用废铁皮制取铁红
 的部分流程示意图如下:
的部分流程示意图如下:
(5)步骤II中发生反应:
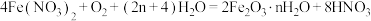 ,反应产生的
,反应产生的 又可将废铁皮中的铁转化为
又可将废铁皮中的铁转化为 ,该反应的化学方程式为:
,该反应的化学方程式为: 可制取新型、高效水处理剂——高铁酸钾
可制取新型、高效水处理剂——高铁酸钾 。
。________
 ________
________ ________
________ ________
________ (高铁酸钾)+________
(高铁酸钾)+________ ________
________
(6)配平上述反应,并用单线桥法表示反应过程中的电子转移方向和数目
(7)此过程中氧化剂是
(8)高铁酸钾
 是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有
是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有工业上常用铝质容器盛装冷浓酸,为研究铝质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(9)将铝片放入氢氧化钠溶液中可去除表面氧化膜,反应的离子方程式为:
(10)将已除去表面氧化膜的铝片继续置于氢氧化钠溶液中,迅速产生大量气泡,反应的化学方程式为:
(11)另取一同样已除去表面氧化膜的铝片放入冷浓硫酸中,10分钟后,移入硫酸铜溶液中,片刻后取出观察,铝片表面无明显变化,其原因是
(12)另称取铝片6.0g放入15.0mL浓硫酸中,加热,充分应后收集到气体X;甲同学取448mL(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量
 溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中
溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中 的体积分数为
的体积分数为分析上述实验中
 体积分数的结果,丙同学认为气体X中还可能含量有
体积分数的结果,丙同学认为气体X中还可能含量有 ;为此设计了下列探究实验装置(图中央持仪器省略)。
;为此设计了下列探究实验装置(图中央持仪器省略)。
(13)丙同学认为还可能产生氢气的理由是
(14)A中试剂可选用________。
| A.溴水 | B.品红溶液 | C.氢氧化钠溶液 | D.饱和食盐水 |
(16)可以证明气体X中含有氢气的实验现象是:
您最近一年使用:0次
7 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
(1)Fe(OH)2很不稳定,露置在空气中容易被氧化,该反应的化学方程式为___________ ,现象为___________ 。
(2)为了获得白色的Fe(OH)2沉淀,在用硫酸亚铁晶体配置硫酸亚铁溶液时,往往会加入___________ ,目的是___________ 。
(3)Fe3+比 Fe2+稳定,请写出 Fe3+的检验过程和现象___________ ,涉及反应的离子方程式是___________ 。
(4)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式___________ ,该反应是___________ (吸或放)热反应,其中铝发生___________ (氧化或还原)反应。
(1)Fe(OH)2很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
(2)为了获得白色的Fe(OH)2沉淀,在用硫酸亚铁晶体配置硫酸亚铁溶液时,往往会加入
(3)Fe3+比 Fe2+稳定,请写出 Fe3+的检验过程和现象
(4)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 如图是铝热反应的装置图,对该反应叙述正确的是


| A.铝热反应是放热反应,所以常温下可以反应 |
| B.KClO3是该反应的催化剂 |
| C.利用铝热反应可焊接钢轨,也可冶炼锰等难熔金属 |
| D.图中a为镁条,b为KClO3,c为Al2O3和Fe的混合物 |
您最近一年使用:0次
名校
解题方法
9 . 铁是一种化学元素,化学符号为 Fe,它是是地壳中含量第四多的元素,由于其机械性能和低成本,铁合金(如钢、不锈钢和合金钢)是到目前为止仍是最常见的工业金属。下列有关说法错误的是
| A.“威尼斯红”的颜色主要来自近纯氧化铁(Fe2O3)的赤铁矿 |
| B.人类可以利用铝热反应的原理焊接铁轨,也可以冶炼金属V、Cr、Mg 等 |
| C.铁粉可以作为食品添加剂,添加入一些补铁食品中 |
| D.指南针是我国的四大发明之一,制造指南针的磁性物质是 Fe3O4 |
您最近一年使用:0次
名校
10 . 金属铝在生产生活中有广泛用途。
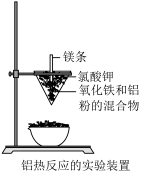
(1)写出工业通过电解法生产铝的化学方程式___________
(2)写出该铝热反应的化学方程式___________ ;利用铝热反应在工业上可冶炼___________ 金属(填编号)。
A.强还原性 B.难熔性 C.易导电 D.活泼
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。______
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为___________ 。

(1)写出工业通过电解法生产铝的化学方程式
(2)写出该铝热反应的化学方程式
A.强还原性 B.难熔性 C.易导电 D.活泼
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为
您最近一年使用:0次



