解题方法
1 . 用废旧复离子电池正极材料分离回收金属元素,正极材料主要为活性材料LiNixCoyMn1-x-yO2与铝箔组成,工艺流程知下:

已知: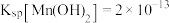 ,
,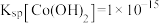 ,
,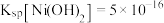
回答下列问题:
(1)碱浸结束后,滤液中的阴离子除了 ,主要还有
,主要还有___________ (填化学式)。正极活性材料LiNixCoyMn1-x-yO2中Ni、Co、Mn化合价相同,则它们的化合价为___________ 。
(2)固相反应一般反应速率较慢,加快还原焙烧反应速率的方法可以是___________ (至少写两种)。
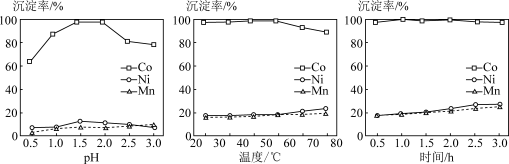
(3)①外界条件pH、温度和搅拌时间对三种金属离子沉淀率的影响如下图,则沉钴最合适的条件为___________ (填标号)。
a.pH=2.0温度55℃时间1.0h b.pH=1.5温度75℃时间1.0h
c.pH=2.0温度55℃时间3.0h d.pH=1.5温度75℃时间3.0h
②洗涤碱式碳酸镍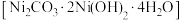 最好选择
最好选择___________ (填标号)。
a.碳酸钠溶液b.氢氧化钠溶液c.氨水d.蒸馏水
③写出沉锰过程中生成 的离子反应方程式:
的离子反应方程式:___________ 。
(4)共沉淀法是将两个或两个以上组分同时沉淀的一种方法。酸浸后也可直接调pH使 、
、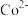 、
、 沉淀完全回收,则pH应大于
沉淀完全回收,则pH应大于___________ (已知:lg2=0.3,溶液中离子浓度小于 认为沉淀完全)。
认为沉淀完全)。

已知:
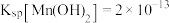 ,
,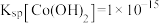 ,
,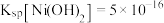
回答下列问题:
(1)碱浸结束后,滤液中的阴离子除了
 ,主要还有
,主要还有(2)固相反应一般反应速率较慢,加快还原焙烧反应速率的方法可以是
(3)①外界条件pH、温度和搅拌时间对三种金属离子沉淀率的影响如下图,则沉钴最合适的条件为
a.pH=2.0温度55℃时间1.0h b.pH=1.5温度75℃时间1.0h
c.pH=2.0温度55℃时间3.0h d.pH=1.5温度75℃时间3.0h

②洗涤碱式碳酸镍
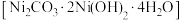 最好选择
最好选择a.碳酸钠溶液b.氢氧化钠溶液c.氨水d.蒸馏水
③写出沉锰过程中生成
 的离子反应方程式:
的离子反应方程式:(4)共沉淀法是将两个或两个以上组分同时沉淀的一种方法。酸浸后也可直接调pH使
 、
、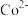 、
、 沉淀完全回收,则pH应大于
沉淀完全回收,则pH应大于 认为沉淀完全)。
认为沉淀完全)。
您最近一年使用:0次
名校
解题方法
2 . 将 由
由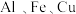 组成的合金等分为两份,将其中一份合金溶于足量的
组成的合金等分为两份,将其中一份合金溶于足量的 溶液中,产生气体
溶液中,产生气体 (标准状况);另一份合金溶于过量的稀硝酸中,得到
(标准状况);另一份合金溶于过量的稀硝酸中,得到 (标准状况下)
(标准状况下) 气体,向反应后的溶液中加入过量的
气体,向反应后的溶液中加入过量的 溶液,过滤得到滤液X和
溶液,过滤得到滤液X和 的沉淀Y(若
的沉淀Y(若 的还原产物仅为
的还原产物仅为 ),则下列说法正确的是
),则下列说法正确的是
 由
由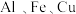 组成的合金等分为两份,将其中一份合金溶于足量的
组成的合金等分为两份,将其中一份合金溶于足量的 溶液中,产生气体
溶液中,产生气体 (标准状况);另一份合金溶于过量的稀硝酸中,得到
(标准状况);另一份合金溶于过量的稀硝酸中,得到 (标准状况下)
(标准状况下) 气体,向反应后的溶液中加入过量的
气体,向反应后的溶液中加入过量的 溶液,过滤得到滤液X和
溶液,过滤得到滤液X和 的沉淀Y(若
的沉淀Y(若 的还原产物仅为
的还原产物仅为 ),则下列说法正确的是
),则下列说法正确的是A. 的合金中含铝 的合金中含铝 | B.滤液X中的溶质只有硝酸钠 |
| C.V为6.72 | D.沉淀Y中含氢氧化铜 |
您最近一年使用:0次
2022-05-14更新
|
728次组卷
|
3卷引用:山东省临沂市2021-2022学年高一下学期期中考试化学试题
3 . 现有金属单质 和气体甲、乙、丙及物质
和气体甲、乙、丙及物质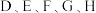 ,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。请根据信息回答下列问题:
,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。请根据信息回答下列问题:
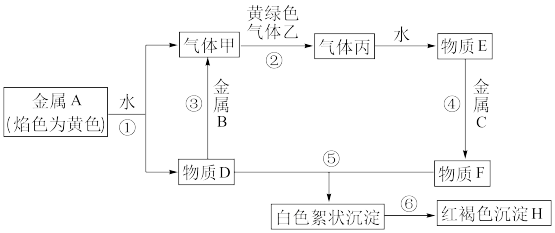
(1)当反应①中有 反应时,生成的气体甲在标准状况下的体积为
反应时,生成的气体甲在标准状况下的体积为_______ 。反应③的离子方程式为_______ 。
(2)写出反应⑥的化学方程式_______ 。
(3)金属A的某种氧化物可用作供氧剂,写出其与水反应的化学方程式_______ 。
(4)向 某浓度的D溶液中缓慢通入一定量的
某浓度的D溶液中缓慢通入一定量的 ,充分反应后,向上述所得溶液中,逐滴滴加
,充分反应后,向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
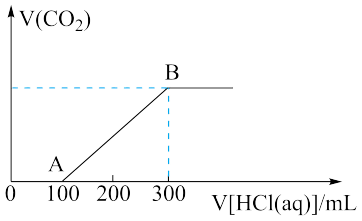
 与D反应所得溶液中溶质的成分为:
与D反应所得溶液中溶质的成分为:_______ 。B点溶液中溶质的物质的量浓度(体积变化忽略不计)是_______ 。
 和气体甲、乙、丙及物质
和气体甲、乙、丙及物质 ,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。请根据信息回答下列问题:
,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。请根据信息回答下列问题:
(1)当反应①中有
 反应时,生成的气体甲在标准状况下的体积为
反应时,生成的气体甲在标准状况下的体积为(2)写出反应⑥的化学方程式
(3)金属A的某种氧化物可用作供氧剂,写出其与水反应的化学方程式
(4)向
 某浓度的D溶液中缓慢通入一定量的
某浓度的D溶液中缓慢通入一定量的 ,充分反应后,向上述所得溶液中,逐滴滴加
,充分反应后,向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
 与D反应所得溶液中溶质的成分为:
与D反应所得溶液中溶质的成分为:
您最近一年使用:0次
2022-01-24更新
|
261次组卷
|
2卷引用:山东省济宁市2021-2022学年高一上学期期末考试化学试题
4 . 兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,具有优良的储氢性能。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如图:
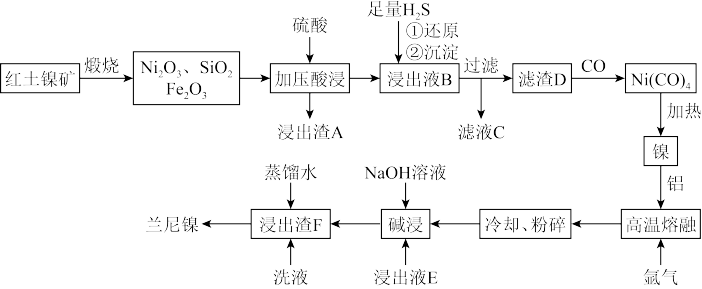
(1)形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___ ,Ni(CO)4含有的化学键类型___ 。
(2)Ni2O3有强氧化性,加压酸浸时,有气体产生且镍被还原为Ni2+,则产生的气体为___ (填化学式)。
(3)滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体生成单质镍的离子方程式:___ 。
(4)“高温熔融”时通入氩气的目的是___ 。
(5)检验滤液C中金属阳离子的试剂是___ (填标号)。
a.KSCN溶液 b.K3[Fe(CN)6] c.酸性高锰酸钾 d.苯酚
(6)碱浸的目的是使镍铝合金产生多孔结构,其原理___ (用化学方程式表示)。

(1)形成Ni(CO)4时碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为
(2)Ni2O3有强氧化性,加压酸浸时,有气体产生且镍被还原为Ni2+,则产生的气体为
(3)滤渣D为单质镍、硫的混合物,请写出向浸出液B中通入H2S气体生成单质镍的离子方程式:
(4)“高温熔融”时通入氩气的目的是
(5)检验滤液C中金属阳离子的试剂是
a.KSCN溶液 b.K3[Fe(CN)6] c.酸性高锰酸钾 d.苯酚
(6)碱浸的目的是使镍铝合金产生多孔结构,其原理
您最近一年使用:0次
名校
解题方法
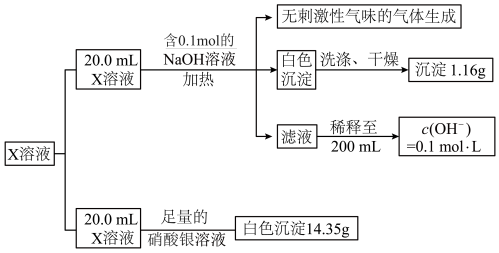
5 . 40mL某溶液可能含有下列离子中的若干种:Cl﹣、 、Na+、Mg2+、Al3+。现对溶液进行下列操作,其现象和结果如图所示:下列说法正确的是
、Na+、Mg2+、Al3+。现对溶液进行下列操作,其现象和结果如图所示:下列说法正确的是
 、Na+、Mg2+、Al3+。现对溶液进行下列操作,其现象和结果如图所示:下列说法正确的是
、Na+、Mg2+、Al3+。现对溶液进行下列操作,其现象和结果如图所示:下列说法正确的是
| A.X溶液中一定含有Na+,且c(Na+)=1.5mol/L |
| B.X溶液中一定含有Mg2+,且c(Mg2+)=0.5mol/L |
C.X溶液中一定含有Mg2+、Cl﹣,不含有 、Al3+,可能有Na+ 、Al3+,可能有Na+ |
| D.X溶液中一定含有Na+、Mg2+、Cl﹣,可能含有Al3+ |
您最近一年使用:0次
2021-04-07更新
|
792次组卷
|
5卷引用:山东省青岛市一中2022-2023学年高一下学期期中考试化学试题
6 . 下图是无机物 A~J在一定条件下的转化关系(部分产物及反应条件未列出)。其中C为红棕色气体;H和I是两种常见的金属单质;过量I与 D溶液反应生成A。
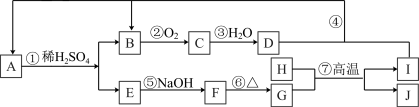
请填写下列空白:
(1)H元素在周期表中的位置是________ ;写出①的离子反应方程式:_________ ;检验E溶液中阳离子的最佳试剂为________ 。
(2)这类反应常用于冶炼高熔点的金属。用MnO2冶炼金属锰的反应中氧化剂与还原剂的物质的量之比为__________ 。
(3)SCR技术处理机动车尾气时,在催化条件下利用氨气与C反应,生成无污染的物质。发生反应的化学方程式为__________ 。
(4)F与NaClO、NaOH溶液反应,可制得一种“绿色”高效净水剂K2FeO4。每生成1molFeO42-时转移____________ mol电子。
(5)B为大气污染物,利用炭粉可以将其还原为无污染的物质X2。
已知:X2(g)+O2(g)=2XO(g) △H=+180.6kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出用碳粉还原B的热化学方程式__________ 。

请填写下列空白:
(1)H元素在周期表中的位置是
(2)这类反应常用于冶炼高熔点的金属。用MnO2冶炼金属锰的反应中氧化剂与还原剂的物质的量之比为
(3)SCR技术处理机动车尾气时,在催化条件下利用氨气与C反应,生成无污染的物质。发生反应的化学方程式为
(4)F与NaClO、NaOH溶液反应,可制得一种“绿色”高效净水剂K2FeO4。每生成1molFeO42-时转移
(5)B为大气污染物,利用炭粉可以将其还原为无污染的物质X2。
已知:X2(g)+O2(g)=2XO(g) △H=+180.6kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出用碳粉还原B的热化学方程式
您最近一年使用:0次
名校
7 . 下列实验现象中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 新制氯水中加入少量CaCO3 | 有气泡产生 | 酸性:HClO>H2CO3 |
| B | 向酸性KMnO4溶液中滴入待测液 | 溶液褪色 | 待测液中含Fe2+ |
| C | 铝箔插入稀硝酸中 | 无明显现象 | 铝箔表面形成了致密的氧化膜 |
| D | 向蔗糖中滴入浓硫酸 | 固体变黑,产生刺激性气体 | 浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
467次组卷
|
4卷引用:2021年秋季高三化学开学摸底考试卷03(山东专用)
(已下线)2021年秋季高三化学开学摸底考试卷03(山东专用)2017届山西临汾一中等五校高三上第二次联考化学试卷安徽省庐巢七校联盟2020届高三第五次联考化学试题湖南省常德市第一中学2021届高三第三次月水平检测化学试题



