名校
1 . 工业上以铝土矿(主要成分为 ,含少量
,含少量 、
、 、
、 等杂质)为主要原料制备氧化铝,流程如下:
等杂质)为主要原料制备氧化铝,流程如下:
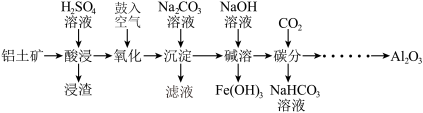
(1)酸浸:
①为提高铝土矿的酸浸率,通常可采用的方法有_______ (写出两种即可)。
②浸渣的主要成分为_______ (填化学式)。
(2)氧化:用 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为_______ ,为证明 已完全被氧化为
已完全被氧化为 ,所需的试剂为
,所需的试剂为_______ 。
(3)沉淀:用 溶液调节pH,将
溶液调节pH,将 、
、 转化为氢氧化物沉淀,溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为氢氧化物沉淀,溶液终点pH对铝、铁沉淀率的影响如图所示。
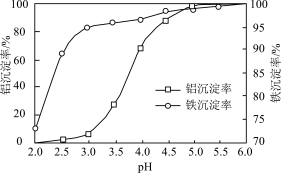
为获得较高的铝、铁沉淀率,应控制溶液pH最佳为________ 左右,其理由是_______ 。
(4)碱溶:用 溶液溶解沉淀,写出发生反应的离子方程式
溶液溶解沉淀,写出发生反应的离子方程式_______ ,分离出 的实验操作
的实验操作_______ (填名称)。
(5)碳分:向碱溶后的溶液中通入过量 气体,该反应的离子方程式为
气体,该反应的离子方程式为________ 。
 ,含少量
,含少量 、
、 、
、 等杂质)为主要原料制备氧化铝,流程如下:
等杂质)为主要原料制备氧化铝,流程如下:
(1)酸浸:
①为提高铝土矿的酸浸率,通常可采用的方法有
②浸渣的主要成分为
(2)氧化:用
 将
将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为 已完全被氧化为
已完全被氧化为 ,所需的试剂为
,所需的试剂为(3)沉淀:用
 溶液调节pH,将
溶液调节pH,将 、
、 转化为氢氧化物沉淀,溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为氢氧化物沉淀,溶液终点pH对铝、铁沉淀率的影响如图所示。
为获得较高的铝、铁沉淀率,应控制溶液pH最佳为
(4)碱溶:用
 溶液溶解沉淀,写出发生反应的离子方程式
溶液溶解沉淀,写出发生反应的离子方程式 的实验操作
的实验操作(5)碳分:向碱溶后的溶液中通入过量
 气体,该反应的离子方程式为
气体,该反应的离子方程式为
您最近半年使用:0次
解题方法
2 . 某化学实验小组欲从Al2O3、CuO、Fe2O3的混合物中分离得到Al2O3、单质铜、绿矾晶体(FeSO4·7H2O)产品。已知A、B为中学常见的化学试剂,实验流程如下,回答下列问题。
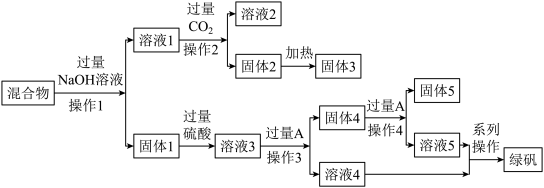
(1)完成操作2所需的玻璃仪器为_______ 。
(2)溶液3中的阳离子为_______ (填离子符号);固体4所含成分的化学式为_______ 。
(3)检验溶液4中金属阳离子的操作方法是_______ 。
(4)溶液3中加入过量试剂A时,同种元素间发生的氧化还原反应的离子方程式为_______ 。
(5)下列说法正确的是_______ 。
a.操作3和操作4的方法相同
b.试剂B可以是盐酸或稀硫酸
c.欲用纯净的绿矾晶体配制1000mL0.1mol/L的FeSO4溶液时,需称量绿矾15.2g
(6)若该小组同学取Al2O3、CuO、Fe2O3的混合物样品10.0g进行实验,假设实验过程中物质均无损失,并且流程涉及的固体均为干燥的物质。实验结束时,称得固体3为2.0g,固体5为3.2g,所得绿矾为44.48g,则初始混合物样品中铁元素的质量分数为_______ %(精确到小数点后一位)。

(1)完成操作2所需的玻璃仪器为
(2)溶液3中的阳离子为
(3)检验溶液4中金属阳离子的操作方法是
(4)溶液3中加入过量试剂A时,同种元素间发生的氧化还原反应的离子方程式为
(5)下列说法正确的是
a.操作3和操作4的方法相同
b.试剂B可以是盐酸或稀硫酸
c.欲用纯净的绿矾晶体配制1000mL0.1mol/L的FeSO4溶液时,需称量绿矾15.2g
(6)若该小组同学取Al2O3、CuO、Fe2O3的混合物样品10.0g进行实验,假设实验过程中物质均无损失,并且流程涉及的固体均为干燥的物质。实验结束时,称得固体3为2.0g,固体5为3.2g,所得绿矾为44.48g,则初始混合物样品中铁元素的质量分数为
您最近半年使用:0次
名校
解题方法
3 . 某化学兴趣小组模拟工业上从铝土矿(主要成分是 ,含
,含 、
、 等杂质)中提取氧化铝的工艺,流程如图,请回答下列问题:
等杂质)中提取氧化铝的工艺,流程如图,请回答下列问题:
已知: 不溶于强酸,但可溶于强碱。
不溶于强酸,但可溶于强碱。

(1)操作I的名称为_______ 。
(2)验证溶液B中是否含有 的方法:
的方法:_______ 。
(3)步骤①中,加入足量盐酸,盐酸与氧化铁反应的离子方程式为:_______ 。
(4)步骤②中, 与过量NaOH溶液反应的离子方程式为:
与过量NaOH溶液反应的离子方程式为:_______ 。
(5)步骤③中得到的不溶物E的化学式为_______ 。
(6)氧化铝为_______ (填字母)。
A.两性氧化物 B.酸性氧化物 C.碱性氧化物
(7)步骤④中,加热灼烧不溶物E所使用的仪器为_______(填字母)。
(8)溶液F中存在的阴离子为_______ (不考虑其中的 离子)。
离子)。
 ,含
,含 、
、 等杂质)中提取氧化铝的工艺,流程如图,请回答下列问题:
等杂质)中提取氧化铝的工艺,流程如图,请回答下列问题:已知:
 不溶于强酸,但可溶于强碱。
不溶于强酸,但可溶于强碱。
(1)操作I的名称为
(2)验证溶液B中是否含有
 的方法:
的方法:(3)步骤①中,加入足量盐酸,盐酸与氧化铁反应的离子方程式为:
(4)步骤②中,
 与过量NaOH溶液反应的离子方程式为:
与过量NaOH溶液反应的离子方程式为:(5)步骤③中得到的不溶物E的化学式为
(6)氧化铝为
A.两性氧化物 B.酸性氧化物 C.碱性氧化物
(7)步骤④中,加热灼烧不溶物E所使用的仪器为_______(填字母)。
| A.坩埚 | B.钳锅 | C.泔涡 | D.坩埚 |
 离子)。
离子)。
您最近半年使用:0次
名校
4 . 铝土矿的主要成分是Al2O3,还有部分SiO2、Fe2O3以及少量不溶于酸碱溶液的其他杂质。工业上从铝土矿中提取铝可采取如下工艺:

下列说法正确的是

下列说法正确的是
| A.沉淀Ⅰ只有SiO2 |
| B.①~⑤中包含两个氧化还原反应 |
| C.步骤②发生的反应为Al3++3OH-=Al(OH)3↓ |
| D.溶液Ⅲ中溶质主要为NaHCO3 |
您最近半年使用:0次
2023-01-21更新
|
662次组卷
|
4卷引用:吉林省“BEST合作体”2022-2023学年高一下学期期末联考化学试题
5 . 铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如图:

请回答下列问题:
(1)沉淀B的化学式为____ ,溶液C中阴离子主要是____ 。
(2)操作I是____ (填操作名称)。
(3)写出①过程中发生反应的离子方程式_____ 。
(4)Al(OH)3沉淀必须进行洗涤才能通过操作IV获得纯净Al2O3,操作IV是____ (填操作名称)。
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有____ (填化学式)。

请回答下列问题:
(1)沉淀B的化学式为
(2)操作I是
(3)写出①过程中发生反应的离子方程式
(4)Al(OH)3沉淀必须进行洗涤才能通过操作IV获得纯净Al2O3,操作IV是
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有
您最近半年使用:0次
名校
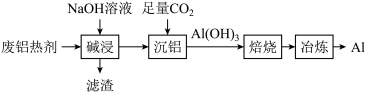
6 . 将使用过的废铝热剂(主要成分为 ,含少量
,含少量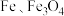 )再生制取金属铝的工艺流程如图所示。下列说法中正确的是
)再生制取金属铝的工艺流程如图所示。下列说法中正确的是
 ,含少量
,含少量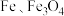 )再生制取金属铝的工艺流程如图所示。下列说法中正确的是
)再生制取金属铝的工艺流程如图所示。下列说法中正确的是
A.“碱浸”时,发生反应的化学方程式为 |
B.“沉铝”时,可以用足量HCl代替 |
| C.冶炼金属铝的方法为热还原法 |
| D.该流程中各步均不涉及氧化还原反应 |
您最近半年使用:0次
2022-10-08更新
|
483次组卷
|
4卷引用:吉林省长春市农安县2023-2024学年高三上学期零模调研化学试题
名校
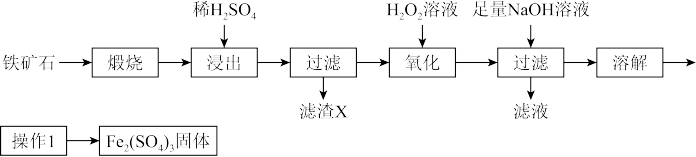
7 . 硫酸铁是一种重要的化工原料,用铁矿石(主要成分为 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下:
已知: 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。
(1)请写出“浸出”过程中 与
与 反应的离子方程式:
反应的离子方程式:_______ ;浸出时,一边加入稀硫酸,一边搅拌的目的是_______ 。
(2)“滤渣X”的成分为_______ 。
(3)“氧化”的目的是_______ ;过程中发生的离子方程式为_______ 。
(4)证明滤液中 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为_______ 。
(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为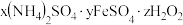 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:
步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
步骤三:另取10.00mL溶液A,加入0.0500
 酸性溶液,发生反应:
酸性溶液,发生反应: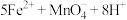
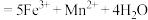 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。
通过计算确定摩尔盐中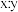 的值:
的值:_______ (写出计算过程)。
 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下:
已知:
 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。(1)请写出“浸出”过程中
 与
与 反应的离子方程式:
反应的离子方程式:(2)“滤渣X”的成分为
(3)“氧化”的目的是
(4)证明滤液中
 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为
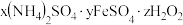 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量
 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。步骤三:另取10.00mL溶液A,加入0.0500

 酸性溶液,发生反应:
酸性溶液,发生反应: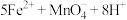
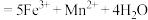 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。通过计算确定摩尔盐中
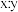 的值:
的值:
您最近半年使用:0次
2022-02-23更新
|
369次组卷
|
3卷引用:吉林省梅河口市第五中学2021-2022学年高一上学期期末联考化学试题
名校
解题方法
8 . 对废催化剂进行回收可有效利用金属资源。某废催化剂主要含 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。
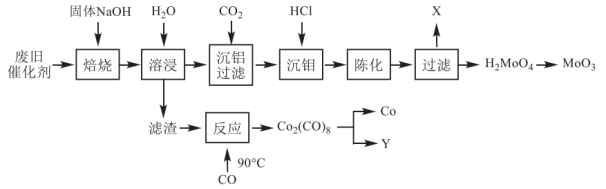
回答下列问题:
(1)“焙烧”时, 转化为
转化为 ,写出相应的化学方程式
,写出相应的化学方程式___________ 。
(2)加快溶浸速率的方法是___________ 。
(3)溶浸后的溶液中,铝元素以 的形态存在。“沉铝”时要使铝元素恰好沉淀完全时,常温下,需调节
的形态存在。“沉铝”时要使铝元素恰好沉淀完全时,常温下,需调节 为
为___________ 。(当溶液中离子浓度小于 为沉淀完全;
为沉淀完全; :
: )
)
(4)“沉钼”后,滤液X的溶质主要是___________ (写化学式)。
(5)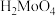 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是___________ 。
(6)已知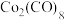 中
中 元素的化合价为0价。
元素的化合价为0价。
①写出 发生反应生成
发生反应生成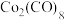 的化学方程式
的化学方程式___________ 。
②Y是一种可以循环利用的物质,Y是___________ (填化学式)。
 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。
回答下列问题:
(1)“焙烧”时,
 转化为
转化为 ,写出相应的化学方程式
,写出相应的化学方程式(2)加快溶浸速率的方法是
(3)溶浸后的溶液中,铝元素以
 的形态存在。“沉铝”时要使铝元素恰好沉淀完全时,常温下,需调节
的形态存在。“沉铝”时要使铝元素恰好沉淀完全时,常温下,需调节 为
为 为沉淀完全;
为沉淀完全; :
: )
)(4)“沉钼”后,滤液X的溶质主要是
(5)
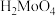 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是(6)已知
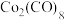 中
中 元素的化合价为0价。
元素的化合价为0价。①写出
 发生反应生成
发生反应生成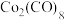 的化学方程式
的化学方程式②Y是一种可以循环利用的物质,Y是
您最近半年使用:0次
2021-12-13更新
|
1038次组卷
|
5卷引用:吉林省长春外国语学校2021-2022学年高二上学期期末考试化学试题
吉林省长春外国语学校2021-2022学年高二上学期期末考试化学试题广东省2021-2022学年高三综合能力测试(二)化学试题(已下线)专题35 物质的检验、分离和提纯(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第17周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)2022年全国甲卷高考真题变式题(非选择题)
名校
9 . 硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层。以高铝铬铁矿(主要含 和
和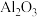 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
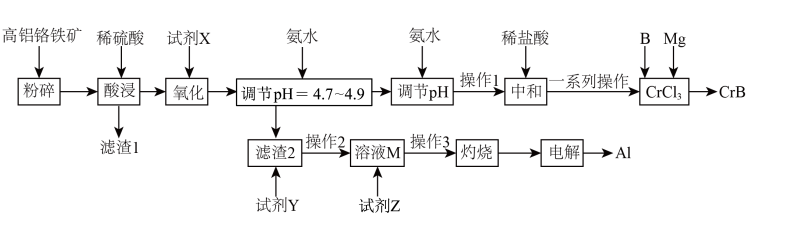
下表列出了相关金属离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)“氧化”的目的是将溶液中的 转化为
转化为 ,试剂X可选用
,试剂X可选用 或
或 ,若氧化等物质的量的
,若氧化等物质的量的 ,需要消耗
,需要消耗 和
和 的质量比为
的质量比为___________ 。
(2)试剂Y是___________ ,操作1的名称是___________ 。
(3)向M溶液中加入过量试剂Z发生反应的离子方程式为___________ 。
(4)第二次加氨水调节pH的范围是___________ ;加稀盐酸中和前,需要洗涤沉淀,证明沉淀洗涤干净的操作方法是___________ 。
(5)硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:___________ 。
 和
和 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 2.3 | 10.4 | 4.9 | 7.5 | 3.4 |
| 沉淀完全的Ph | 4.1 | 12.4 | 6.8 | 9.7 | 4.7 |
(1)“氧化”的目的是将溶液中的
 转化为
转化为 ,试剂X可选用
,试剂X可选用 或
或 ,若氧化等物质的量的
,若氧化等物质的量的 ,需要消耗
,需要消耗 和
和 的质量比为
的质量比为(2)试剂Y是
(3)向M溶液中加入过量试剂Z发生反应的离子方程式为
(4)第二次加氨水调节pH的范围是
(5)硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
您最近半年使用:0次
2021-11-17更新
|
238次组卷
|
4卷引用:吉林省通化市梅河口市第五中学2022-2023学年高三上学期10月期中考试化学试题
名校
解题方法
10 . 我国西北富产软锰矿,其主要成分为MnO2,还含有Al2O3、SiO2等杂质,是工业生产KMnO4的重要原料。某研究所设计由软锰矿制备KMnO4的生产流程如下。

已知:①K2MnO4固体和溶液的颜色均为墨绿色。
②K2MnO4溶液中存在以下平衡:3MnO +2H2O
+2H2O 2MnO
2MnO +MnO2+4OH-。回答下列问题:
+MnO2+4OH-。回答下列问题:
(1)“熔融煅烧”时,MnO2参与反应的化学方程式为___________ 。
(2)向“浸取”液中通入CO2调节其pH,经“过滤”得滤渣Ⅰ,滤渣Ⅰ成分为___________ (填化学式)。
(3)“歧化”时加入冰醋酸的目的是___________ 。“歧化”时,下列酸可以用来代替冰醋酸的有___________ (填标号)。
a.稀硫酸 b.亚硫酸 c.氢溴酸 d.乙二酸
(4)“结晶”时,当表面出现晶膜时,停止加热,___________ ,抽滤即可获得紫黑色 KMnO4晶体。
(5)KMnO4在酸性条件下能够与 Na2C2O4反应,生成Mn2+和CO2.取0.70 g上述所得产品,用0.5 mol·L-1 的Na2C2O4溶液滴定 3次,平均消耗Na2C2O4溶液20.00 mL。则 KMnO4样品的纯度为___________ %(保留 1 位小数)。

已知:①K2MnO4固体和溶液的颜色均为墨绿色。
②K2MnO4溶液中存在以下平衡:3MnO
 +2H2O
+2H2O 2MnO
2MnO +MnO2+4OH-。回答下列问题:
+MnO2+4OH-。回答下列问题:(1)“熔融煅烧”时,MnO2参与反应的化学方程式为
(2)向“浸取”液中通入CO2调节其pH,经“过滤”得滤渣Ⅰ,滤渣Ⅰ成分为
(3)“歧化”时加入冰醋酸的目的是
a.稀硫酸 b.亚硫酸 c.氢溴酸 d.乙二酸
(4)“结晶”时,当表面出现晶膜时,停止加热,
(5)KMnO4在酸性条件下能够与 Na2C2O4反应,生成Mn2+和CO2.取0.70 g上述所得产品,用0.5 mol·L-1 的Na2C2O4溶液滴定 3次,平均消耗Na2C2O4溶液20.00 mL。则 KMnO4样品的纯度为
您最近半年使用:0次



