解题方法
1 . 某待测液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 12种离子中的某几种.为探究其组成现设计如图流程.
12种离子中的某几种.为探究其组成现设计如图流程.
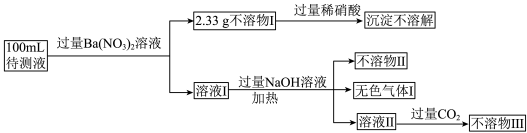
已知该待测液中所有离子的浓度均相等.
(1)待测液中
______  .
.
(2)生成不溶物Ⅰ的离子方程式为______ .
(3)不溶物Ⅱ和不溶物Ⅲ的化学式分别为______ 、______ .
(4)若向溶液Ⅰ中加入过量的稀盐酸,观察到的现象为______ ;若向不溶物Ⅲ中加入过量的NaOH溶液,反应的离子方程式为______ .
(5)待测液中一定不含的离子是______ .
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 12种离子中的某几种.为探究其组成现设计如图流程.
12种离子中的某几种.为探究其组成现设计如图流程.
已知该待测液中所有离子的浓度均相等.
(1)待测液中

 .
.(2)生成不溶物Ⅰ的离子方程式为
(3)不溶物Ⅱ和不溶物Ⅲ的化学式分别为
(4)若向溶液Ⅰ中加入过量的稀盐酸,观察到的现象为
(5)待测液中一定不含的离子是
您最近一年使用:0次
2 . 为探究由3种短周期元素构成的化合物X的性质。完成以下实验:
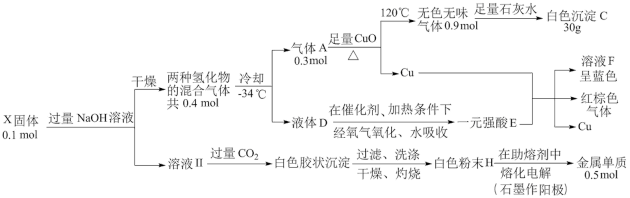
(1)X的化学式为___________ 。
(2)气体A与足量CuO反应的化学方程式为___________ 。
(3)溶液II通入过量CO2时,发生反应的离子方程式为___________ 、___________ 。
(4)将F溶液通过一系列操作获得结晶水合物(含有结晶水的盐),加热该结晶水合物。将生成的红棕色混合气体(>100°C)全部收集并冷却。气体全部反应无剩余,得到一元强酸E的水溶液(其中E与水的物质的量之比1∶1)写出该结晶水合物受热分解的化学方程式___________ 。
(5)设计实验证明F溶液的阴离子(OH—除外)___________ 。

(1)X的化学式为
(2)气体A与足量CuO反应的化学方程式为
(3)溶液II通入过量CO2时,发生反应的离子方程式为
(4)将F溶液通过一系列操作获得结晶水合物(含有结晶水的盐),加热该结晶水合物。将生成的红棕色混合气体(>100°C)全部收集并冷却。气体全部反应无剩余,得到一元强酸E的水溶液(其中E与水的物质的量之比1∶1)写出该结晶水合物受热分解的化学方程式
(5)设计实验证明F溶液的阴离子(OH—除外)
您最近一年使用:0次
解题方法
3 . 重铬酸钠是一种用途极广的氧化剂,以铬铁矿[主要成分Fe(CrO2)2,含有Al2O3、Fe2O3、SiO2等杂质]为主要原料生产重铬酸钠晶体,同时回收Cr的主要工艺流程如图:
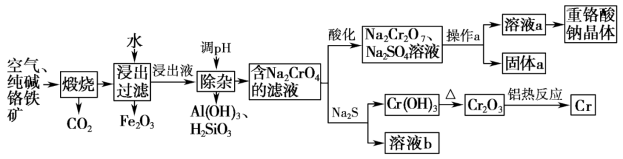
已知部分物质的溶解度曲线如图所示。
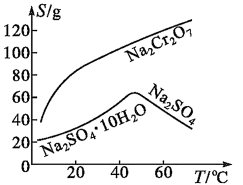
请回答下列问题:
(1)煅烧生成Na2CrO4的化学方程式为___________ 。
(2)将Fe2O3溶于稀硫酸后得到对应盐溶液,检验该溶液中金属阳离子的方法是___________ 。
(3)若通过加入稀硫酸调节溶液pH使铝元素转化为Al(OH)3,所发生反应的离子方程式为___________ 。
(4)Na2CrO4经酸化转化为Na2Cr2O7的原理为___________ (结合离子方程式用平衡移动原理解释)。
(5)操作a的实验步骤为___________ 。
(6)加入Na2S溶液反应后,硫元素全部以S2O 的形式存在,该反应中氧化剂和还原剂的物质的量之比为
的形式存在,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(7)含铬废水会对环境造成污染,要经过化学处理才能排放。现将含CrO 的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于
的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于___________ mol•L−1,CrO 才能沉淀完全[当溶液中c(CrO
才能沉淀完全[当溶液中c(CrO )≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
)≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]

已知部分物质的溶解度曲线如图所示。

请回答下列问题:
(1)煅烧生成Na2CrO4的化学方程式为
(2)将Fe2O3溶于稀硫酸后得到对应盐溶液,检验该溶液中金属阳离子的方法是
(3)若通过加入稀硫酸调节溶液pH使铝元素转化为Al(OH)3,所发生反应的离子方程式为
(4)Na2CrO4经酸化转化为Na2Cr2O7的原理为
(5)操作a的实验步骤为
(6)加入Na2S溶液反应后,硫元素全部以S2O
 的形式存在,该反应中氧化剂和还原剂的物质的量之比为
的形式存在,该反应中氧化剂和还原剂的物质的量之比为(7)含铬废水会对环境造成污染,要经过化学处理才能排放。现将含CrO
 的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于
的废水加入可溶性钡盐生成BaCrO4沉淀,加入可溶性钡盐后,废水中Ba2+的浓度应不小于 才能沉淀完全[当溶液中c(CrO
才能沉淀完全[当溶液中c(CrO )≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
)≤1×10-5 mol•L−1时,可视作该离子沉淀完全,已知Ksp(BaCrO4)=1.2×10−10]
您最近一年使用:0次
4 . 某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如图所示(部分反应物或生成物未列出),其中E为白色沉淀,I为红褐色沉淀。
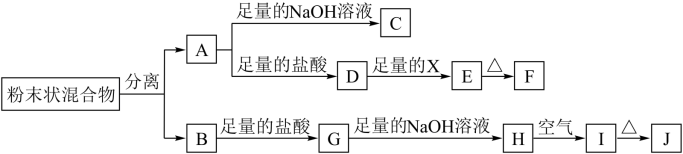
(1)写出下列物质的化学式:F___ ,G___ 。
(2)分离粉末状混合物最简单的方法是___ 。
(3)D→E转化中,加入足量的X,试剂X可能是___ ,写出其离子方程式___ 。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)A→C的离子方程式___ 。
(5)检验G溶液中的阳离子的方法___ 。

(1)写出下列物质的化学式:F
(2)分离粉末状混合物最简单的方法是
(3)D→E转化中,加入足量的X,试剂X可能是
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)A→C的离子方程式
(5)检验G溶液中的阳离子的方法
您最近一年使用:0次
5 . 铝元素含量居金属首位,主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领域应用广泛。
Ⅰ、工业上用铝土矿制备铝的某种化合物的工艺流程如下:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
Fe2++□ClO-+□ ═□Fe(OH)3↓+□Cl-+□__________
②检验滤液B中是否还含有铁元素的方法为:_________________________
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________ (选填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、__________ (填操作名称)、过滤、洗涤。
Ⅱ、明矾(KAl(SO4)2·12H2O)在日常生活、生产中也占有一席之地。
(1)明矾曾经是净水明星,用离子方程式表示其净水原理_____________________________ 。
(2)明矾净水时,若不慎过量会有一定程度的副作用。将含有明矾的水溶液中加入Ba(OH)2溶液至铝离子恰好完全沉淀,并且过滤,就可以避免,请用离子反方程式描述其过程______________ 。
Ⅰ、工业上用铝土矿制备铝的某种化合物的工艺流程如下:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
Fe2++□ClO-+□ ═□Fe(OH)3↓+□Cl-+□
②检验滤液B中是否还含有铁元素的方法为:
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
Ⅱ、明矾(KAl(SO4)2·12H2O)在日常生活、生产中也占有一席之地。
(1)明矾曾经是净水明星,用离子方程式表示其净水原理
(2)明矾净水时,若不慎过量会有一定程度的副作用。将含有明矾的水溶液中加入Ba(OH)2溶液至铝离子恰好完全沉淀,并且过滤,就可以避免,请用离子反方程式描述其过程
您最近一年使用:0次
2017-11-30更新
|
917次组卷
|
4卷引用:山西省吕梁市2018届高三上学期第一次阶段性测试化学试题
山西省吕梁市2018届高三上学期第一次阶段性测试化学试题陕西省延安市吴起高级中学2019-2020学年高二下学期第三次质量检测化学试题(已下线)第6讲 铝及其化合物-2021年高考化学一轮复习名师精讲练安徽省定远县育才学校2021届高三8月月考化学试题
6 . 铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下:
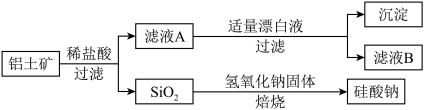
(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是___________ (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_________(填代号)。
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)。
①由滤液B制备氯化铝晶体(将AlCl3·6H2O)涉及的操作为_______ 、冷却结晶、________ (填操作名称)、洗涤。
②将AlCl3·6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的________ (填序号)。
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_____ (填代号)。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是___________ (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_________(填代号)。
| A.氢氧化钠溶液 | B.硫酸溶液 | C.氨水 | D.二氧化碳 |
①由滤液B制备氯化铝晶体(将AlCl3·6H2O)涉及的操作为_______ 、冷却结晶、________ (填操作名称)、洗涤。
②将AlCl3·6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的________ (填序号)。
| A.氧化性 | B.吸水性 | C.脱水性 |
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
7 . 某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子,并尽可能减少AlCl3的损失.请回答下列问题:

(1)混合物溶液中需加入足量氢氧化钠溶液,该氢氧化钠溶液为什么不能用氨水代替? .
(2)溶液a中存在的离子有 ;在溶液a中加入盐酸时需控制盐酸的用量,为什么? ;为此,改进方法是 ,写出该反应的离子方程式是 .

(1)混合物溶液中需加入足量氢氧化钠溶液,该氢氧化钠溶液为什么不能用氨水代替? .
(2)溶液a中存在的离子有 ;在溶液a中加入盐酸时需控制盐酸的用量,为什么? ;为此,改进方法是 ,写出该反应的离子方程式是 .
您最近一年使用:0次
8 . 已知B、C为用途广泛的金属,H具有磁性氧化物,I是一种白色胶状沉淀,它们有如图所示的转化关系(部分产物未列出):

回答下列问题:
(1).E和G的化学式分别为_______ 。
(2).写出反应的化学方程式:①_______ 、③_______ 。
(3)写出反应的离子方程式②_______ 、④_______ 。

回答下列问题:
(1).E和G的化学式分别为
(2).写出反应的化学方程式:①
(3)写出反应的离子方程式②
您最近一年使用:0次



