名校
1 . 下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向NaAlO2溶液中滴加AlCl3溶液,无明显现象 | NaAlO2与AlCl3不反应 |
| C | 将Na加入CuSO4溶液中,生成红色沉淀 | Na与CuSO4发生置换反应 |
| D | 向饱和Na2CO3中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-09-11更新
|
200次组卷
|
2卷引用:【全国百强校】宁夏回族自治区育才中学2019届高三上学期第一次月考化学试题
解题方法
2 . 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。请回答下列问题:
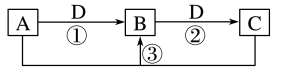
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式是___________ ;工业上制取A的离子方程式为___________ 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为___________ 。将B、C的混合气体溶于氢氧化钠溶液中的化学方程式___________ 。
(3)若D是氯碱工业的主要产品之一,B物质具有两性,则反应②的离子方程式是___________ 。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___________ 。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:___________ 。

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式是
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
(3)若D是氯碱工业的主要产品之一,B物质具有两性,则反应②的离子方程式是
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途。完成下列填空:
(1) 实验室配制氯化铝溶液时加入盐酸的目的是____________ 。
(2)往AlCl3溶液中加入过量下列溶液,最终得到无色澄清溶液的是______ (填编号)。
a Na2CO3 b NaOH c NaAlO2 d H2SO4
取AlCl3溶液,用小火持续加热至水刚好蒸干,生成白色固体的组成可表示为:Al2(OH)nCl(6-n),为确定n的值,取3.490g白色固体,全部溶解在0.1120 mol的HNO3(足量)中,并加水稀释成100 mL,将溶液分成两等价,进行如下实验:
(3)一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得Al2O3的质量为1.020g。判断加入氨水已足量的操作是________ 。过滤、洗涤后至少要灼烧_______ 次(填写数字);测定样品中铝元素含量时不选择测定干燥Al(OH)3的质量,而是测定A12O3的质量的原因可能是____ (选填编号)。
a 干燥Al(OH)3固体时易失水 b Al2O3的质量比Al(OH)3大,误差小
c 沉淀Al(OH)3时不完全 d 灼烧氧化铝时不分解
(4)从另一份溶液中取出20.00 mL,用0.1290 mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00 mL,终点时滴定管液面(局部)如图所示(背景为白底蓝线的滴定管)。则滴定管的读数__________ mL,Al2(OH)nCl(6-n)中n的值为__________ 。

(1) 实验室配制氯化铝溶液时加入盐酸的目的是
(2)往AlCl3溶液中加入过量下列溶液,最终得到无色澄清溶液的是
a Na2CO3 b NaOH c NaAlO2 d H2SO4
取AlCl3溶液,用小火持续加热至水刚好蒸干,生成白色固体的组成可表示为:Al2(OH)nCl(6-n),为确定n的值,取3.490g白色固体,全部溶解在0.1120 mol的HNO3(足量)中,并加水稀释成100 mL,将溶液分成两等价,进行如下实验:
(3)一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得Al2O3的质量为1.020g。判断加入氨水已足量的操作是
a 干燥Al(OH)3固体时易失水 b Al2O3的质量比Al(OH)3大,误差小
c 沉淀Al(OH)3时不完全 d 灼烧氧化铝时不分解
(4)从另一份溶液中取出20.00 mL,用0.1290 mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00 mL,终点时滴定管液面(局部)如图所示(背景为白底蓝线的滴定管)。则滴定管的读数

您最近一年使用:0次
2020-03-24更新
|
177次组卷
|
2卷引用:四川省泸县第四中学2020届高三下学期第二次高考适应性考试理综化学试题
名校
解题方法
4 . A、B、C、D是中学化学中的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如右图所示(反应中的其他产物已略去)。请填空:

(1)若B是常见的两性氢氧化物
①若D是强酸,则能确定A中肯定含的离子的化学式是________ 。
②若D是强碱,则反应②的离子方程式是___________________________ 。
(2)若A为淡黄色固体单质,D为空气中的主要成分,则请写出A与C的浓溶液发生反应的化学方程式___________________________ 。
(3)若A、B、C的的焰色反应都呈黄色,D是一种无色无味的气态酸性氧化物,则反应③的离子方程式是______________________________ 。
(4)若D是生产、生活中用量最大、用途最广的金属单质
①若A可用于自来水消毒,则请写出工业制取A的化学方程式______________ 。
②若A是某强酸的稀溶液,则A的化学式可能是_________ 。

(1)若B是常见的两性氢氧化物
①若D是强酸,则能确定A中肯定含的离子的化学式是
②若D是强碱,则反应②的离子方程式是
(2)若A为淡黄色固体单质,D为空气中的主要成分,则请写出A与C的浓溶液发生反应的化学方程式
(3)若A、B、C的的焰色反应都呈黄色,D是一种无色无味的气态酸性氧化物,则反应③的离子方程式是
(4)若D是生产、生活中用量最大、用途最广的金属单质
①若A可用于自来水消毒,则请写出工业制取A的化学方程式
②若A是某强酸的稀溶液,则A的化学式可能是
您最近一年使用:0次
2020-10-12更新
|
159次组卷
|
2卷引用:福建省福州市第四中学2021届高三10月月考化学试题
名校
5 . A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途:___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:________ 。
(3)若D物质具有两性,②、③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:_________ 。
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同主族,且溶液均显碱性,其中C可用作粘合剂。写出④反应的化学方程式:______ 。
(5)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于刻蚀印刷铜电路板,写出该反应的离子方程式:______ 。

(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途:
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:
(3)若D物质具有两性,②、③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同主族,且溶液均显碱性,其中C可用作粘合剂。写出④反应的化学方程式:
(5)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于刻蚀印刷铜电路板,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
6 . 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。请回答下列问题:

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。则B的化学式为__ 。
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是__ 。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___ 。
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是___ 。

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。则B的化学式为
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是
您最近一年使用:0次
解题方法
7 . 如图所示中学化学中常见物质的实验转化过程,部分物质和反应条件略去。

(1)写出F的化学式______ ;写出物质A的一种用途______ ;
(2)写出单质B与强碱溶液反应的离子方程式______ ,写出沉淀J生成H溶液的离子方程式______ ;
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式______ ;
(4)溶液I中所含金属离子是______ 。

(1)写出F的化学式
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式
(4)溶液I中所含金属离子是
您最近一年使用:0次
名校
解题方法
8 . 工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如图:

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式___ 。
(2)沉淀C的化学式___ ,颜色为___ ,写出它的一种用途___ 。
(3)操作I、操作II、操作III的名称为___ ,这个过程用到的玻璃仪器有烧杯、___ 。
(4)整个生产过程中,除可以循环使用的物质有___ (写出3种,填化学式),用此法制取铝的副产品是___ (写出2种,填化学式)。
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?___ 。

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式
(2)沉淀C的化学式
(3)操作I、操作II、操作III的名称为
(4)整个生产过程中,除可以循环使用的物质有
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?
您最近一年使用:0次
2020-03-24更新
|
415次组卷
|
5卷引用:上海市闵行区华二中学2017-2018学年高二上学期期中考试化学试题
上海市闵行区华二中学2017-2018学年高二上学期期中考试化学试题(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
解题方法
9 . 甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系 其它产物已略去
其它产物已略去 。
。

 若丁为KOH溶液,写出乙的一种用途
若丁为KOH溶液,写出乙的一种用途________ ,甲 丙的离子方程式为
丙的离子方程式为________ 。
 若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式:
若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式:________ ;该实验现象为________ 。
 若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为
若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为________ 。
 其它产物已略去
其它产物已略去 。
。 
 若丁为KOH溶液,写出乙的一种用途
若丁为KOH溶液,写出乙的一种用途 丙的离子方程式为
丙的离子方程式为 若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式:
若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式: 若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为
若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为
您最近一年使用:0次
10 . 已知A~K均为中学化学的常见物质,它们之间的转化关系如下图所示,其中A、D为金属单质,反应过程中生成的水及其他部分产物已略去。

请回答以下问题:
(1)B的主要用途是______________ (填一项),C的化学式为__________ 。
(2)E中阳离子的结构示意图为____________ ,CO2的电子式为________________ 。
(3)向F中通入足量CO2生成K的离子方程式是______________________________ 。
(4)J在工业上可用于净水,其原理是_____________________ (用离子方程式表示)。
(5)写出H在空气中生成I的化学方程式________________________ 。

请回答以下问题:
(1)B的主要用途是
(2)E中阳离子的结构示意图为
(3)向F中通入足量CO2生成K的离子方程式是
(4)J在工业上可用于净水,其原理是
(5)写出H在空气中生成I的化学方程式
您最近一年使用:0次



