名校
解题方法
1 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
| B.维生素C具有还原性,可用作食品抗氧化剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近一年使用:0次
2023-08-22更新
|
235次组卷
|
2卷引用:贵州省贵阳市2024届高三上学期开学考试化学试题
2 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
B. 吸收 吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近一年使用:0次
3 . 表中用途与其性质或原理对应关系错误的是
| 选项 | 现象或事实 | 解释 |
| A | 光导纤维的主要成分是二氧化硅 | 二氧化硅有导电性 |
| B | 液氨可以作制冷剂 | 液氨汽化大量吸热 |
| C | FeCl3溶液可用于刻制印刷铜电路板 | FeCl3可与Cu发生反应 |
| D | 铁制器皿用作盛放浓硫酸的容器 | 铁能被浓硫酸钝化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-22更新
|
230次组卷
|
5卷引用:贵州省“三新”改革联盟校2021-2022学年高一下学期联考试题(四) 化学试题
4 . 下列物质的性质与用途对应关系正确的是
| A.浓硫酸具有吸水性,可用于干燥二氧化硫 |
| B.氯化钙能够吸水,可用作豆腐制作过程中的凝固剂 |
| C.明矾和小苏打两种溶液混合会产生大量泡沫,可用于电器灭火 |
| D.FeCl3易溶于水,可用于印刷电路板回收铜 |
您最近一年使用:0次
2021-09-23更新
|
90次组卷
|
2卷引用:贵州省遵义市2022届高三上学期第一联考化学试题
名校
解题方法
5 . 下列有关物质的性质与用途具有对应关系的是
| A.Al2O3具有两性,可用作耐高温材料 |
| B.NaHCO3溶液呈碱性,可用于制备纯碱 |
| C.铝具有良好导热性,可用作贮运浓硝酸 |
| D.FeCl3溶液具有氧化性,可用作蚀刻铜电路板 |
您最近一年使用:0次
2020-07-22更新
|
278次组卷
|
5卷引用:贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题
真题
名校
6 . 下列有关物质的性质与用途具有对应关系的是
| A.SO2具有氧化性,可用于漂白纸浆 | B.NH4HCO3受热易分解,可用作氮肥 |
| C.Fe2(SO4)3易溶于水,可用作净水剂 | D.Al2O3熔点高,可用作耐高温材料 |
您最近一年使用:0次
2019-01-30更新
|
1653次组卷
|
37卷引用:贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题
贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2015-2016学年江西省樟树中学、高安二中高二下期末化学试卷2015-2016学年山东省桓台二中高二下期末化学试卷2017届黑龙江省哈尔滨六中高三上9月月考化学试卷2017届广西桂林十八中高三上10月月考化学试卷2016-2017学年山东省淄博市淄川中学高二下学期学分认定(期中)考试化学试卷山西省晋中市名校2016-2017学年高一下学期期中考试化学试题湖北省仙桃市汉江高级中学2016-2017学年高一下学期期中考试化学试题2018版化学(苏教版)高考总复习专题一对接高考精练--物质的组成、性质及分类辽宁省庄河市高级中学2018届高三上学期开学考试化学试题河北省衡水中学2018届高三上学期一调考试化学试题(已下线)二轮复习 专题1 物质的组成、性质、分类与化学用语 押题专练江苏省泰州中学2017-2018学年高二上学期期末考试化学试题云南民族大学附属中学2017-2018学年高一下学期第一次月考化学试题(已下线)解密01 物质的组成、性质和分类 化学用语——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】广东省蓝精灵中学2018-2019学年高二上学期联考化学试题安徽省白泽湖中学2017届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第3讲 铁及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第2讲 铝及其化合物(已下线)2018年12月30日 《每日一题》 高考二轮复习-每周一测(已下线)2019高考备考二轮复习精品资料-专题1 物质的组成、性质、分类与化学用语(押题专练)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)上海交通大学附属中学2018-2019学年高二上学期期中考试化学试题福建省厦门双十中学2018届高三期中考试化学试题上海市上海财经大学附属中学2019——2020学年高三上学期期中考试化学试题福建省三明第一中学2020届高三上学期第二次月考化学试题福建省永春第一中学2018-2019学年高二下学期期末考试化学试题上海市青浦区高级中学2017-2018学年高三上学期期中考试化学试题(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训上海市黄浦区2019-2020学年高三下学期学业等级考科目阶段性调研化学试题江苏省扬州市江都区大桥高级中学2019-2020学年高二下学期期中考试化学试题陕西省西安市西航一中2021~2022学年高一上学期期末考试化学试题上海市奉贤区致远高级中学2021-2022学年高二上学期期中教学评估(等级考)化学试题
名校
7 . 化学与生产、实验密切相关。下列有关物质的性质与用途具有对应关系的是( )
A. 熔点高,可用作耐高温材料 熔点高,可用作耐高温材料 |
B. 溶液呈酸性,可用于腐蚀电路板上的 溶液呈酸性,可用于腐蚀电路板上的 |
| C.石墨具有导电性,可用于制铅笔芯 |
D.浓硫酸具有强氧化性,可用于干燥 |
您最近一年使用:0次
2020-04-28更新
|
582次组卷
|
15卷引用:【校级联考】贵州省遵义市第四教育集团2019届高三上学期第二次联考理综化学试题
【校级联考】贵州省遵义市第四教育集团2019届高三上学期第二次联考理综化学试题江苏省泰州市2018届高三第一次调研化学试题甘肃省白银市第一中学2018届高三3月测试化学试题江苏省启东市2020届高三上学期期中考试化学试题2019届上海奉贤区高考第一次模拟化学试题湖南省永州市祁阳县2018-2019学年高二上学期期末考试化学试题2020届上海市奉贤区高考化学一模试卷江苏省海安高级中学2020届高三模拟考试化学试题江苏省海安高级中学2020届高三调研考试化学试题天津市河西区2020芦台一中高三模拟测试江苏省扬州中学2021届高三上学期12月月考化学试题江苏省邗江中学2020-2021学年高二(2019级新疆班)下学期期中化学试题重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题江苏省泰兴市第一高级中学2021-2022学年高二下学期第一次阶段测试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高三上学期第一次月考化学试题
解题方法
8 . 下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 | 操作和现象 | 结论 |
| A | 向某溶液中加盐酸酸化,再滴加 溶液,产生白色沉淀且沉淀不溶解 溶液,产生白色沉淀且沉淀不溶解 | 该溶液中一定含有 |
| B | 向某溶液中先加氯水,再滴加 溶液,溶液变红 溶液,溶液变红 | 该溶液中一定含有 |
| C | 向土豆片上滴加碘溶液,土豆片变蓝 | 淀粉遇碘元素变蓝 |
| D | 向某盐溶液中加入 溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 铁及其化合物在日常生产生活中用途广泛,利用FeSO4制备还原铁粉的工业流程如图:

实验室中可用FeSO4(由铁粉和稀硫酸反应制得)和NH4HCO3用如图装置模拟上述流程中的“转化”环节。
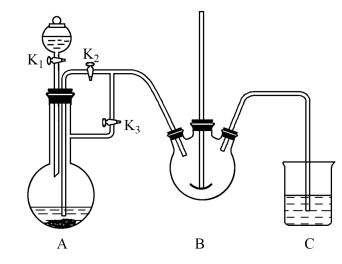
回答下列问题:
(1)配制溶液所用的蒸馏水须先除去其中溶解的氧气,具体方法是___________ 。
(2)装置A用于制备FeSO4,实验过程中,欲将生成的FeSO4溶液与装置B中的NH4HCO3溶液混合,操作方法是关闭___________ ,打开___________ (填“K1”、“K2”或“K3”);装置B中生成FeCO3的离子方程式为___________ 。
(3)转化过程中温度不超过35℃,主要原因是___________ ;“过滤”环节,不需要使用下列仪器中的___________ (填仪器名称)。

(4)干燥过程的主要目的是脱去游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为___________ ;检验产品中是否含Fe3+需要的试剂有稀H2SO4和___________ (填化学式)。
(5)取干燥后的FeCO3样品(含少量FeOOH)37.47g,与炭混合后焙烧,最终得到还原铁粉18.48g,计算样品中FeCO3的质量分数为___________ %(计算结果取整数)。

实验室中可用FeSO4(由铁粉和稀硫酸反应制得)和NH4HCO3用如图装置模拟上述流程中的“转化”环节。

回答下列问题:
(1)配制溶液所用的蒸馏水须先除去其中溶解的氧气,具体方法是
(2)装置A用于制备FeSO4,实验过程中,欲将生成的FeSO4溶液与装置B中的NH4HCO3溶液混合,操作方法是关闭
(3)转化过程中温度不超过35℃,主要原因是

(4)干燥过程的主要目的是脱去游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为
(5)取干燥后的FeCO3样品(含少量FeOOH)37.47g,与炭混合后焙烧,最终得到还原铁粉18.48g,计算样品中FeCO3的质量分数为
您最近一年使用:0次
2022-03-22更新
|
614次组卷
|
2卷引用:贵州省贵阳市2022届高三一模理综化学试卷
解题方法
10 . 明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:
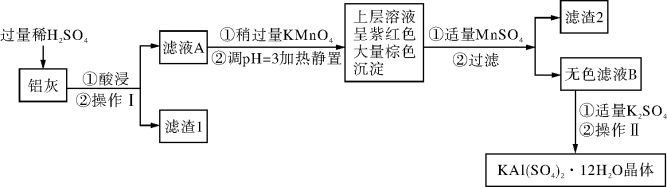
回答下列问题:
(1)明矾净水的原理是___________ (用离子方程式表示)。
(2)操作Ⅰ是___________ ,滤液B中K+焰色反应颜色为:___________ 。
(3)检验滤液A中是否存在Fe2+的试剂是___________ (只用一种试剂)。
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为___________ 。
已知:生成氢氧化物沉淀的pH如下表所示:
注:金属离子的起始浓度为0.1 mol·L-1。
根据表中数据解释调节pH=3的目的:___________ 。
(5)已知:在pH=3、加热条件下,MnO 可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为:
可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为:___________ 。滤渣2含有的物质是___________ 。

回答下列问题:
(1)明矾净水的原理是
(2)操作Ⅰ是
(3)检验滤液A中是否存在Fe2+的试剂是
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为
已知:生成氢氧化物沉淀的pH如下表所示:
| 物质 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1。
根据表中数据解释调节pH=3的目的:
(5)已知:在pH=3、加热条件下,MnO
 可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为:
可与Mn2+反应生成MnO2,加入MnSO4发生反应的离子方程式为:
您最近一年使用:0次



