解题方法
1 . 下列化学用语解释事实或过程正确的是
A.用含 Al粉和 NaOH疏通剂疏通管道: |
B.用FeCl3溶液刻蚀覆铜板制作印刷电路板:  |
C.用石灰乳制漂白粉: 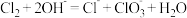 |
D.用 NaOH 溶液吸收  |
您最近一年使用:0次
解题方法
2 . 常温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液: 溶液: 、 、 、 、 |
B. 稀硫酸: 稀硫酸: 、 、 、 、 |
C. 溶液: 溶液: 、 、 、 、 |
D. 溶液: 溶液: 、 、 、 、 |
您最近一年使用:0次
解题方法
3 . 以锌灰(含ZnO及少量PbO、CuO、Fe2O3、SiO2)和Fe2(SO4)3为原料制备的ZnFe2O4脱硫剂,可用于脱除煤气中的H2S。脱硫剂的制备过程可表示为
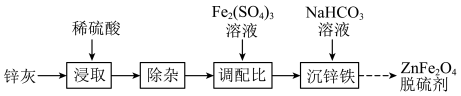
(1)“浸取”时需不断通入高温水蒸气,其目的是___________ 。
(2)“除杂”包括:向浸取后的滤液中加足量锌粉、过滤、加H2O2氧化等步骤。过滤所得滤渣的成分为(填化学式)___________ 。
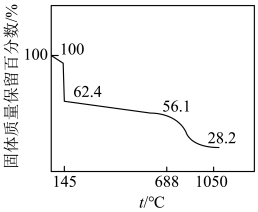
(3)ZnSO4溶液经结晶可得ZnSO4∙7H2O固体。加热该固体,固体质量保留百分数与温度的关系如图所示。温度从688℃升高到1050℃时,分解生成的产物中有两种气体(只有一种是氧化物),该过程中发生反应的化学方程式为___________ 。
(4)400℃时,将一定比例H2、H2S的混合气体以一定流速通过装有ZnFe2O4脱硫剂的硫化反应器进行硫化。已知:硫化过程中ZnFe2O4反应后生成ZnS和FeS,该过程中发生的化学反应方程式为______________________ 。
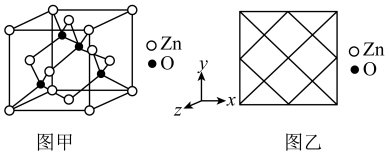
(5)①氧化锌晶体的一种晶胞是如图甲所示的立方晶胞,其中与Zn原子距离最近的O原子数目有___________ 个,请在图乙中画出该晶胞沿y轴方向的平面投影图___________ 。
②Zn2+能形成多种配离子,已知Zn2+形成的一种配离子[Zn(NH3)2(H2O)2]2+只有一种空间结构,则[Zn(NH3)4]2+的空间结构为___________ 。

(1)“浸取”时需不断通入高温水蒸气,其目的是
(2)“除杂”包括:向浸取后的滤液中加足量锌粉、过滤、加H2O2氧化等步骤。过滤所得滤渣的成分为(填化学式)
(3)ZnSO4溶液经结晶可得ZnSO4∙7H2O固体。加热该固体,固体质量保留百分数与温度的关系如图所示。温度从688℃升高到1050℃时,分解生成的产物中有两种气体(只有一种是氧化物),该过程中发生反应的化学方程式为

(4)400℃时,将一定比例H2、H2S的混合气体以一定流速通过装有ZnFe2O4脱硫剂的硫化反应器进行硫化。已知:硫化过程中ZnFe2O4反应后生成ZnS和FeS,该过程中发生的化学反应方程式为
(5)①氧化锌晶体的一种晶胞是如图甲所示的立方晶胞,其中与Zn原子距离最近的O原子数目有

②Zn2+能形成多种配离子,已知Zn2+形成的一种配离子[Zn(NH3)2(H2O)2]2+只有一种空间结构,则[Zn(NH3)4]2+的空间结构为
您最近一年使用:0次
解题方法
4 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向[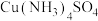 ]溶液中加入乙醇,析出深蓝色固体 ]溶液中加入乙醇,析出深蓝色固体 | [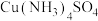 ]与乙醇反应生成了难溶于水的物质 ]与乙醇反应生成了难溶于水的物质 |
| B | 向 溶液中滴加几滴KSCN溶液,振荡,无明显现象,再滴加几滴新制氯水,溶液变红 溶液中滴加几滴KSCN溶液,振荡,无明显现象,再滴加几滴新制氯水,溶液变红 | 一定是 将 将 氧化为 氧化为 |
| C | 向蔗糖溶液中加入稀硫酸,加热。待溶液冷却后向其中加入少量新制 ,加热未产生砖红色沉淀 ,加热未产生砖红色沉淀 | 蔗糖没有发生水解 |
| D | 向溴水中加入植物油,振荡后静置,水层颜色变浅,油层呈无色 |  与植物油发生了反应 与植物油发生了反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从高铟灰渣(主要含PbO、SiO2、FeAsO4·2H2O、In2O3)中提取铟的工艺流程如下:

已知:FeS4O6为强电解质;P2O4为磷酸二异辛酯;Ksp[In(OH)3]=1.4×10-33。回答下列问题:
(1)FeAsO4·2H2O中铁元素化合价为+3价,As的化合价为___________ 。Fe3+的价层电子排布式___________ 。
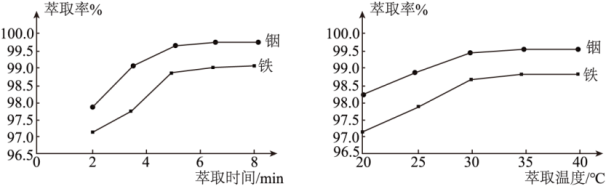
(2)“硫酸化焙烧”后金属元素均以硫酸盐的形式存在。在其他条件一定时,“水浸”铟、铁的萃取率结果如图所示,则萃取所采用的最佳条件为:萃取时间___________ ,萃取温度___________ 。
(3)“水浸”时,浸渣除了As2O3外,还含有___________ 。
(4)“还原铁”时反应的离子方程式为___________ 。
(5)“萃取除铁”时,用30%的P2O4作萃取剂时,发现当溶液pH >1.5后,铟萃取率随pH值的升高而下降,原因是___________ 。
(6)“萃取”过程中用酸(用H2A2表示)作萃取剂,使In3+进入有机相,发生反应:In3++3H2A2 In(HA2)3+3H+,平衡常数为K。已知c(H+)与萃取率(E%)的关系符合公式:
In(HA2)3+3H+,平衡常数为K。已知c(H+)与萃取率(E%)的关系符合公式: 。当pH = 2.30 时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH = 2.30 时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=___________ (已知lg19 =1.28,忽略萃取剂浓度的变化,结果保留三位有效数字)。
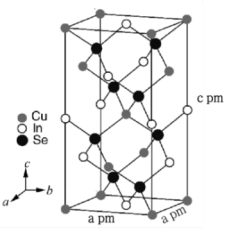
(7)立方晶系CuInSe2的晶胞结构如图所示,晶胞参数如图。CuInSe2的相对分子质量为M,则该晶体密度ρ=___________ g·cm-3(用含M、NA的式子表示),与In原子最近且距离相等的Se原子个数为___________ 。

已知:FeS4O6为强电解质;P2O4为磷酸二异辛酯;Ksp[In(OH)3]=1.4×10-33。回答下列问题:
(1)FeAsO4·2H2O中铁元素化合价为+3价,As的化合价为
(2)“硫酸化焙烧”后金属元素均以硫酸盐的形式存在。在其他条件一定时,“水浸”铟、铁的萃取率结果如图所示,则萃取所采用的最佳条件为:萃取时间

(3)“水浸”时,浸渣除了As2O3外,还含有
(4)“还原铁”时反应的离子方程式为
(5)“萃取除铁”时,用30%的P2O4作萃取剂时,发现当溶液pH >1.5后,铟萃取率随pH值的升高而下降,原因是
(6)“萃取”过程中用酸(用H2A2表示)作萃取剂,使In3+进入有机相,发生反应:In3++3H2A2
 In(HA2)3+3H+,平衡常数为K。已知c(H+)与萃取率(E%)的关系符合公式:
In(HA2)3+3H+,平衡常数为K。已知c(H+)与萃取率(E%)的关系符合公式: 。当pH = 2.30 时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH = 2.30 时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=(7)立方晶系CuInSe2的晶胞结构如图所示,晶胞参数如图。CuInSe2的相对分子质量为M,则该晶体密度ρ=

您最近一年使用:0次
2024-01-28更新
|
394次组卷
|
2卷引用:福建省厦门双十中学2024届高三模拟预测化学试题
名校
解题方法
6 . 下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生的离子反应 |
| A |  、 、 、 、 |  溶液 溶液 | 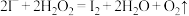 |
| B |  、 、 、 、 |  溶液 溶液 |  |
| C |  、 、 、 、 |  溶液 溶液 |  |
| D |  、 、 、 、 | NaOH溶液 | 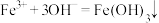 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-10更新
|
732次组卷
|
4卷引用:福建省南平市2023届高中毕业班第三次质量检测化学试题
名校
7 . 下列操作能实现相应的实验目的的是
| 选项 | 实验目的 | 操作步骤及现象 |
| A | 验证淀粉水解生成葡萄糖 | 将淀粉和稀硫酸混合水浴加热一段时间;待溶液冷却后,加入NaOH溶液,调pH至碱性,再加入新制的 ,加热,有砖红色沉淀产生 ,加热,有砖红色沉淀产生 |
| B | 证明某钠盐为 或 或 | 向某钠盐中滴加浓盐酸,并将产生的气体通入品红溶液中,品红溶液褪色 |
| C | 除去乙醇中混有的少量乙酸 | 向混合液中加入饱和 溶液,分液 溶液,分液 |
| D | 证明氧化性: | 将硫酸酸化的 滴入 滴入 溶液中,再滴入KSCN溶液,溶液变红 溶液中,再滴入KSCN溶液,溶液变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-23更新
|
541次组卷
|
3卷引用:福建省百校联盟2023届高三第三次模拟考试化学试题
解题方法
8 . 实验小组探究 和
和 溶液的反应原理。
溶液的反应原理。
(1)配制溶液
用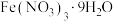 标准试剂配制
标准试剂配制 溶液,下列仪器中无需使用的有
溶液,下列仪器中无需使用的有_______ (填名称)。

(2) 溶液成分探究
溶液成分探究
甲同学认为溶质离子主要成分为 和
和 ,乙同学认为还有
,乙同学认为还有 ,于是用
,于是用_______ (填仪器名称)测得 溶液
溶液 为1.10。
为1.10。
(3)提出假设
假设ⅰ:_______ ,发生:
假设ⅱ: 将
将 氧化,发生:
氧化,发生:
(4)实验探究
实验Ⅰ:向 溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组通过实验证明了反应中有
溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组通过实验证明了反应中有 生成,实验方案为
生成,实验方案为_______ 。
实验Ⅱ:向 的
的_______ 溶液中加入过量铜粉并充分振荡,无明显现象。综合“实验Ⅰ”和“实验Ⅱ”可知,假设_______ 成立。
(5)查阅资料知,铜粉与 溶液可能涉及的反应有:
溶液可能涉及的反应有:
反应①: ;
;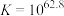 ;速率很慢。
;速率很慢。
反应②: ;
;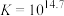 ;速率较快。
;速率较快。
反应③: (深棕色)
(深棕色) ;
;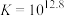 ;速率很快。
;速率很快。
反应④: (深棕色)
(深棕色)
(ⅰ)对反应①来说, 起到的作用为
起到的作用为_______ ;为验证这一作用,设计实验方案为_______ 。
(ⅱ)“实验Ⅰ”反应中无论 过量多少,始终都能检测到
过量多少,始终都能检测到 的存在,原因是
的存在,原因是_______ 。
 和
和 溶液的反应原理。
溶液的反应原理。(1)配制溶液
用
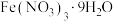 标准试剂配制
标准试剂配制 溶液,下列仪器中无需使用的有
溶液,下列仪器中无需使用的有
(2)
 溶液成分探究
溶液成分探究甲同学认为溶质离子主要成分为
 和
和 ,乙同学认为还有
,乙同学认为还有 ,于是用
,于是用 溶液
溶液 为1.10。
为1.10。(3)提出假设
假设ⅰ:

假设ⅱ:
 将
将 氧化,发生:
氧化,发生:
(4)实验探究
实验Ⅰ:向
 溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组通过实验证明了反应中有
溶液中加入过量铜粉并充分振荡,溶液变成深棕色,无气泡产生。实验小组通过实验证明了反应中有 生成,实验方案为
生成,实验方案为实验Ⅱ:向
 的
的(5)查阅资料知,铜粉与
 溶液可能涉及的反应有:
溶液可能涉及的反应有:反应①:
 ;
;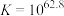 ;速率很慢。
;速率很慢。反应②:
 ;
;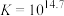 ;速率较快。
;速率较快。反应③:
 (深棕色)
(深棕色) ;
;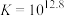 ;速率很快。
;速率很快。反应④:
 (深棕色)
(深棕色)
(ⅰ)对反应①来说,
 起到的作用为
起到的作用为(ⅱ)“实验Ⅰ”反应中无论
 过量多少,始终都能检测到
过量多少,始终都能检测到 的存在,原因是
的存在,原因是
您最近一年使用:0次
名校
9 . 中药材铁华粉的主要成分是(CH3COO)2Fe,其检测流程如图所示。下列说法正确的是


| A.刺激性气体X为SO2 |
| B.铁华粉中可能含有铁单质 |
| C.向滤液中滴加酸性KMnO4溶液,一定能证明Fe2+具有还原性 |
| D.滤液中加入K3[Fe(CN)6]试液,产生蓝色沉淀说明溶液中含有Fe3+ |
您最近一年使用:0次
2022-05-06更新
|
467次组卷
|
4卷引用:化学(福建B卷)-学易金卷:2023年高考第一次模拟考试
(已下线)化学(福建B卷)-学易金卷:2023年高考第一次模拟考试广东省汕头市2022届普通高中毕业班第二次模拟试化学试题黑龙江省双鸭山市第一中学2022-2023学年高三上学期开学考试化学试题湖南省株洲市九方中学2022-2023学年高三上学期第五次月考化学试题
10 . 下列实验操作对应的现象和根据现象得出的结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 溶液中加入浓KOH溶液 溶液中加入浓KOH溶液 | 溶液由黄色变为红褐色 | 生成了氢氧化铁胶体 |
| B | 向某溶液中滴加NaSCN溶液 | 产生红色沉淀 | 溶液中存在三价铁离子 |
| C | 向某溶液中滴加 溶液 溶液 | 产生蓝色沉淀 | 溶液中存在亚铁离子 |
| D | 向 溶液中滴加 溶液中滴加 溶液 溶液 | 有白色沉淀和气体产生 |  与 与 发生了相互促进水解反应 发生了相互促进水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-16更新
|
673次组卷
|
7卷引用:化学-2022年高考考前押题密卷(福建卷)
(已下线)化学-2022年高考考前押题密卷(福建卷)云南省名校联盟2022届高三第二次模拟考试理科综合化学试题(已下线)秘籍19 综合实验装置分析与实验操作及实验现象描述-备战2022年高考化学抢分秘籍(全国通用)(已下线)专题12化学实验方案的设计与评价-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题12化学实验方案的设计与评价-五年(2018~2022)高考真题汇编(全国卷)湖南省邵阳市第一中学2023届高三第五次月考化学试题湖南省湘潭市第一中学2023届高三上学期第五次月考化学试题



