名校
1 . 化学来源于生活,且应用于生活。请根据题意填空:
(1)钠盐有多种,其中常用作食用碱的是______ (填“ ”或“NaOH”)
”或“NaOH”)
(2)电子工业中用覆铜板制作印刷电路板的原理为 。该反应中
。该反应中 作
作______ (填“氧化剂”或“还原剂”)。
(3)铝制品表面有一层氧化铝( )薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
)薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
______ 。
(1)钠盐有多种,其中常用作食用碱的是
 ”或“NaOH”)
”或“NaOH”)(2)电子工业中用覆铜板制作印刷电路板的原理为
 。该反应中
。该反应中 作
作(3)铝制品表面有一层氧化铝(
 )薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
)薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
您最近一年使用:0次
解题方法
2 . 钠、铁及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
① 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是___________ 。
② 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是___________ (填“还原产物”或“氧化产物”)。
(2)铁及其重要化合物之间的部分转化关系如图所示。___________ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的___________ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为___________ 。
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为___________ ,此过程中发生的氧化还原反应为(用化学方程式表达)___________ 。
(1)某汽车安全气囊的产气药剂主要含有
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,
等物质。当汽车发生碰撞时, 迅速分解产生
迅速分解产生 和Na,同时放出大量的热,
和Na,同时放出大量的热, 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。①
 是助氧化剂,可处理产生的Na,其中氯元素的化合价是
是助氧化剂,可处理产生的Na,其中氯元素的化合价是②
 是主氧化剂,也可处理产生的Na,反应为
是主氧化剂,也可处理产生的Na,反应为 ,反应中
,反应中 是
是(2)铁及其重要化合物之间的部分转化关系如图所示。
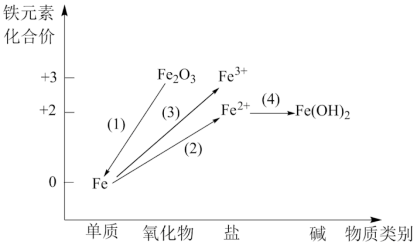
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
②实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
③在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为血红色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为
④在FeSO4中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
您最近一年使用:0次
解题方法
3 . I.现有A、B、C、D四种可溶性物质,它们溶于水后电离产生的所有离子如下表所示:(各物质中所含离子均不相同)
已知:①A物质是中学里用来检验Cl-的盐;
②向B物质的溶液中滴入无色酚酞溶液,呈红色;
③C物质分别与其它三种物质在溶液中反应均能产生白色沉淀,且B和C反应产生的白色沉淀会迅速变为灰绿色,最后变为红褐色。
回答下列问题:
(1)写出下列物质的化学式:A___________ ,D___________ 。
(2)写出③中沉淀颜色变化过程中涉及的化学反应方程式___________ 。
(3)检验溶液中Fe2+是否变质的操作是___________ 。
(4)D物质和C物质在溶液中反应的离子方程式为___________ 。
II.研究钠及其化合物的性质有重要的意义。
(5)某同学向 和
和 的混合液中逐滴加入一定浓度的盐酸,生成
的混合液中逐滴加入一定浓度的盐酸,生成 的体积(标准状况)与加入盐酸的体积的关系如图所示:
的体积(标准状况)与加入盐酸的体积的关系如图所示: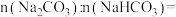
___________ 。
②盐酸的物质的量浓度为___________ 。
| 阳离子 |
|
| 阴离子 |
|
②向B物质的溶液中滴入无色酚酞溶液,呈红色;
③C物质分别与其它三种物质在溶液中反应均能产生白色沉淀,且B和C反应产生的白色沉淀会迅速变为灰绿色,最后变为红褐色。
回答下列问题:
(1)写出下列物质的化学式:A
(2)写出③中沉淀颜色变化过程中涉及的化学反应方程式
(3)检验溶液中Fe2+是否变质的操作是
(4)D物质和C物质在溶液中反应的离子方程式为
II.研究钠及其化合物的性质有重要的意义。
(5)某同学向
 和
和 的混合液中逐滴加入一定浓度的盐酸,生成
的混合液中逐滴加入一定浓度的盐酸,生成 的体积(标准状况)与加入盐酸的体积的关系如图所示:
的体积(标准状况)与加入盐酸的体积的关系如图所示:
②盐酸的物质的量浓度为
您最近一年使用:0次
名校
解题方法
4 . 茶是中国人喜爱的一种饮品,茶叶中含有铁元素,可以用以下实验操作检验茶叶中的铁元素:A.取少量茶叶;B.检验滤液中的 Fe3+;C.过滤得到滤液;D.将茶叶灼烧为茶叶灰;E.用足量稀盐酸溶解茶叶灰,并加蒸馏水稀释;请回答下列问题。
(1)上述实验操作的正确顺序是___________ (填字母)。
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、___________ 。
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式___________ 。
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式___________ 。
(1)上述实验操作的正确顺序是
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式
您最近一年使用:0次
5 . 根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
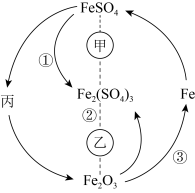
6 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题: 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
(1)根据分析可知丙为______ (填化学式);甲可能是______ (填标号,下同),乙可能是______ 。
A.稀硝酸 B. 溶液
溶液
C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量______ (填药品名称);可以用______ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为______ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是______ (填化学方程式)。
(4)绿矾 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为______ ;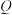 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为______ 。
 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。(1)根据分析可知丙为
A.稀硝酸 B.
 溶液
溶液C.
 D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
(4)绿矾
 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为
您最近一年使用:0次
2024-03-27更新
|
171次组卷
|
5卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
名校
7 . 请回答:
(1)Na的原子结构示意图是________________ ;MgCl2电子式是___________________ 。
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有________________ 性。
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是________________ 。
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是________________ ;此反应的离子方程式是________________ 。然后在溶液中再加入足量的铁粉,现象是________________ ,此时反应的离子方程式是________________ 。
(1)Na的原子结构示意图是
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是
您最近一年使用:0次
名校
8 . 按要求回答下列问题。
(1)写出重晶石主要成分的化学式_______ 。
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式_______ 。
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是_______ 。
(1)写出重晶石主要成分的化学式
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是
您最近一年使用:0次
名校
9 . 根据要求完成下列填空。
(1)画出氯原子结构示意图______ 。
(2)写出氨气和氢氧化钠的电子式:氨气_______ ,氢氧化钠______ 。
(3)写出氯化铁和铁反应的离子方程式_________ 。
(4)除去 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是____ ,化学方程式为________ 。
(1)画出氯原子结构示意图
(2)写出氨气和氢氧化钠的电子式:氨气
(3)写出氯化铁和铁反应的离子方程式
(4)除去
 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是
您最近一年使用:0次
名校
解题方法
10 . 除去下列物质中所混有的少量杂质,指明应加入的试剂和使用的分离方法,写出有关的反应方程式。
(1)铜粉中混有少量铝粉_______ 。
(2)FeCl3溶液中混有少量FeCl2_______ 。
(3)Na2CO3固体中混有少量NaHCO3_______ 。
(1)铜粉中混有少量铝粉
(2)FeCl3溶液中混有少量FeCl2
(3)Na2CO3固体中混有少量NaHCO3
您最近一年使用:0次

 Na+、Fe2+、Ag+、Ba2+
Na+、Fe2+、Ag+、Ba2+ 、
、


