名校
解题方法
1 . 茶是中国人喜爱的一种饮品,茶叶中含有铁元素,可以用以下实验操作检验茶叶中的铁元素:A.取少量茶叶;B.检验滤液中的 Fe3+;C.过滤得到滤液;D.将茶叶灼烧为茶叶灰;E.用足量稀盐酸溶解茶叶灰,并加蒸馏水稀释;请回答下列问题。
(1)上述实验操作的正确顺序是___________ (填字母)。
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、___________ 。
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式___________ 。
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式___________ 。
(1)上述实验操作的正确顺序是
(2)操作D所用仪器有:酒精灯、三脚架、泥三角、玻璃棒、
(3)请选择检验滤液中含有Fe3+的最佳方法并写出相关反应的离子方程式
(4)很多人喜欢用铁壶泡茶,请写出铁壶泡茶时可能发生反应的离子方程式
您最近一年使用:0次
2 . 根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
3 . 高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。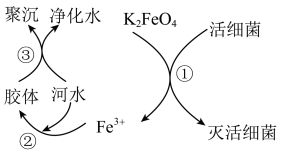
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
4 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
5 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:___________ 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式
您最近一年使用:0次
解题方法
6 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。

请回答以下问题:
(1)K2FeO4中Fe的化合价为_____ 。
(2) 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 ,发生相应反应的离子方程式为
,发生相应反应的离子方程式为_____ ,当有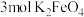 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为_____  。
。
(3)Fe2O3是否为碱性氧化物_____ (填是或否),理由:_____ 。
(4)制备氢氧化亚铁时,观察到白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释该现象:_____ ,其中检验溶液中Fe3+的试剂是KSCN溶液,该反应的离子方程式为:_____ 。

请回答以下问题:
(1)K2FeO4中Fe的化合价为
(2)
 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 ,发生相应反应的离子方程式为
,发生相应反应的离子方程式为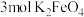 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为 。
。(3)Fe2O3是否为碱性氧化物
(4)制备氢氧化亚铁时,观察到白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释该现象:
您最近一年使用:0次
7 . 宏观辨识与微观探析是化学学科核心素养之一。根据所学知识,回答下列问题:
(1)铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等。
①氯化铁常用作印刷电路板的蚀刻剂,写出Cu与 反应的离子方程式:
反应的离子方程式:_______ ;反应后再通入氯气,又可将氯化亚铁转化为氯化铁,则通入氯气后反应的离子方程式为_______ 。
②氯化铁常用于净水,是因为铁离子转化为 胶体,胶体使水中悬浮物聚沉。
胶体,胶体使水中悬浮物聚沉。 胶体分散质粒子直径的范围是
胶体分散质粒子直径的范围是_______ ,检验氢氧化铁胶体是否制备成功常用的方法是_______ 。
(2)用电弧法合成的纳米碳管中常含有大量的杂质碳纳米颗粒,可用氧化气化法提纯,反应的化学方程式为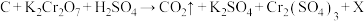 (X中的元素在反应前后未变价,反应未配平)。
(X中的元素在反应前后未变价,反应未配平)。
①该反应中,氧化剂是_______ (填化学式),被氧化的元素是_______ (填元素符号)。
②配平上述方程式:______ 。每生成4.4g  ,该反应转移的电子的物质的量为
,该反应转移的电子的物质的量为______ mol。
(1)铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等。
①氯化铁常用作印刷电路板的蚀刻剂,写出Cu与
 反应的离子方程式:
反应的离子方程式:②氯化铁常用于净水,是因为铁离子转化为
 胶体,胶体使水中悬浮物聚沉。
胶体,胶体使水中悬浮物聚沉。 胶体分散质粒子直径的范围是
胶体分散质粒子直径的范围是(2)用电弧法合成的纳米碳管中常含有大量的杂质碳纳米颗粒,可用氧化气化法提纯,反应的化学方程式为
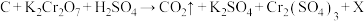 (X中的元素在反应前后未变价,反应未配平)。
(X中的元素在反应前后未变价,反应未配平)。①该反应中,氧化剂是
②配平上述方程式:
 ,该反应转移的电子的物质的量为
,该反应转移的电子的物质的量为
您最近一年使用:0次
解题方法
8 . 从物质类别和化合价两个角度总结、预测物质的性质是学习化学的重要方法之一。参考铁元素的“价类二维图”,回答下列问题。

Ⅰ相同类别不同价态的物质变化
(1)高铁酸钾是一种常见的水处理剂,可以同时起到杀菌消毒的作用和净水的作用,利用离子方程式表示其原理为______________ ;处理后的废水,调节pH至碱性,通入氯气,可实现水处理剂的循环利用,通入1molCl2理论上可以制备_____ gK2FeO4。
(2)铁氰化钾(K3[Fe(CN)6]),常用于配制铁锈指示剂检验金属的氧化程度,检验Fe2+的现象是___________________ ;工业上可用氯气氧化亚铁氰化钾(K4[Fe(CN)6])制备,离子方程式为______________ 。
Ⅱ不同类别不同价态的物质变化
(3)铁与水蒸气在高温环境下生成黑色固体的方程式:_______________ ;已知黑色固体可以被磁铁吸引,请设计实验,简述如何确定黑色固体的含量________ 。

Ⅰ相同类别不同价态的物质变化
(1)高铁酸钾是一种常见的水处理剂,可以同时起到杀菌消毒的作用和净水的作用,利用离子方程式表示其原理为
(2)铁氰化钾(K3[Fe(CN)6]),常用于配制铁锈指示剂检验金属的氧化程度,检验Fe2+的现象是
Ⅱ不同类别不同价态的物质变化
(3)铁与水蒸气在高温环境下生成黑色固体的方程式:
您最近一年使用:0次
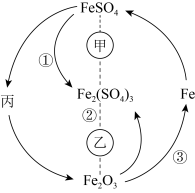
9 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题: 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
(1)根据分析可知丙为______ (填化学式);甲可能是______ (填标号,下同),乙可能是______ 。
A.稀硝酸 B. 溶液
溶液
C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量______ (填药品名称);可以用______ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为______ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是______ (填化学方程式)。
(4)绿矾 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为______ ; 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为______ 。
 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。(1)根据分析可知丙为
A.稀硝酸 B.
 溶液
溶液C.
 D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
(4)绿矾
 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为
您最近一年使用:0次
2024-03-27更新
|
126次组卷
|
4卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
名校
10 . 请回答:
(1)Na的原子结构示意图是________________ ;MgCl2电子式是___________________ 。
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有________________ 性。
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是________________ 。
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是________________ ;此反应的离子方程式是________________ 。然后在溶液中再加入足量的铁粉,现象是________________ ,此时反应的离子方程式是________________ 。
(1)Na的原子结构示意图是
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是
您最近一年使用:0次



