名校
1 . 某同学通过查阅得到以下资料:
材料一:BaSO4、BaSO3都难溶于水,BaSO4难溶于强酸,但BaSO3可溶于强酸,故BaSO4作为造影剂用于X射线检查,而BaSO3不能。
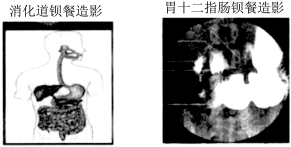
材料二:三氯化铁与二氧化硫能发生下列反应:2FeCl3+SO2+2H2O=FeCl2+FeSO4+4HCl。
在含有FeCl3和BaCl2的酸性溶液中通入一定量的SO2,有白色沉淀生成,由此得出的结论中正确的是
材料一:BaSO4、BaSO3都难溶于水,BaSO4难溶于强酸,但BaSO3可溶于强酸,故BaSO4作为造影剂用于X射线检查,而BaSO3不能。

材料二:三氯化铁与二氧化硫能发生下列反应:2FeCl3+SO2+2H2O=FeCl2+FeSO4+4HCl。
在含有FeCl3和BaCl2的酸性溶液中通入一定量的SO2,有白色沉淀生成,由此得出的结论中正确的是
| A.白色沉淀是BaSO3 |
| B.无法确定白色沉淀的成分 |
| C.白色沉淀是BaSO3和BaSO4的混合物 |
| D.FeCl3被SO2还原为FeCl2 |
您最近一年使用:0次
2021-03-05更新
|
182次组卷
|
2卷引用:河北省石家庄精英中学2021届高三二轮专题一阶段考试化学试卷
名校
2 . 化学与生产、生活密切相关。下列有关物质的性质与用途对应关系错误的是
| A.FeCl3溶液具有酸性,可用于蚀刻铜制品 |
| B.过氧乙酸具有强氧化性,可用于杀菌消毒 |
| C.甘油具有吸水性,可用作化妆品的保湿剂 |
| D.Na具有还原性,可用于高温下与TiCl4反应制备Ti |
您最近一年使用:0次
2021-03-03更新
|
452次组卷
|
5卷引用:河北省张家口市宣化第一中学2021届高三下学期阶段模拟(五)化学试题
河北省张家口市宣化第一中学2021届高三下学期阶段模拟(五)化学试题江苏省常州市2021届高三下学期期初调研考试化学试题吉林省松原市实验高级中学2020-2021学年高三下学期第三次摸底测试化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题1-5)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(选择题1-5)
解题方法
3 . 用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4,其流程示意图如图:
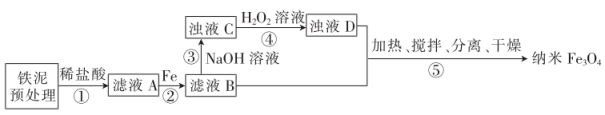
下列叙述正确的是

下列叙述正确的是
| A.步骤①发生的反应均为氧化还原反应 |
| B.步骤②中,发生反应的离子方程式为2Fe3++Fe=Fe2+ |
| C.浊液C和浊液D中分散质含量不相同 |
| D.步骤⑤中,“分离”包含的操作有过滤、洗涤 |
您最近一年使用:0次
名校
解题方法
4 . 乙醚是常用的有机试剂,久置容易产生过氧化物,带来安全隐患。以下不可用来定性检出过氧化物的试剂是
A. 溶液 溶液 |
| B.弱酸性淀粉KI溶液 |
C. 和稀 和稀 溶液 溶液 |
D. 的稀 的稀 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
2021-01-25更新
|
1300次组卷
|
6卷引用:河北省2021年普通高中学业水平选择考适应性测试化学试题
河北省2021年普通高中学业水平选择考适应性测试化学试题江西景德镇市浮梁一中2020-2021学年高二下学期4月月考争优部化学试题重庆市实验中学2021届高三下学期三诊化学试题陕西省西安市铁一中学2022届高三第二次月考化学试题(已下线)专题06 离子共存、检验和推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
5 . 化学与生活密切相关。下列叙述不涉及氧化还原反应的是
| A.牙膏中添加氟化物用于预防龋齿 |
| B.绿化造林助力实现碳中和目标 |
| C.氯化铁用于蚀刻金属眼镜架 |
| D.可降解包装材料的完全降解有利于减少白色污染 |
您最近一年使用:0次
2021-01-25更新
|
1394次组卷
|
9卷引用:河北省2021年普通高中学业水平选择考适应性测试化学试题
河北省2021年普通高中学业水平选择考适应性测试化学试题(已下线)押全国卷理综第7题 化学与社会生产生活-备战2021年高考化学临考题号押题(课标全国卷)(已下线)2021年高考化学押题预测卷(山东卷)03(含考试版、答题卡、参考答案、全解全析)辽宁省葫芦岛市第八高级中学2022届高三上学期10月月考化学试题(已下线)押全国卷理综第7题 化学与社会生产生活及传统文化-备战2022年高考化学临考题号押题(课标全国卷)(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省双鸭山市集贤县一中、四中等2021-2022学年高二下学期期末考试化学试题(已下线)专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第4讲 氧化还原反应的基本概念与规律
6 . 下列物质跟铁反应后的生成物,能跟KSCN溶液作用生成红色溶液的是
| A.盐酸 | B.稀硫酸 | C.CuSO4溶液 | D.氯气 |
您最近一年使用:0次
2021-01-24更新
|
241次组卷
|
17卷引用:河北省张家口宣化一中2020-2021学年高一下学期3月月考化学试题
河北省张家口宣化一中2020-2021学年高一下学期3月月考化学试题湖南省衡阳市第二十六中学2020-2021学年高一上学期期末考试化学试题(已下线)3.1.3 铁盐和亚铁盐-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)2019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题(已下线)2010—2011年福建省厦门市杏南中学高一12月月考化学卷(已下线)2012-2013学年甘肃省兰州五十五中高一上学期期末考试化学试卷(已下线)2012-2013学年山东省平邑县曾子学校高二期中考试文科化学试卷2014-2015学年天津市宝坻区四校高一11月联考化学试卷2016-2017学年山东省枣庄八中高一12月月考化学卷浙江省宁波诺丁汉大学附属中学2017-2018学年高一上学期期中考试化学试题云南省盐津县第三中学2018-2019学年高一第一学期12月份考试化学试题江苏省淮安市钦工中学2018-2019学年高二上学期期中考试化学试题上海市金山中学2016-2017学年高二上学期期中考试等级考试化学试题山东省青岛平度市2019-2020学年高一下学期线上阶段测试化学试题云南省梁河县第一中学2020-2021学年高一上学期第二次月考化学试题课前-3.1.1铁及其化合物(课前)-鲁科版2019必修第一册陕西省宝鸡市陈仓区2021-2022学年高一上学期期末考试化学试题
名校
解题方法
7 . 下列各组离子在指定溶液中能大量共存的是
①常温下pH=11的溶液中: 、
、 、
、 、
、
②加入铝粉能放出 的溶液中:
的溶液中: 、
、 、
、 、
、
③无色透明、酸性溶液中: 、
、 、
、 、
、
④含有大量 的溶液中:
的溶液中: 、
、 、
、 、
、
①常温下pH=11的溶液中:
 、
、 、
、 、
、
②加入铝粉能放出
 的溶液中:
的溶液中: 、
、 、
、 、
、
③无色透明、酸性溶液中:
 、
、 、
、 、
、
④含有大量
 的溶液中:
的溶液中: 、
、 、
、 、
、
| A.①② | B.①③④ | C.① | D.②③ |
您最近一年使用:0次
2021-01-12更新
|
188次组卷
|
5卷引用:河北省保定市唐县一中2021-2022学年高三上学期第二次月考化学试题
8 . 硫化镍矿的主要成分是 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
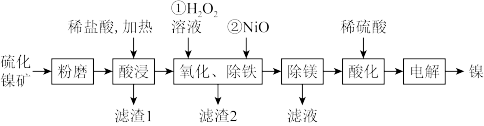
(1)硫化镍矿粉磨的目的是_______ ,“酸浸”时,硫化镍与稀盐酸反应的化学方程式为_______ 。
(2)“氧化、除铁”过程中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_______ ;加入氧化镍的目的是除去铁元素,用化学平衡移动原理解释除去铁元素的原因_______ 。
(3)已知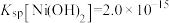 ,
,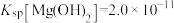 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中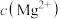 ≤
≤_______ 。
(4)电解硫酸镍溶液时,在_______ 极得到镍单质,电解产物_______ (填化学式)可以循环使用。
 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
(1)硫化镍矿粉磨的目的是
(2)“氧化、除铁”过程中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为(3)已知
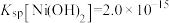 ,
,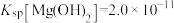 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中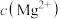 ≤
≤(4)电解硫酸镍溶液时,在
您最近一年使用:0次
9 . 下列实验操作、实验现象及原因表述均正确的是
| 选项 | 实验操作 | 实验现象 | 原因 |
| A | 室温下,向铝箔上滴加浓硝酸 | 产生大量红棕色气体 | 浓硝酸具有强氧化性 |
| B | 向溶液中滴加硫氰化钾溶液 | 无明显现象 | 溶液中不存在Fe3+ |
| C | 向等浓度的NaCl和NaBr的混合溶液中滴加AgNO3溶液 | 先出现淡黄色沉淀 | Ksp(AgCl)<Ksp(AgBr) |
| D | 向NaBr溶液中通入过量氯气,再加入淀粉-KI溶液 | 溶液先变黄色最终变蓝 | 氧化性:Cl2>Br2>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 为探究硫酸亚铁晶体(FeSO4∙xH2O)在加热条件下的分解产物、设计如图1实验。称取ag硫酸亚铁晶体,加热使其完全分解;对其分解产物进行分析验证,并测定其结晶水个数x的值。

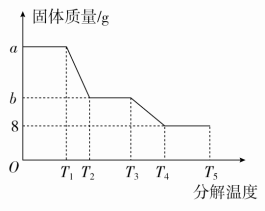
图1 图2
(1)实验过程中需缓慢持续通入氮气,其目的是排除装置中的空气和___________ ,
(2)装置B中可观察到的现象是___________ 。装置C中的现象是酸性高锰酸钾溶液褪色,检测表明溶液中含有Mn2+,则C中发生反应的离子方程式为___________ 。
(3)实验结束后发现装置A中有红棕色固体,经分析硫酸亚铁分解产物之一为SO3, 则FeSO4分解的化学方程式为___________ 。
(4)装置D球形干燥管的作用___________ 。
(5)利用热分析仪对硫酸亚铁晶体(FeSO4∙xH2O)进行热分解实验并绘制固体质量与分解温度的关系图(如图2)。
①温度介于T2~T3之间,固体物质的化学式为___________ 。
②计算FeSO4∙xH2O中x的值,x=___________ (用含a、b的代数式表示)。


图1 图2
(1)实验过程中需缓慢持续通入氮气,其目的是排除装置中的空气和
(2)装置B中可观察到的现象是
(3)实验结束后发现装置A中有红棕色固体,经分析硫酸亚铁分解产物之一为SO3, 则FeSO4分解的化学方程式为
(4)装置D球形干燥管的作用
(5)利用热分析仪对硫酸亚铁晶体(FeSO4∙xH2O)进行热分解实验并绘制固体质量与分解温度的关系图(如图2)。
①温度介于T2~T3之间,固体物质的化学式为
②计算FeSO4∙xH2O中x的值,x=
您最近一年使用:0次



