名校
1 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】1.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。2. KSCN中的硫元素为-2价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)将补铁剂碾碎的目的是_______ 。
(2)试剂1是_______ 。
(3)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ 。
(4)能证明溶液①中含有Fe2+的实验现象是_______ 。
(5)写出上述条件下Fe2+与H2O2发生反应的离子方程式_______ 。
(6)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的SCN-与H2O2发生了化学反应。
a. 甲同学猜测的依据是_______ 。
b. 乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
实验Ⅱ. 测定该补铁剂中铁元素的含量。
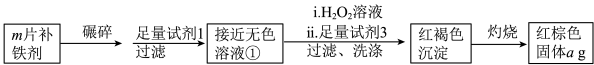
(7)计算每片该补铁剂含铁元素的质量为_______ g。
(8)人体只能吸收Fe2+,医生建议在服用该补铁剂时,同时服用有较强还原性的维生素C,理由是_______ 。
【查阅资料】1.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。2. KSCN中的硫元素为-2价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)将补铁剂碾碎的目的是
(2)试剂1是
(3)加入试剂2后溶液变为浅红色,说明溶液①中含有
(4)能证明溶液①中含有Fe2+的实验现象是
(5)写出上述条件下Fe2+与H2O2发生反应的离子方程式
(6)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的SCN-与H2O2发生了化学反应。
a. 甲同学猜测的依据是
b. 乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
实验Ⅱ. 测定该补铁剂中铁元素的含量。

(7)计算每片该补铁剂含铁元素的质量为
(8)人体只能吸收Fe2+,医生建议在服用该补铁剂时,同时服用有较强还原性的维生素C,理由是
您最近一年使用:0次
名校
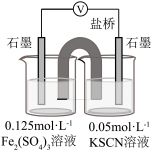
2 . 某小组研究溶液中 与
与 、
、 的反应。
的反应。
资料: 在溶液中呈棕色。
在溶液中呈棕色。
(1)研究现象a中的黄色溶液。
①用___________ 溶液检出溶液中含有 。
。
②甲认为是O2氧化了溶液中的 。乙认为O2不是主要原因,理由是
。乙认为O2不是主要原因,理由是___________ 。
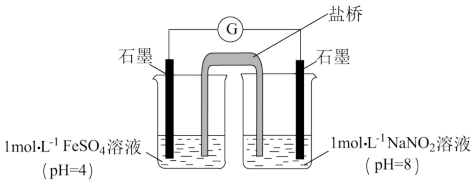
③进行实验Ⅱ,装置如下图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式是___________ 。实验Ⅱ的目的是___________ 。
(2)研究现象a中的棕色溶液。
①综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的 或
或 发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为
发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为 与NO发生了反应。实验Ⅲ的操作和现象是
与NO发生了反应。实验Ⅲ的操作和现象是___________ 。
②加热实验I中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释产生红褐色沉淀的原因是___________ 。
(3)研究酸性条件下,溶液中 与
与 、
、 的反应。
的反应。
①i中溶液变为棕色的离子方程式是___________ 、___________ 。
②iii中出现棕色的原因是___________ 。
实验结论:本实验条件下,溶液中 、
、 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。
 与
与 、
、 的反应。
的反应。| 实验Ⅰ | 试剂 | 现象 | |
| 滴管 | 试管 | ||
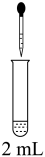 |  溶液(pH=4) 溶液(pH=4) |  溶液(pH=8) 溶液(pH=8) | a.滴入1滴FeSO4溶液,溶液变黄色,继续滴加,溶液变为棕色。2小时后,无明显变化 |
 溶液(加NaOH溶液至pH=8) 溶液(加NaOH溶液至pH=8) | b.持续滴加FeSO4溶液,无明显变化。 | ||
 在溶液中呈棕色。
在溶液中呈棕色。(1)研究现象a中的黄色溶液。
①用
 。
。②甲认为是O2氧化了溶液中的
 。乙认为O2不是主要原因,理由是
。乙认为O2不是主要原因,理由是③进行实验Ⅱ,装置如下图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式是

(2)研究现象a中的棕色溶液。
①综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的
 或
或 发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为
发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为 与NO发生了反应。实验Ⅲ的操作和现象是
与NO发生了反应。实验Ⅲ的操作和现象是②加热实验I中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释产生红褐色沉淀的原因是
(3)研究酸性条件下,溶液中
 与
与 、
、 的反应。
的反应。| 序号 | 操作 | 现象 |
| i | 取 的NaNO2溶液,加醋酸至pH=3,加入 的NaNO2溶液,加醋酸至pH=3,加入 溶液 溶液 | 溶液立即变为棕色 |
| ii | 取 的NaNO3溶液,加醋酸至pH=3,加入 的NaNO3溶液,加醋酸至pH=3,加入 溶液 溶液 | 无明显变化 |
| iii | 分别取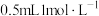 的NaNO3溶液与 的NaNO3溶液与 的FeSO4溶液,混合,小心加入0.5mL浓硫酸 的FeSO4溶液,混合,小心加入0.5mL浓硫酸 | 液体分为两层,稍后,在两层液体界面上出现棕色环 |
②iii中出现棕色的原因是
实验结论:本实验条件下,溶液中
 、
、 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。
您最近一年使用:0次
名校
解题方法
3 . 某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度。
I.实验一:探究温度和浓度对反应速率的影响。
实验原理及方案:在酸性溶液中,碘酸钾( )和亚硫酸钠可发生反应生成碘,反应原理是
)和亚硫酸钠可发生反应生成碘,反应原理是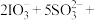
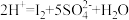 ,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
(1)则
_______ mL,
_______ mL。
Ⅱ.实验二:探究KI和 混合时生成KCl、I2和
混合时生成KCl、I2和 的反应存在一定的限度。
的反应存在一定的限度。
实验原理: 。
。
实验步骤:向5mL 0.1 KI溶液中滴加5~6滴0.1
KI溶液中滴加5~6滴0.1
 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
(2)向甲中滴加 ,充分振荡、静置,下层溶液出现紫红色,说明有
,充分振荡、静置,下层溶液出现紫红色,说明有 生成;向乙中滴加试剂
生成;向乙中滴加试剂_______ ,若现象为_______ ,则说明该反应有一定的限度。
Ⅲ.800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图,分析图像回答问题:

(3)该反应的化学方程式为_______ 。
(4)2min内,用C来表示的化学反应速率为_______ 。
(5)在其他条件下,测得A的反应速率为0.05 ,此时的反应与800℃时相比,
,此时的反应与800℃时相比,_______ (填字母)。
A.比800℃时快B.比800℃时慢C.和800℃时速率一样
I.实验一:探究温度和浓度对反应速率的影响。
实验原理及方案:在酸性溶液中,碘酸钾(
 )和亚硫酸钠可发生反应生成碘,反应原理是
)和亚硫酸钠可发生反应生成碘,反应原理是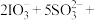
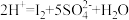 ,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝| 实验序号 | 0.01  酸性溶液(含淀粉)的体积/mL 酸性溶液(含淀粉)的体积/mL | 0.01  溶液的体积/mL 溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 |  | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 |  | 35 | 25 |


Ⅱ.实验二:探究KI和
 混合时生成KCl、I2和
混合时生成KCl、I2和 的反应存在一定的限度。
的反应存在一定的限度。实验原理:
 。
。实验步骤:向5mL 0.1
 KI溶液中滴加5~6滴0.1
KI溶液中滴加5~6滴0.1
 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。(2)向甲中滴加
 ,充分振荡、静置,下层溶液出现紫红色,说明有
,充分振荡、静置,下层溶液出现紫红色,说明有 生成;向乙中滴加试剂
生成;向乙中滴加试剂Ⅲ.800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图,分析图像回答问题:

(3)该反应的化学方程式为
(4)2min内,用C来表示的化学反应速率为
(5)在其他条件下,测得A的反应速率为0.05
 ,此时的反应与800℃时相比,
,此时的反应与800℃时相比,A.比800℃时快B.比800℃时慢C.和800℃时速率一样
您最近一年使用:0次
名校
解题方法
4 . 某小组研究SCN-分别与Cu2+和Fe3+的反应:
下列说法不正确的是
| 编号 | 1 | 2 | 3 |
| 实验 |
|
|
|
| 现象 | 溶液变为黄绿色,产生白色沉淀(白色沉淀为CuSCN) | 溶液变红,向反应后的溶液中加入K3[Fe(CN)6]溶液,产生蓝色沉淀,且沉淀量逐渐增多 | 接通电路后,电压表指针不偏转。一段时间后,取出左侧烧杯中少量溶液,滴加K3[Fe(CN)6]溶液,没有观察到蓝色沉淀 |
| A.实验1中发生了氧化还原反应,KSCN为还原剂 |
| B.实验2中“溶液变红”是Fe3+与SCN-结合形成了配合物 |
| C.若将实验3中Fe2(SO4)3溶液替换为0.25 mol/LCuSO4溶液,接通电路后,可推测出电压表指针会发生偏转 |
| D.综合实验1~3,微粒的氧化性与还原产物的价态和状态有关 |
您最近一年使用:0次
2023-03-24更新
|
836次组卷
|
6卷引用:北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题
名校
5 . 某校化学兴趣小组探究 与
与 溶液的反应。实验I:向
溶液的反应。实验I:向 溶液中通入
溶液中通入 至饱和,发现溶液变成红色,静置
至饱和,发现溶液变成红色,静置 后,溶液的颜色从红色慢慢变回黄色。静置
后,溶液的颜色从红色慢慢变回黄色。静置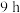 后,溶液慢慢由黄色变为浅绿色。查阅资料:
后,溶液慢慢由黄色变为浅绿色。查阅资料: 能与
能与 微粒形成红色配合物。该小组同学猜想可能是
微粒形成红色配合物。该小组同学猜想可能是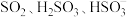 与
与 形成配合物而使溶液呈现红色。进行如下实验:
形成配合物而使溶液呈现红色。进行如下实验:
下列说法不正确 的是
 与
与 溶液的反应。实验I:向
溶液的反应。实验I:向 溶液中通入
溶液中通入 至饱和,发现溶液变成红色,静置
至饱和,发现溶液变成红色,静置 后,溶液的颜色从红色慢慢变回黄色。静置
后,溶液的颜色从红色慢慢变回黄色。静置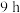 后,溶液慢慢由黄色变为浅绿色。查阅资料:
后,溶液慢慢由黄色变为浅绿色。查阅资料: 能与
能与 微粒形成红色配合物。该小组同学猜想可能是
微粒形成红色配合物。该小组同学猜想可能是 与
与 形成配合物而使溶液呈现红色。进行如下实验:
形成配合物而使溶液呈现红色。进行如下实验:| 序号 | 实验 | 加入试剂 | 现象 |
| II |  |  的 的 溶液;再滴加几滴盐酸 溶液;再滴加几滴盐酸 | 溶液变成红色,比I红色深;滴加盐酸后,溶液颜色由红色变成黄色 |
| III |  的 的 溶液 溶液 | 溶液变成红色,比II中溶液红色深 |
A. |
B.根据实验II和实验III现象对比,红色物质可能与 有关 有关 |
C. 与 与 溶液反应,可以发生配位反应、氧化还原反应 溶液反应,可以发生配位反应、氧化还原反应 |
D. 与 与 溶液的配位反应速率快,但限度小:氧化还原反应速率较慢,但限度较大 溶液的配位反应速率快,但限度小:氧化还原反应速率较慢,但限度较大 |
您最近一年使用:0次
名校
解题方法
6 . 下列实验现象或操作不能达到相应实验目的的是
| 选项 | 实验目的 | 实验现象或操作 |
| A | 验证浓硫酸的脱水性 | 将浓硫酸滴加到蔗糖上,蔗糖变黑,体积膨胀,放出有刺激性气味的气体 |
| B | 验证Fe3+具有氧化性 | 向FeCl3溶液中加入过量铁粉,溶液由黄色变为浅绿色 |
| C | 验证浓硝酸可被炭还原为NO2 | 将炽热的木炭加入浓硝酸中,有红棕色气体产生 |
| D | 验证NH3具有还原性 | 将NH3通过灼热的CuO,黑色固体变为红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-10更新
|
1015次组卷
|
6卷引用:北京师范大学附属实验中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
7 . 某溶液中含大量Fe2+、Mg2+、Fe3+、Na+、Cl-、SO 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是| A.Na+、Fe2+ | B.Mg2+、SO | C.Fe3+、SO | D.Mg2+、Cl- |
您最近一年使用:0次
2023-01-17更新
|
471次组卷
|
2卷引用:北京师范大学附属中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 探究0.5mol/LFeCl3溶液(pH=1)与不同金属反应时的多样性的原因。
(各组实验中:所用FeCl3溶液体积相同;金属过量;静置、不振荡)
(1)根据实验Ⅰ中的现象,推测红褐色液体为胶体,并用光束照射该液体,在与光束垂直的方向观察到_______ 得以证实。
(2)已知:Fe和Fe3O4均能被磁铁吸引。
①为了确定黑色固体的成分是否含有Fe与Fe3O4,重复实验Ⅰ,及时取少量镁条表面生成的黑色粉末,洗净后进行实验如下:
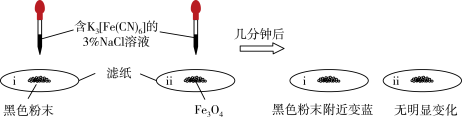
该实验说明黑色固体中一定含有_______ ,结合现象写出判断的理由:_______ 。
②除上述结论外,分析实验Ⅰ的现象,可知被还原得到的产物一定还有_______ 。
(3)实验Ⅰ、Ⅱ中现象的差异,与Fe3+、Mg2+、Fe2+、H+、Cu2+的氧化性强弱有关,其顺序是Mg2+<Fe2+<_______ 。
(各组实验中:所用FeCl3溶液体积相同;金属过量;静置、不振荡)
| 编号 | 金属 | 现象及产物检验 |
| Ⅰ | 镁条 | 立即产生大量气体,金属表面变黑,该黑色固体能被磁铁吸引,液体颜色由棕黄色逐渐变为红褐色; 片刻后气泡减少,金属表面覆盖有红褐色沉淀,此时取反应后的液体,滴加K3[Fe(CN)6]溶液,生成蓝色沉淀。 |
| Ⅱ | 铜粉 | 无气体产生,溶液逐渐变为蓝绿色; 取反应后的溶液,滴加K3[Fe(CN)6]溶液,生成蓝色沉淀。 |
(2)已知:Fe和Fe3O4均能被磁铁吸引。
①为了确定黑色固体的成分是否含有Fe与Fe3O4,重复实验Ⅰ,及时取少量镁条表面生成的黑色粉末,洗净后进行实验如下:

该实验说明黑色固体中一定含有
②除上述结论外,分析实验Ⅰ的现象,可知被还原得到的产物一定还有
(3)实验Ⅰ、Ⅱ中现象的差异,与Fe3+、Mg2+、Fe2+、H+、Cu2+的氧化性强弱有关,其顺序是Mg2+<Fe2+<
您最近一年使用:0次
名校
解题方法
9 . 某废旧金属材料中主要含Fe、Cu、Al、 、FeO、
、FeO、 、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Cu、Al、绿矾等。回答下列问题:
、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Cu、Al、绿矾等。回答下列问题:_______ 。
(2)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是_______ 。
(3)加入试剂a后发生的化学反应中有一个属于化合反应,其离子方程式为_______ 。
(4)滤液Ⅱ经过结晶法制取绿矾晶体,绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体8.22g溶于稀盐酸后,加入足量的 溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的
溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的 完全氧化。
完全氧化。
①为确定绿矾未被全部氧化,可选择的最佳试剂是_______ (填标号)。
A. 溶液 B.KSCN溶液
溶液 B.KSCN溶液
C.NaOH溶液 D. 溶液
溶液
②推测晶体中
_______ 。
 、FeO、
、FeO、 、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Cu、Al、绿矾等。回答下列问题:
、CuO和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Cu、Al、绿矾等。回答下列问题: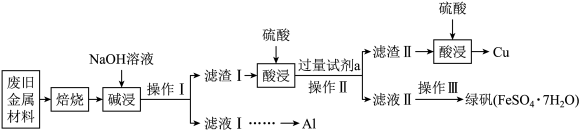
(2)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
(3)加入试剂a后发生的化学反应中有一个属于化合反应,其离子方程式为
(4)滤液Ⅱ经过结晶法制取绿矾晶体,绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体8.22g溶于稀盐酸后,加入足量的
 溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的
溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的 完全氧化。
完全氧化。①为确定绿矾未被全部氧化,可选择的最佳试剂是
A.
 溶液 B.KSCN溶液
溶液 B.KSCN溶液C.NaOH溶液 D.
 溶液
溶液②推测晶体中

您最近一年使用:0次
2023-01-07更新
|
617次组卷
|
3卷引用:北京市第八中学2022-2023学年高一上学期期末考试化学试题
名校
10 . 在某酸性溶液中,能大量共存的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
2023-01-07更新
|
574次组卷
|
3卷引用:北京市第八中学2022-2023学年高一上学期期末考试化学试题