解题方法
1 . 根据实验目的,下列实验及现象操作、结论都正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 制备Fe(OH)3胶体 | 向沸水中逐滴加入5~6滴饱和FeCl3溶液,持续加热,生成红褐色固体 | FeCl3与水反应产生Fe(OH)3胶体 |
| B | 验证Cl2的漂白性 | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃瓶,一段时间后有色鲜花褪色 | Cl2有漂白性 |
| C | 检验溶液中的Na+ | 用硫酸洗净后的铂丝蘸取少量溶液在酒精灯外焰上灼烧,产生黄色火焰 | 溶液中存在Na+ |
| D | 验证Fe3+的氧化性 | 在盛有2mLFeCl3的溶液中加入过量Fe粉,充分振荡后滴入几滴KSCN溶液,溶液未变红色 | Fe3+可以被Fe还原 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 向 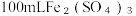 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
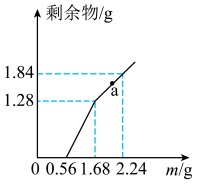
(1)加入少量铁粉时,发生的离子反应______________ 。
(2)原溶液中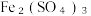 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为_______ 。
(3)a点时溶液中溶质的物质的量浓度为____________ 。
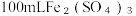 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
(1)加入少量铁粉时,发生的离子反应
(2)原溶液中
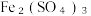 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为(3)a点时溶液中溶质的物质的量浓度为
您最近一年使用:0次
3 . 称取6.00g氧化铜和氧化铁固体混合物,加入75.0mL2.00mol/L的硫酸充分溶解,往所得溶液中加入8.40g铁粉,充分反应后,得固体的质量为4.56g。请计算:
(1)加入的铁粉的物质的量为___________ mol。
(2)加入铁粉充分反应后,溶液中溶质为___________ ,其物质的量浓度为___________ mol/L(不考虑体积变化)。
(3)固体混合物中氧化铜的质量百分比为___________ 。
(1)加入的铁粉的物质的量为
(2)加入铁粉充分反应后,溶液中溶质为
(3)固体混合物中氧化铜的质量百分比为
您最近一年使用:0次
22-23高一下·浙江·期中
解题方法
4 . 下列化合物中不能通过化合反应制取的是
| A.FeSO4 | B.H2SiO3 | C.H2SO4 | D.HNO3 |
您最近一年使用:0次
22-23高一下·浙江·期中
5 . 将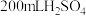 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少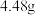 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到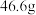 白色沉淀。请计算:
白色沉淀。请计算:
(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①___________ 、②___________ 。
(2)原溶液中
___________  ;
;
(3)原溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
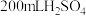 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少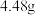 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到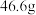 白色沉淀。请计算:
白色沉淀。请计算:(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①
(2)原溶液中

 ;
;(3)原溶液中
 和
和 的物质的量浓度之比为
的物质的量浓度之比为
您最近一年使用:0次
解题方法
6 . 将1.00mol/L硫酸铜溶液和2.00mol/L硫酸铁溶液按体积比2:3混合得到1L混合液(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量的铁粉,充分反应后,铁粉有剩余。请计算:
(1)混合后溶液中铜离子的物质的量为______ mol。
(2)溶解的铁粉的质量为______ g。
(3)最后所得溶液中硫酸亚铁的物质的量浓度为______ mol/L。
(1)混合后溶液中铜离子的物质的量为
(2)溶解的铁粉的质量为
(3)最后所得溶液中硫酸亚铁的物质的量浓度为
您最近一年使用:0次
7 . 下列关于元素及其化合物的性质说法不正确的是
A. 与 与 反应可生成C 反应可生成C |
B. 与 与 反应可生成 反应可生成 |
C.可通过化合反应生成 |
D.工业上用 和澄清石灰水反应来制备漂白粉 和澄清石灰水反应来制备漂白粉 |
您最近一年使用:0次
8 . 某工厂的工业废水中含有大量的 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属
。为减少污染并变废为宝,工厂计划从该废水中回收金属 和硫酸亚铁晶体,流程如下:
和硫酸亚铁晶体,流程如下:

下列说法不正确 的是
 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属
。为减少污染并变废为宝,工厂计划从该废水中回收金属 和硫酸亚铁晶体,流程如下:
和硫酸亚铁晶体,流程如下:
下列说法
A.检验硫酸亚铁晶体中的金属阳离子时,滴加的试剂依次是 溶液、氯水 溶液、氯水 |
| B.试剂A为铁粉,试剂B可能是稀硫酸 |
| C.操作Ⅱ是蒸发浓缩、冷却结晶、过滤洗涤、干燥 |
D.溶液Z中的离子只有 |
您最近一年使用:0次
9 . 下列物质转化不能通过一步反应完成的是
A. →HClO →HClO | B.S→ | C. | D.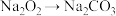 |
您最近一年使用:0次
10 . 下列化学反应的离子方程式书写正确的是
A.铁与氯化铁溶液反应: |
B.向澄清石灰水中通入少量 : : |
C.用醋酸清除水垢: |
D.用铝粉和NaOH溶液反应制取少量 : : |
您最近一年使用:0次



