1 . 下列化学反应,所得产物只含一种价态铁元素的是
| A.在空气中加热FeO | B.在空气中加热Fe(OH)2 |
| C.在空气中加热Fe(OH)3 | D.在氧气中点燃Fe |
您最近一年使用:0次
名校
2 . “类比”是研究物质变化规律的重要方法。下列有关“类比”对物质性质的推测正确的是
| A.CO2与CaCl2溶液不反应,推测CO2与Ca(NO3)2溶液也不反应 |
| B.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
C.Na在空气中加热生成 ,Li在空气中加热也生成 ,Li在空气中加热也生成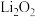 |
D. 溶解度大于 溶解度大于 , , 的溶解度也大于 的溶解度也大于 |
您最近一年使用:0次
2024-01-11更新
|
223次组卷
|
2卷引用:重庆市第一中学校2023-2024学年高一下学期3月定时练习化学试题
名校
3 . 某兴趣小组研究合铁元素的盐类物质的性质、制备。
实验I.通过 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
(1)实验ⅰ中滴加NaOH溶液后出现的一系列现象是___________ ;
(2)探究实验ⅱ中滴加 溶液时实验现象为
溶液时实验现象为___________ ;其反应的离子方程式为___________ ;加碱后溶液无明显变化的原因___________ 。
实验II.高铁酸钠( ,
, )是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
)是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:

(3) 中铁元素的化合价为
中铁元素的化合价为___________
(4)“氧化”过程的反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ ;当有 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为___________  。
。
(5)产品经干燥后得到纯品 ,则
,则 的产率为
的产率为___________ (保留两位有效数字)。[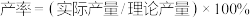 。一般以百分数表示]
。一般以百分数表示]
实验I.通过
 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
 | 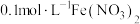 溶液 溶液 | 实验ⅰ: 先滴加 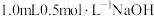 溶液; 溶液;再滴加 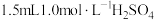 溶液 溶液 | i.滴加NaOH溶液后___________;加酸后溶液变为黄色 |
| 实验ⅱ: 先滴加 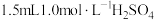 溶液; 溶液;再滴加 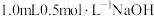 溶液 溶液 | ii.滴加 溶液时___________;加碱后溶液无明显变化 溶液时___________;加碱后溶液无明显变化 | ||
(2)探究实验ⅱ中滴加
 溶液时实验现象为
溶液时实验现象为实验II.高铁酸钠(
 ,
, )是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
)是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
(3)
 中铁元素的化合价为
中铁元素的化合价为(4)“氧化”过程的反应体系中共存在下列6种粒子:
 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式
,写出该反应的离子方程式 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为 。
。(5)产品经干燥后得到纯品
 ,则
,则 的产率为
的产率为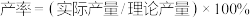 。一般以百分数表示]
。一般以百分数表示]
您最近一年使用:0次
名校
4 . 类比推理是化学中常用的思维方法,下列推理正确的是
| A.CO2与CaCl2溶液不反应,推测CO2与Ca(NO3)2溶液也不反应 |
| B.CaCO3的溶解度小于Ca(HCO3)2,推测Na2CO3的溶解度小于NaHCO3 |
| C.电解熔融氯化镁可制备金属镁,推测电解熔融氯化铝可制备金属铝 |
| D.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
您最近一年使用:0次
5 . 关于 的实验室制备,下列说法不正确的是
的实验室制备,下列说法不正确的是

 的实验室制备,下列说法不正确的是
的实验室制备,下列说法不正确的是
A.常用煮沸的方法除去NaOH溶液中的 |
| B.将苯换成酒精同样可以达到隔绝空气的作用 |
C.该反应的离子方程式为: |
| D.氢氧化亚铁是难溶于水的白色沉淀 |
您最近一年使用:0次
6 . 铁、铝的混合物进行如下实验:

(1)操作X的名称是____________ ;
(2)气体A是____________ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成_____________ (填化学式),A在该反应中作为_____________ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH-外还有____________________ (填离子符号),溶液D中存在的金属离子为__________________ (填离子符号);
(5)加入稀盐酸发生反应的离子方程式为:________________________ ;
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:__________________________ 。

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH-外还有
(5)加入稀盐酸发生反应的离子方程式为:
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
i、从废液中提纯并结晶出FeSO4·7H2O,并将其配成溶液。
ii、FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
iii、将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
iv、煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中会发生分解。
(1)步骤i从废液中提纯并结晶出FeSO4·7H2O的主要操作为___________ 、过滤、洗涤、干燥。
(2)步骤ii中,生成FeCO3的化学方程式是___________ 。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色[Fe(OH)3],写出发生反应的化学方程式是___________ 。
(3)步骤iii中,过滤需要使用到的玻璃仪器有___________ ;通过检验SO 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入___________ ,若___________ ,证明沉淀已经洗涤干净。
(4)已知煅烧FeCO3的化学方程式是4FeCO3+O2 2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是___________ kg。
i、从废液中提纯并结晶出FeSO4·7H2O,并将其配成溶液。
ii、FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
iii、将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
iv、煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中会发生分解。
(1)步骤i从废液中提纯并结晶出FeSO4·7H2O的主要操作为
(2)步骤ii中,生成FeCO3的化学方程式是
(3)步骤iii中,过滤需要使用到的玻璃仪器有
 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入(4)已知煅烧FeCO3的化学方程式是4FeCO3+O2
 2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
您最近一年使用:0次
名校
8 . 下列实验能达到实验目的且符合操作要求的是
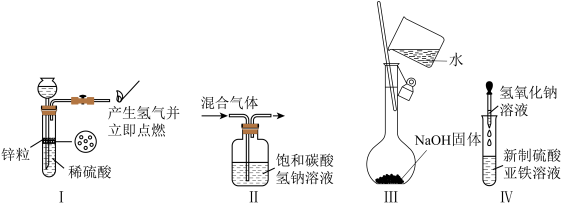

| A.Ⅰ可用于制备并检验氢气的可燃性 |
| B.Ⅱ可用于除去CO2中的HCl |
| C.用Ⅲ来配制一定物质的量浓度的NaOH溶液 |
| D.用Ⅳ中操作制备氢氧化亚铁并观察其颜色 |
您最近一年使用:0次
2022-09-06更新
|
932次组卷
|
4卷引用:重庆市沙坪坝实验中学校2021-2022学年高一上学期期末考试化学试题
重庆市沙坪坝实验中学校2021-2022学年高一上学期期末考试化学试题(已下线)3.1.1铁及其化合物-同步学习必备知识上海市南洋模范中学2022-2023学年高一上学期阶段练习一化学试题(已下线)选择题11-15
名校
解题方法
9 . 某学习小组为认识铁及其化合物的性质做了如下一组综合实验,根据实验流程回答相关问题:
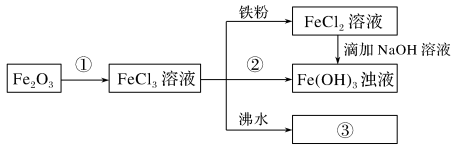
(1)物质②为_______ 。
(2)请写出FeCl3与铁粉反应的离子方程式_______ 。
(3)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_______ ,此过程中发生的氧化还原反应为(用化学方程式表达)_______ 。
(4)检验溶液中Fe3+存在的试剂是_______ ,证明Fe3+存在的现象是_______ 。

(1)物质②为
(2)请写出FeCl3与铁粉反应的离子方程式
(3)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
(4)检验溶液中Fe3+存在的试剂是
您最近一年使用:0次
名校
解题方法
10 . 在稀硫酸溶液中加入适量铁粉,反应完全后再加入适量氢氧化钠溶液,放置片刻,从反应体系中观察到颜色的变化是
| A.无色→灰绿色→红褐色 |
| B.灰绿色→红褐色→蓝灰色→红棕色 |
| C.无色→浅绿色→白色→灰绿色→红褐色 |
| D.无色→白色→浅绿色→灰绿色→红褐色 |
您最近一年使用:0次
2022-04-06更新
|
251次组卷
|
6卷引用:重庆市求精中学2021-2022学年高一上学期第二次月考化学试题
重庆市求精中学2021-2022学年高一上学期第二次月考化学试题河南省叶县高级中学2022-2023学年高一上学期1月期末考试化学试题(已下线)【精品卷】3.1.2 铁的重要化合物课堂例题-人教版2023-2024学年必修第一册(已下线)2012年人教版高中化学选修6 3.2 物质含量的测定练习卷(已下线)2012年鲁科版高中化学选修6 3.2 物质中某组分含量的测定练习卷(已下线)8.1 铁及其化合物-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)



