1 . 下列化学反应,所得产物只含一种价态铁元素的是
| A.在空气中加热FeO | B.在空气中加热Fe(OH)2 |
| C.在空气中加热Fe(OH)3 | D.在氧气中点燃Fe |
您最近半年使用:0次
名校
2 . “类比”是研究物质变化规律的重要方法。下列有关“类比”对物质性质的推测正确的是
| A.CO2与CaCl2溶液不反应,推测CO2与Ca(NO3)2溶液也不反应 |
| B.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
C.Na在空气中加热生成 ,Li在空气中加热也生成 ,Li在空气中加热也生成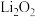 |
D. 溶解度大于 溶解度大于 , , 的溶解度也大于 的溶解度也大于 |
您最近半年使用:0次
2024-01-11更新
|
213次组卷
|
2卷引用:重庆市第一中学校2023-2024学年高一下学期3月定时练习化学试题
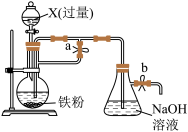
3 . 某同学欲利用如图所示装置制取能较长时间存在的 。下列分析错误的是
。下列分析错误的是
 。下列分析错误的是
。下列分析错误的是
A.反应结束后若关闭止水夹b和分液漏斗的活塞,则 可较长时间存在 可较长时间存在 |
| B.实验开始时应先打开止水夹a、b,再向烧瓶中加入X |
| C.实验所用溶液应现配现用且配制溶液所用的蒸馏水需要先加热煮沸后迅速冷却 |
| D.X可以是稀硫酸、稀硝酸或稀盐酸 |
您最近半年使用:0次
2023-10-09更新
|
203次组卷
|
2卷引用:重庆市梁平区2023-2024学年高三上学期第一次调研考试化学试题
4 . 某化学兴趣小组对绿矾(FeSO4•xH2O)的性质进行探究,进行以下实验:
(1)绿矾溶液的性质:取少量绿矾样品,在试管中加水溶解,滴加KSCN溶液,无明显现象。在空气中用力振荡后静置,溶液逐渐变红,由此可得出结论___________ (用离子方程式解释)
(2)将绿矾(FeSO4•xH2O)溶于水,加入氢氧化钠溶液,白色沉淀很快变成了灰绿色,最后变成了红褐色,请用化学方程式解释沉淀颜色变化的原因___________ 。
(3)测定绿矾中结晶水的含量:称量两端带开关K1和K2的石英玻璃管(装置A)的质量,记为m1g。向石英玻璃管中装入一定量的样品,再次称量装置A的质量,记为m2g。按如图连接好装置进行实验(夹持仪器已略去)。
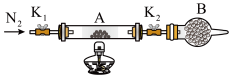
①仪器B的名称是___________ ;
②实验时下列操作步骤次序正确的是:d→a→____→____→____→e(填标号)________ ;重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d. 打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③实验前通入氮气的目的是______________ ,实验时,如果按a→d→∙∙∙的次序操作,则x的测定结果___________ (填“偏大”、“偏小”或“无影响”)。
(4)据古籍记载,焙烧绿矾( )能制备铁红。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
)能制备铁红。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
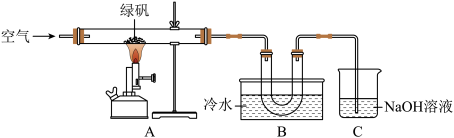
若绿矾在空气中充分焙烧的过程中只生成一种酸性气体,则焙烧发生的化学方程式为______ 。
(1)绿矾溶液的性质:取少量绿矾样品,在试管中加水溶解,滴加KSCN溶液,无明显现象。在空气中用力振荡后静置,溶液逐渐变红,由此可得出结论
(2)将绿矾(FeSO4•xH2O)溶于水,加入氢氧化钠溶液,白色沉淀很快变成了灰绿色,最后变成了红褐色,请用化学方程式解释沉淀颜色变化的原因
(3)测定绿矾中结晶水的含量:称量两端带开关K1和K2的石英玻璃管(装置A)的质量,记为m1g。向石英玻璃管中装入一定量的样品,再次称量装置A的质量,记为m2g。按如图连接好装置进行实验(夹持仪器已略去)。

①仪器B的名称是
②实验时下列操作步骤次序正确的是:d→a→____→____→____→e(填标号)
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d. 打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③实验前通入氮气的目的是
(4)据古籍记载,焙烧绿矾(
 )能制备铁红。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
)能制备铁红。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
若绿矾在空气中充分焙烧的过程中只生成一种酸性气体,则焙烧发生的化学方程式为
您最近半年使用:0次
名校
5 . 某兴趣小组研究合铁元素的盐类物质的性质、制备。
实验I.通过 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
(1)实验ⅰ中滴加NaOH溶液后出现的一系列现象是___________ ;
(2)探究实验ⅱ中滴加 溶液时实验现象为
溶液时实验现象为___________ ;其反应的离子方程式为___________ ;加碱后溶液无明显变化的原因___________ 。
实验II.高铁酸钠( ,
, )是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
)是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:

(3) 中铁元素的化合价为
中铁元素的化合价为___________
(4)“氧化”过程的反应体系中共存在下列6种粒子: 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ ;当有 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为___________  。
。
(5)产品经干燥后得到纯品 ,则
,则 的产率为
的产率为___________ (保留两位有效数字)。[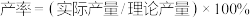 。一般以百分数表示]
。一般以百分数表示]
实验I.通过
 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
的性质实验,探究试剂添加顺序的不同对现象和反应的影响。| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
 | 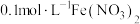 溶液 溶液 | 实验ⅰ: 先滴加 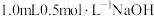 溶液; 溶液;再滴加 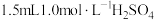 溶液 溶液 | i.滴加NaOH溶液后___________;加酸后溶液变为黄色 |
| 实验ⅱ: 先滴加 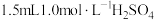 溶液; 溶液;再滴加 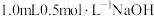 溶液 溶液 | ii.滴加 溶液时___________;加碱后溶液无明显变化 溶液时___________;加碱后溶液无明显变化 | ||
(2)探究实验ⅱ中滴加
 溶液时实验现象为
溶液时实验现象为实验II.高铁酸钠(
 ,
, )是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
)是一种新型绿色消毒剂,主要应用于饮用水处理,工业制备高铁酸钠有多种方法,下图是实验室模拟制备高铁酸钠的流程:
(3)
 中铁元素的化合价为
中铁元素的化合价为(4)“氧化”过程的反应体系中共存在下列6种粒子:
 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式
,写出该反应的离子方程式 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为 。
。(5)产品经干燥后得到纯品
 ,则
,则 的产率为
的产率为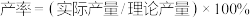 。一般以百分数表示]
。一般以百分数表示]
您最近半年使用:0次
名校
6 . 类比推理是化学中常用的思维方法,下列推理正确的是
| A.CO2与CaCl2溶液不反应,推测CO2与Ca(NO3)2溶液也不反应 |
| B.CaCO3的溶解度小于Ca(HCO3)2,推测Na2CO3的溶解度小于NaHCO3 |
| C.电解熔融氯化镁可制备金属镁,推测电解熔融氯化铝可制备金属铝 |
| D.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
您最近半年使用:0次
7 . 关于 的实验室制备,下列说法不正确的是
的实验室制备,下列说法不正确的是

 的实验室制备,下列说法不正确的是
的实验室制备,下列说法不正确的是
A.常用煮沸的方法除去NaOH溶液中的 |
| B.将苯换成酒精同样可以达到隔绝空气的作用 |
C.该反应的离子方程式为: |
| D.氢氧化亚铁是难溶于水的白色沉淀 |
您最近半年使用:0次
8 . 铁、铝的混合物进行如下实验:

(1)操作X的名称是____________ ;
(2)气体A是____________ (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成_____________ (填化学式),A在该反应中作为_____________ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH-外还有____________________ (填离子符号),溶液D中存在的金属离子为__________________ (填离子符号);
(5)加入稀盐酸发生反应的离子方程式为:________________________ ;
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:__________________________ 。

(1)操作X的名称是
(2)气体A是
(3)A与Cl2混合光照可能发生爆炸,生成
(4)溶液B中阴离子除OH-外还有
(5)加入稀盐酸发生反应的离子方程式为:
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:
您最近半年使用:0次
名校
解题方法
9 . 某实验小组探究NiO能否催化NO和CO反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是


 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
A.从理论上推断, 与 与 生成 生成 和 和 的反应,高温有利于自发进行 的反应,高温有利于自发进行 |
B.在空气中加热 可制备NiO 可制备NiO |
C.打开装置1中气球,通过观察气体是否变为红棕色判断是否生成 |
D.若以上实验证明 能够成功催化该反应,且固体A是 能够成功催化该反应,且固体A是 ,则装置2中的反应方程式为: ,则装置2中的反应方程式为: |
您最近半年使用:0次
2022-11-28更新
|
338次组卷
|
5卷引用:重庆2023届拔尖强基联合11月定时检测化学试题
重庆2023届拔尖强基联合11月定时检测化学试题重庆市西南大学附属中学校2022-2023学年高三上学期11月拔尖强基联合定时检测化学试题四川外国语大学附属外国语学校2024届高三上学期10月月考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)湖北省荆州中学2023-2024学年高三上学期10月半月考化学试题
名校
解题方法
10 . 以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
i、从废液中提纯并结晶出FeSO4·7H2O,并将其配成溶液。
ii、FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
iii、将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
iv、煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中会发生分解。
(1)步骤i从废液中提纯并结晶出FeSO4·7H2O的主要操作为___________ 、过滤、洗涤、干燥。
(2)步骤ii中,生成FeCO3的化学方程式是___________ 。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色[Fe(OH)3],写出发生反应的化学方程式是___________ 。
(3)步骤iii中,过滤需要使用到的玻璃仪器有___________ ;通过检验SO 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入___________ ,若___________ ,证明沉淀已经洗涤干净。
(4)已知煅烧FeCO3的化学方程式是4FeCO3+O2 2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是___________ kg。
i、从废液中提纯并结晶出FeSO4·7H2O,并将其配成溶液。
ii、FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
iii、将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体。
iv、煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中会发生分解。
(1)步骤i从废液中提纯并结晶出FeSO4·7H2O的主要操作为
(2)步骤ii中,生成FeCO3的化学方程式是
(3)步骤iii中,过滤需要使用到的玻璃仪器有
 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入(4)已知煅烧FeCO3的化学方程式是4FeCO3+O2
 2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是
您最近半年使用:0次



